Clear Sky Science · fr
L’axe adipocyte-STAT3-ANGPT2-PTGIS favorise les métastases cutanées du cancer du sein et constitue une voie ciblable
Pourquoi la dissémination cutanée du cancer du sein importe
Lorsque le cancer du sein se propage, la plupart des gens pensent aux os, au foie ou aux poumons. Pourtant, pour de nombreux patients, le cancer réapparaît dans un endroit inattendu : la peau de la paroi thoracique, parfois des années après l’ablation de la tumeur initiale. Ces nodules cutanés persistants et douloureux ne sont pas qu’un problème esthétique : ils signalent une maladie agressive et difficile à traiter. Cette étude explore pourquoi certains cancers du sein sont attirés par la peau et révèle un partenariat surprenant entre les cellules cancéreuses, le tissu adipeux voisin et les vaisseaux sanguins et lymphatiques qui nourrissent les tumeurs.
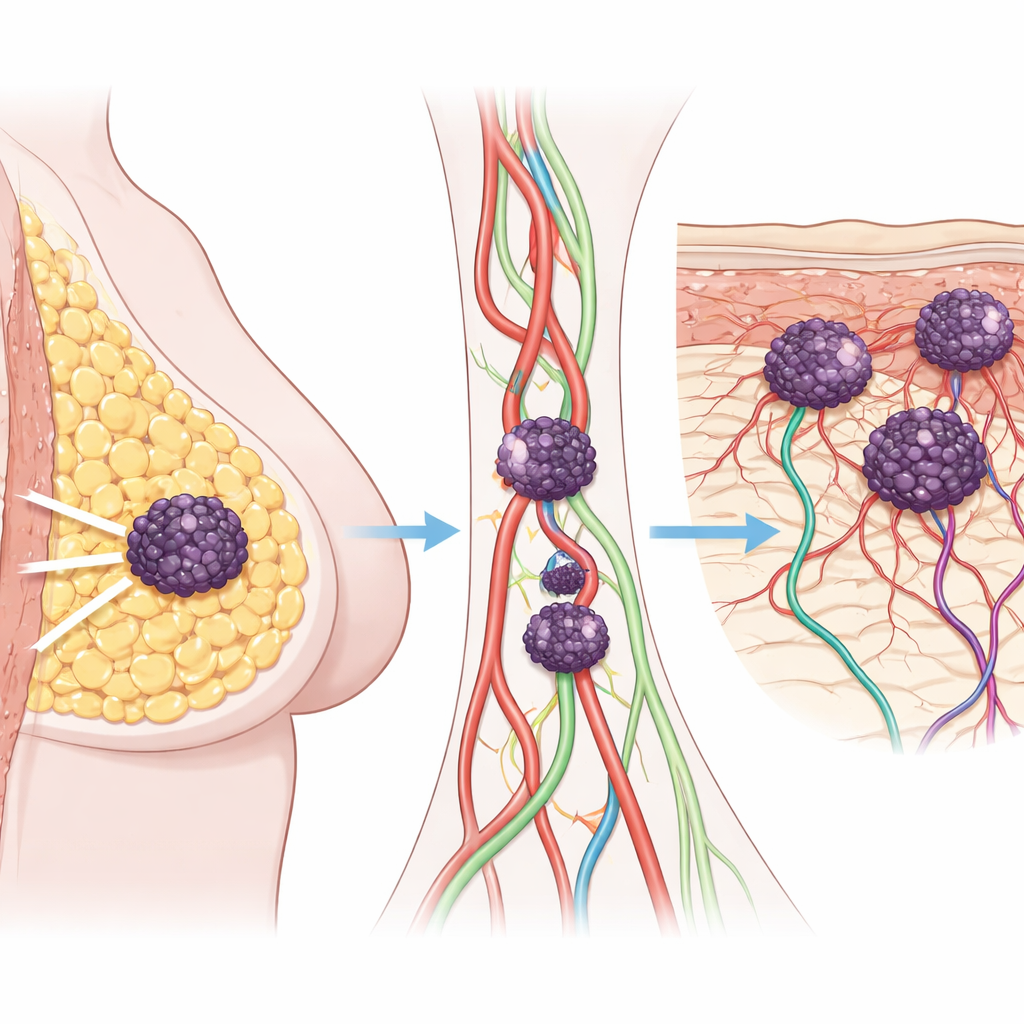
Les tumeurs cutanées comme signe d’alerte
Les chercheurs ont d’abord examiné les dossiers médicaux de 126 personnes atteintes d’un cancer du sein, en comparant celles qui n’ont jamais rechuté, celles dont le cancer s’est propagé à des organes comme le poumon ou l’os, et celles qui ont développé des métastases cutanées. Les patientes dont la maladie est réapparue uniquement au niveau de la peau présentaient déjà des tumeurs plus avancées et à croissance rapide au moment du diagnostic. Leurs cancers montraient des taux élevés de division cellulaire et une invasion précoce des vaisseaux sanguins et lymphatiques. Même si certaines de ces patientes ne présentaient pas de dissémination visible vers des organes distants, leur survie globale et leur survie sans maladie étaient moins bonnes que celles des patientes sans atteinte cutanée, soulignant que la métastase cutanée désigne une forme particulièrement agressive du cancer du sein.
Vaisseaux sanguins et tissu adipeux façonnent le niche cutanée
Pour comprendre ce qui rend la peau si fertile, l’équipe a suivi un patient sur plusieurs années, prélevant des échantillons de la tumeur mammaire initiale puis des nodules cutanés ultérieurs. Au microscope, les lésions mammaires et cutanées étaient remplies de nouveaux vaisseaux sanguins et lymphatiques — de petites autoroutes qui aident les cellules cancéreuses à voyager et à s’implanter. Le profilage de l’activité génique a montré qu’à mesure que la maladie progressait, les tumeurs activaient des réseaux entiers liés à la croissance des vaisseaux, à l’inflammation et au métabolisme des graisses et des acides gras. En particulier, les voies de dégradation de graisses alimentaires courantes, comme l’acide arachidonique et l’acide linoléique, devenaient plus actives, suggérant que le carburant fourni par les lipides et les couches graisseuses de la peau participe à l’évolution tumorale.
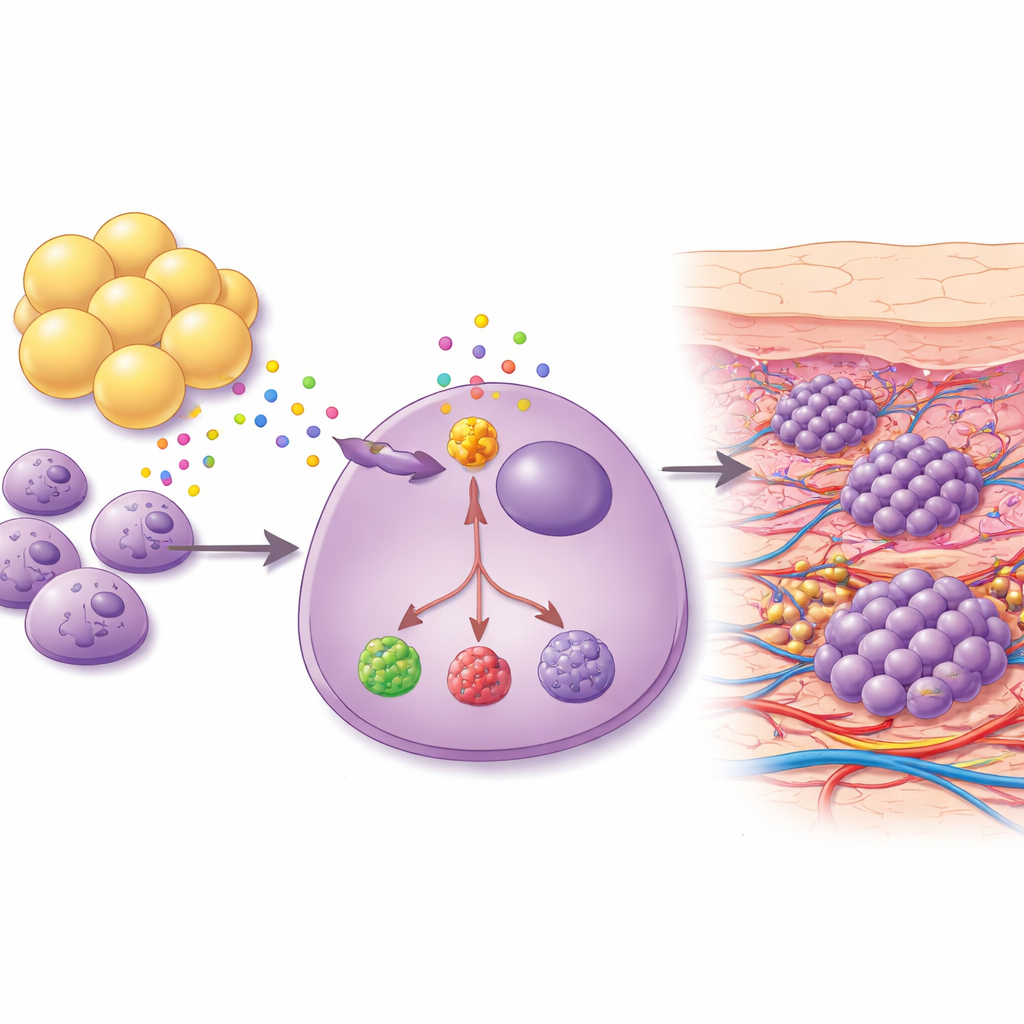
Les adipocytes envoient de puissants signaux de croissance
Étant donné que le sein et la paroi thoracique sous-jacente sont riches en graisse, les scientifiques se sont demandés si les adipocytes eux-mêmes pouvaient inciter les cellules cancéreuses à migrer vers la peau. Ils ont cultivé des cellules de cancer du sein avec des adipocytes — des cellules graisseuses matures — provenant du même patient et ont collecté le mélange de molécules sécrété par ces adipocytes. Ce cocktail a fortement stimulé la capacité des cellules des vaisseaux sanguins à former des structures tubulaires en laboratoire, un signe caractéristique d’angiogenèse. Chez la souris, l’exposition des tumeurs au liquide dérivé des adipocytes a entraîné une nouvelle croissance tumorale dans des zones riches en peau et en graisse, comme le cou et le dos. Les cellules cancéreuses prélevées sur ces lésions cutanées étaient plus de type souche, plus résistantes à la mort cellulaire et produisaient des niveaux plus élevés de facteurs pro-croissance et pro-inflammatoires, y compris une protéine appelée ANGPT2 et une enzyme métabolique nommée PTGIS.
Un interrupteur de signalisation qui peut être désactivé
En approfondissant l’analyse, l’équipe a comparé les cellules tumorales ordinaires à leurs homologues à tendance cutanée et a constaté qu’une voie de communication intracellulaire courante — la voie JAK–STAT — était fortement activée, en particulier la protéine STAT3. Une fois activé, STAT3 agissait comme un contrôleur maître, augmentant ANGPT2, VEGFC (un moteur de la croissance des vaisseaux lymphatiques) et PTGIS, qui favorisent tous la formation de vaisseaux sanguins et le remodelage du microenvironnement tumoral. Le blocage de STAT3 avec un médicament appelé Stattic a réduit la croissance des tumeurs cutanées chez la souris et diminué les niveaux de ces facteurs en aval. Dans les échantillons tumoraux de patients, une activité élevée de STAT3, ANGPT2 et PTGIS était associée à une moins bonne survie sans progression et sans maladie, et ces marqueurs étaient particulièrement élevés chez les patients dont les métastases se limitaient à la peau.
Ce que cela signifie pour les patients
Ensemble, ces travaux décrivent le cancer du sein métastatique cutané comme un sous-type distinct et dangereux alimenté par une interaction à trois voies entre les cellules cancéreuses, la graisse environnante et les vaisseaux qui nourrissent les tumeurs. Les signaux provenant des adipocytes activent STAT3 à l’intérieur des cellules cancéreuses, ce qui, à son tour, augmente ANGPT2 et PTGIS et reconfigure le métabolisme des acides gras, faisant de la peau une niche accueillante où les tumeurs peuvent s’implanter et se développer. Pour les patients, cela signifie que les métastases cutanées ne sont pas simplement des récidives « locales », mais un marqueur d’une biologie agressive. Côté optimiste, la même voie qui pilote ce processus pourrait aussi être sa faiblesse : des médicaments ciblant STAT3 ou des enzymes métaboliques clés comme PTGIS pourraient, à l’avenir, aider à couper les lignes de soutien permettant au cancer du sein de coloniser la peau.
Citation: Luo, CW., Ou-Yang, F., Chang, SJ. et al. Adipocyte-driven STAT3-ANGPT2-PTGIS axis promotes cutaneous metastasis in breast cancer and represents a targetable pathway. npj Precis. Onc. 10, 111 (2026). https://doi.org/10.1038/s41698-025-01184-1
Mots-clés: métastase cutanée du cancer du sein, microenvironnement tumoral, signalisation des adipocytes, voie STAT3, angiogenèse