Clear Sky Science · fr
Méthodes pour une évaluation randomisée, en aveugle et contrôlée des interventions présumées contre la maladie dans des réseaux d’évaluation préclinique multi-laboratoires
Pourquoi cela compte pour la santé quotidienne
De nombreux traitements prometteurs semblent efficaces dans les études animales, puis échouent dans de vastes essais cliniques coûteux. Cet article montre, de façon concrète, comment les scientifiques peuvent repenser ces premiers tests animaux pour que leurs résultats soient plus fiables et aient davantage de chances de prédire ce qui se passera chez les patients réels — en prenant l’AVC comme cas d’étude. 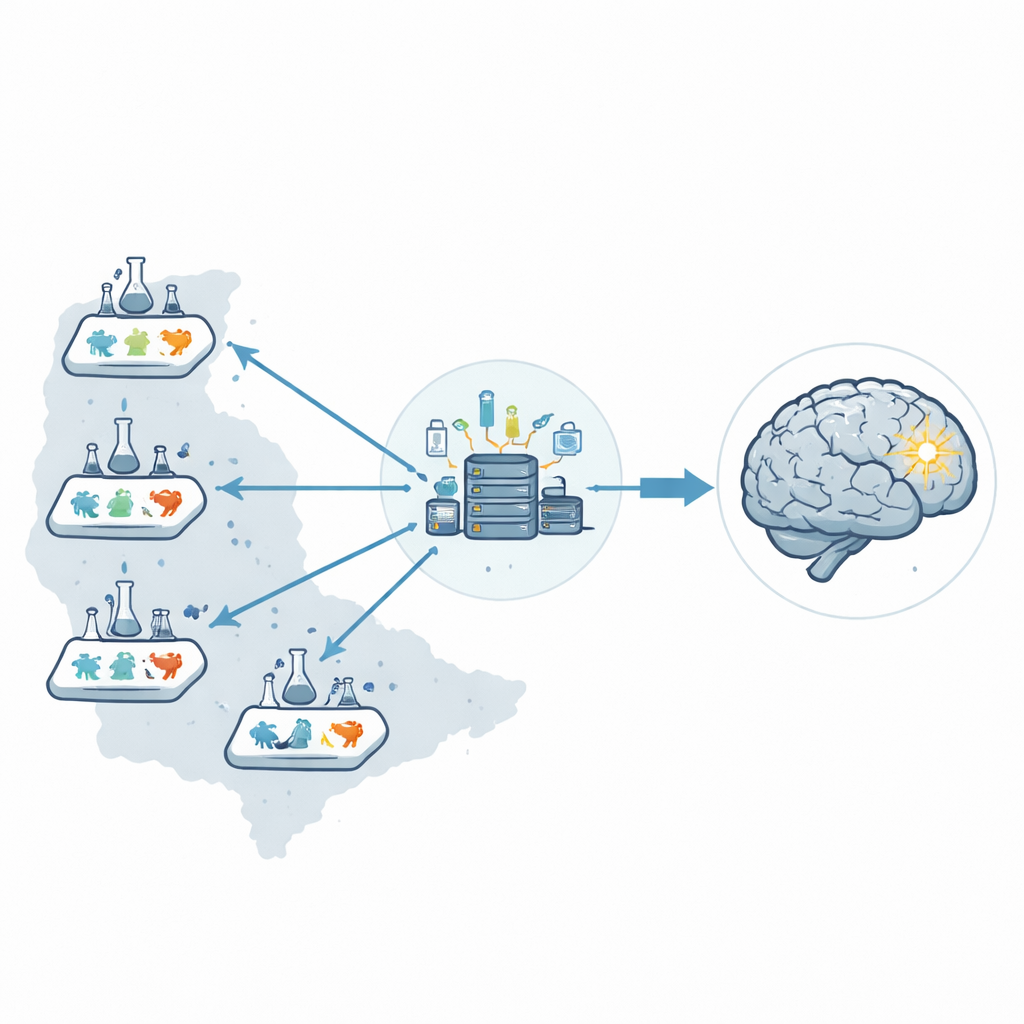
Construire un réseau plutôt qu’un seul laboratoire
Plutôt que de s’appuyer sur un seul laboratoire, les chercheurs ont créé un réseau préclinique de six laboratoires aux États-Unis, appelé Stroke Preclinical Assessment Network. Un centre de coordination central gérait l’ensemble de l’opération : expédition des flacons de médicament codés, attribution aléatoire des traitements, réception de toutes les données et réalisation des analyses statistiques. En séparant ces rôles des personnes réalisant les interventions chirurgicales ou évaluant les résultats, ils ont réduit le risque que les attentes humaines influencent subtilement les résultats.
Mettre en pratique l’équité et la dissimulation
Pour imiter les règles d’un bon essai clinique, chaque animal était inclus, étiqueté et suivi dès son arrivée au laboratoire. Les traitements étaient dissimulés dans des flacons identiques afin que les chirurgiens ne puissent pas distinguer les médicaments réels des placebos pendant l’induction de l’AVC et l’administration des soins. Un plan de randomisation structuré a assuré que les mâles et femelles, les différents modèles d’AVC et les six sites contribuaient de manière équilibrée à chaque groupe de traitement. Même si un animal mourait ou qu’une procédure échouait, il restait dans l’enregistrement afin que les pertes ne puissent pas être ignorées discrètement, ce qui aide à éviter les biais cachés.
Tester les traitements dans des modèles d’AVC réalistes
Le réseau a utilisé cinq modèles de rongeurs différents qui, ensemble, capturaient des aspects importants de l’AVC humain, notamment l’âge, l’hypertension et l’obésité induite par l’alimentation. L’AVC était reproduit de la même manière sur tous les sites en bloquant brièvement une artère cérébrale majeure, puis en restaurant le flux sanguin — similaire aux procédures modernes d’extraction de caillot chez l’homme. Les animaux recevaient l’un des six traitements candidats protecteurs ou un contrôle correspondant. L’équipe les a ensuite suivis avec des tests de mouvement simples, tels que leur façon de tourner dans un coin ou de marcher sur une grille, et avec des imageries cérébrales pour mesurer la taille de la lésion sur 30 jours.
Notation en aveugle, données partagées et statistiques intelligentes
Pour garder les jugements impartiaux, les tests comportementaux étaient filmés et téléversés dans une archive centrale. Ces vidéos, dépourvues de toute information d’identification, étaient envoyées à des évaluateurs formés dans d’autres laboratoires, qui les notaient sans savoir quel traitement l’animal avait reçu ni où il avait été testé. Les images par résonance magnétique étaient traitées via un pipeline d’analyse automatisé qui segmentait le cerveau et la zone de lésion avec une intervention humaine minimale. Tous les résultats alimentaient un plan statistique multi-bras et en plusieurs étapes permettant de tester plusieurs traitements en parallèle : les candidats faibles ou clairement inefficaces pouvaient être éliminés tôt, tandis que les options prometteuses continuaient vers les étapes ultérieures. 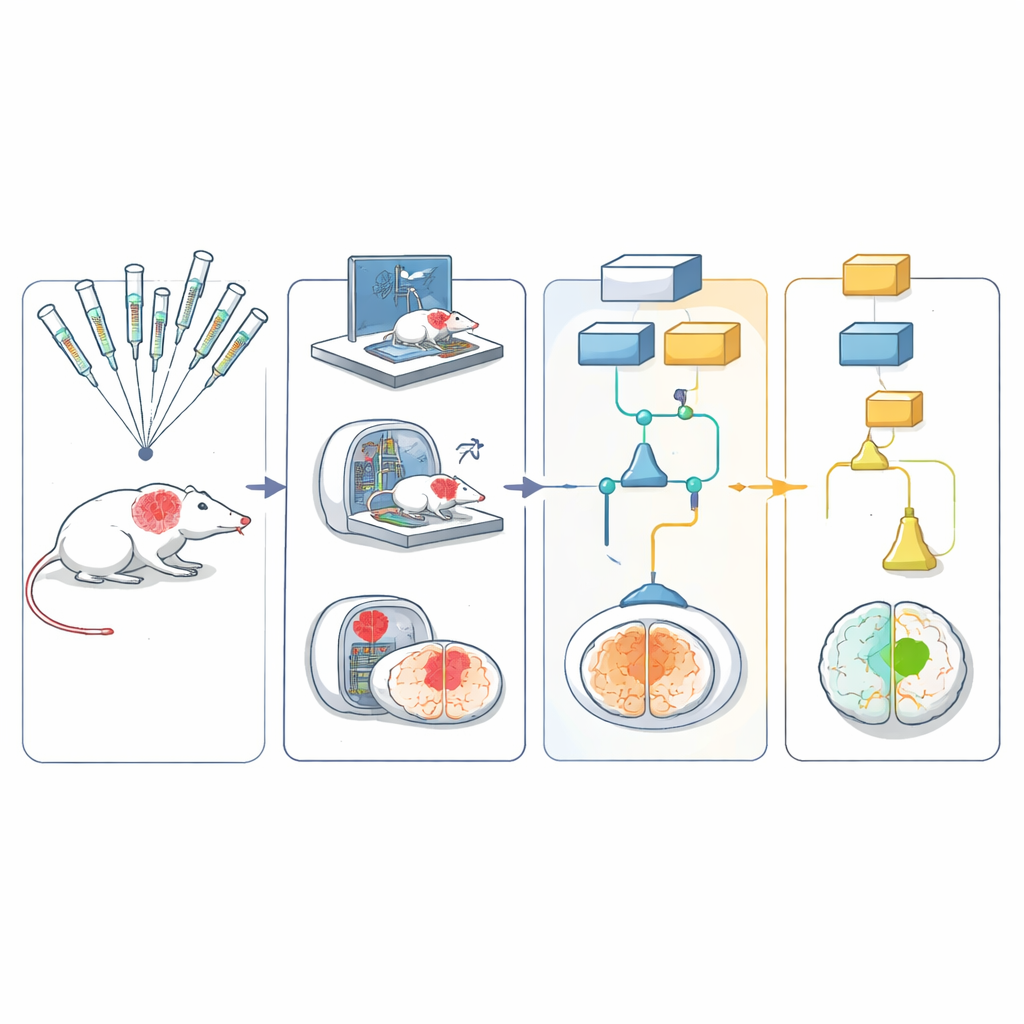
Ce que les résultats ont révélé sur les thérapies contre l’AVC
Sur quatre étapes et 2 615 animaux, le système s’est avéré opérationnel même pendant les perturbations liées à la pandémie de COVID-19. Les méthodes ont constamment maintenu l’équilibre entre les groupes de traitement, minimisé les erreurs de dosage et montré une amélioration de la qualité des données à mesure que les sites progressaient sur la courbe d’apprentissage. Au final, cinq des six traitements ont été écartés, tandis qu’un seul — l’acide urique, un capteur de radicaux libres — a atteint le seuil prédéfini de bénéfice. Parallèlement, le travail a mis en évidence des limites de certains modèles populaires, comme des taux de mortalité très élevés chez des souris âgées, suggérant qu’ils peuvent ne pas être pratiques ou réalistes pour des études futures.
Vue d’ensemble : un modèle pour une science préclinique plus fiable
Pour un lecteur non spécialiste, le message clé est que la manière dont nous testons les traitements chez l’animal importe autant que ce que nous testons. En important dans la recherche animale les garde-fous des essais cliniques modernes — randomisation, aveuglement, comptabilisation complète de chaque sujet et statistiques rigoureuses — ce réseau montre que les premières études peuvent être à la fois plus rigoureuses et plus efficaces. Le manuel détaillé qu’ils fournissent peut être adapté à d’autres maladies, offrant une voie vers des résultats de laboratoire capables de résister à la réplication et donnant aux médecins, aux patients et aux financeurs davantage de confiance qu’un traitement a réellement une chance de fonctionner en clinique.
Citation: Lamb, J., Nagarkatti, K., Diniz, M.A. et al. Methods for randomized, blinded, controlled evaluation of putative disease interventions in multilaboratory, preclinical assessment networks. Lab Anim 55, 74–82 (2026). https://doi.org/10.1038/s41684-026-01683-z
Mots-clés: accident vasculaire cérébral, essais précliniques, modèles animaux, rigueur de la recherche, études multicentriques