Clear Sky Science · fr
Transgénèse médiée par PiggyBac et knockout CRISPR–Cas9 chez la grande mite de cire, Galleria mellonella
Une minuscule chenille au grand potentiel médical
Imaginez tester de nouveaux antibiotiques ou étudier des infections dangereuses sans recourir à des souris ou à d’autres mammifères. Les larves de la grande mite de cire, Galleria mellonella, émergent comme un substitut peu coûteux et d’un intérêt éthique pour ce type d’expériences. Cette étude montre comment des scientifiques ont franchi une étape majeure en dotant ces chenilles des mêmes outils génétiques qui ont rendu la drosophile et le poisson zèbre si précieux pour la recherche biomédicale.
Pourquoi cet insecte compte pour la santé humaine
Les larves de Galleria mellonella reproduisent de façon surprenante certaines réponses physiologiques humaines aux agents pathogènes. Elles peuvent être maintenues à 37 °C — la température du corps humain — et peuvent être infectées par une large gamme de bactéries et de champignons d’importance médicale. Lorsqu’elles tombent malades, leur corps noircit par un processus appelé mélanisation, offrant aux chercheurs un indicateur visible de l’état de santé. Étant des invertébrés, elles évitent de nombreux obstacles juridiques et éthiques associés aux travaux sur des vertébrés, et elles sont peu coûteuses à élever en grand nombre. On a même découvert que les larves peuvent dégrader des plastiques courants, ce qui suggère des usages en recherche environnementale.
La boîte à outils génétique manquante
Malgré ces avantages, les larves de mite de cire manquaient des outils génétiques sophistiqués disponibles chez les animaux de laboratoire classiques. Au cours de la dernière décennie, plusieurs équipes ont séquencé le génome de la mite et catalogué ses gènes et protéines exprimés, mais les chercheurs ne pouvaient pas facilement activer ou désactiver des gènes ni ajouter des marqueurs utiles. Cette lacune limitait les usages du modèle — par exemple, construire des animaux qui s’illuminent lors d’une infection, ou supprimer des gènes précis pour tester leur rôle dans l’immunité. L’article actuel aborde directement ce problème en adaptant deux systèmes puissants d’ingénierie génétique, connus sous les noms PiggyBac et CRISPR–Cas9, pour une utilisation chez Galleria mellonella.
Construire des larves rapporteurs qui brillent dans l’obscurité
L’équipe a d’abord étudié la chronologie du développement embryonnaire précoce de la mite et a identifié une fenêtre d’environ six heures après la ponte pendant laquelle tous les noyaux en division partagent encore un cytoplasme commun. Injecter de l’ADN durant cette période permet au matériel génétique d’être transmis à tous les tissus ultérieurs, y compris les futurs spermatozoïdes et ovules. Profitant de cette fenêtre, les chercheurs ont introduit des constructions d’ADN basées sur le transposon PiggyBac, un élément « couper‑coller » qui insère de larges fragments d’ADN dans le génome. Après avoir testé différents plasmides auxiliaires, ils ont identifié une version portant une enzyme PiggyBac hyperactive qui a permis d’obtenir des lignées transgéniques. Ces larves exprimaient des protéines fluorescentes vertes et rouges dans des tissus corporels distincts, et l’analyse de l’ADN a montré que la cassette génétique s’était insérée dans une région neutre entre des gènes natifs.
Observer les cellules et supprimer des gènes
Puis, les auteurs ont créé des lignées rapporteurs plus spécialisées. Une construction a marqué une protéine structurale appelée tubuline par une fluorescence verte pour mettre en évidence le cytosquelette, tandis qu’une autre a fusionné un marqueur rouge à une histone qui enroule l’ADN dans le noyau. Ces lignées brillaient selon des motifs caractéristiques dans l’intestin, le tissu adipeux, les glandes à soie et d’autres tissus, permettant aux chercheurs de visualiser les structures cellulaires dans des larves vivantes ou fixées. Pour aller au‑delà de l’ajout de gènes et les rendre inactifs, l’équipe a utilisé CRISPR–Cas9. Ils ont injecté des complexes pré‑assemblés protéines–ARN CRISPR ciblant le marqueur fluorescent vert dans des embryons déjà porteurs de la cassette rapporteur. De nombreux descendants ont montré une perte partielle ou totale du signal vert tout en conservant la fluorescence rouge des yeux, et le séquençage de l’ADN a confirmé de petites insertions et délétions au site de coupure ciblé par CRISPR.
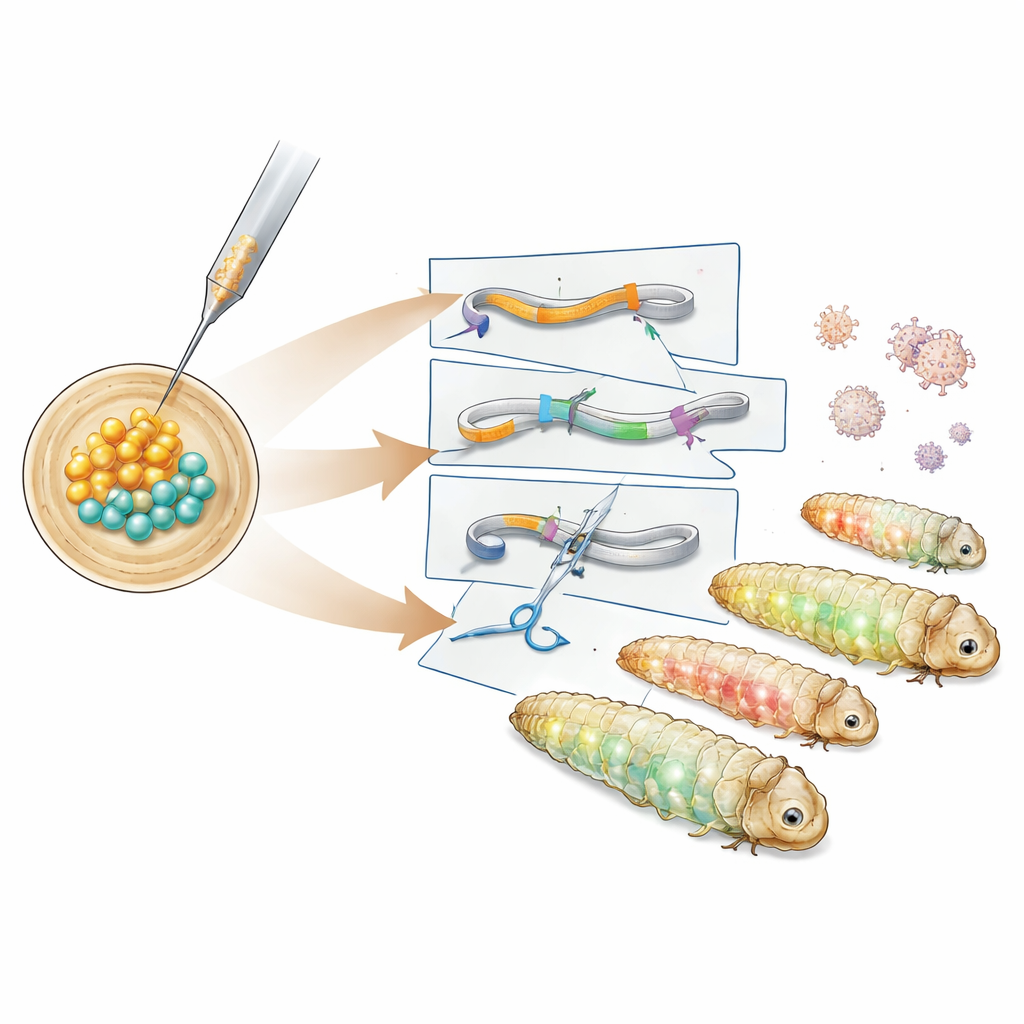
De l’avancée technique à l’impact pratique
Bien que l’efficacité de PiggyBac et de CRISPR chez ces mites reste modeste comparée à certains autres insectes, les auteurs décrivent des voies claires d’amélioration en ajustant les promoteurs, les variantes enzymatiques et les stratégies d’injection. Même dans sa forme actuelle, la boîte à outils est suffisante pour générer des lignées stables qui visualisent des composants cellulaires clés ou portent des knockouts géniques ciblés. Pour les non‑spécialistes, l’essentiel est que Galleria mellonella peut désormais être manipulée presque aussi souplement que des animaux de laboratoire mieux connus. Cela signifie que les chercheurs peuvent construire des chenilles qui signalent une infection, modélisent des aspects de maladies humaines ou testent de nouveaux médicaments de façon plus rapide, moins coûteuse et plus humaine, réduisant potentiellement la dépendance aux modèles mammifères en biologie des infections et dans des domaines connexes.
Citation: Pearce, J.C., Campbell, J.S., Prior, J.L. et al. PiggyBac-mediated transgenesis and CRISPR–Cas9 knockout in the greater wax moth, Galleria mellonella. Lab Anim 55, 95–102 (2026). https://doi.org/10.1038/s41684-025-01665-7
Mots-clés: Galleria mellonella, modèle d’infection d’invertébré, génie génétique, transgénèse PiggyBac, knockouts CRISPR