Clear Sky Science · fr
Formation multiphase accrue de nitrate et de sulfate particulaires pilotée par le NO2 dans des conditions de forte humidité
Pourquoi l’air humide peut rester pollué
Beaucoup de gens s’imaginent que le temps humide et brumeux nettoie l’air en lessivant la pollution. Mais dans le sud de la Chine, l’inverse se produit souvent : lorsque l’air océanique chaud et humide rencontre de l’air continental plus froid, une brume épaisse s’installe même si les mécanismes atmosphériques classiques d’élimination sont faibles. Cette étude explique pourquoi, montrant comment un polluant courant du trafic, le dioxyde d’azote, alimente discrètement la formation rapide de particules fines nocives quand l’air est très humide.
Un air collant au-dessus d’une ville côtière
Les chercheurs se sont concentrés sur Xiamen, une ville côtière du sud de la Chine, durant deux semaines du début du printemps 2024. À cette période, l’air océanique chaud et humide entre fréquemment en collision avec de l’air continental plus froid et sec et stagne, créant des fronts quasi stationnaires. Lors de ces épisodes de forte humidité, l’air devient stagnant, les vents faiblissent et une couche d’air peu épaisse s’installe au-dessus de la ville. Les mesures d’une station de surveillance sur un toit ont montré que les niveaux de particules fines (PM2,5) augmentaient, la visibilité diminuait et du brouillard se formait souvent à mesure que l’humidité montait. Pendant ces périodes brumeuses, la composition chimique des particules évoluait en deux phases distinctes : d’abord les nitrates dominaient, puis les sulfates ont fortement augmenté.
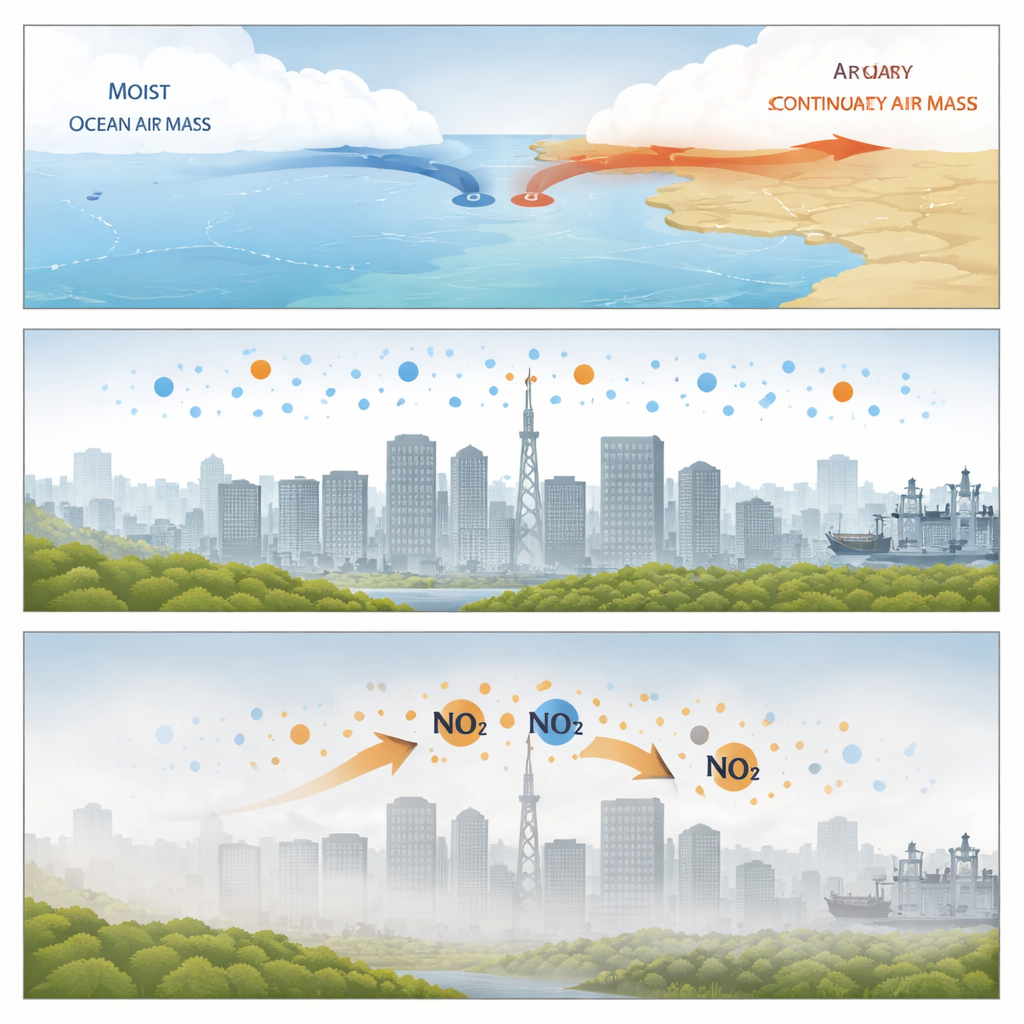
Deux phases d’une chimie cachée
Dans les premières heures très humides de ces épisodes, les particules sont devenues riches en nitrate, alors même que la chimie habituelle menée par la lumière solaire était faible et que les niveaux d’ozone étaient bas. L’équipe a constaté que la meilleure explication était l’absorption directe du dioxyde d’azote issu du trafic et d’autres sources par les surfaces humides des particules et par de minces films d’eau au sol. Dans ces gouttelettes concentrées, le dioxyde d’azote réagit plus rapidement que dans de l’eau ordinaire, produisant à la fois du nitrate et une autre forme réactive d’azote susceptible de retourner dans l’air. Le lien étroit entre le dioxyde d’azote, l’eau des aérosols, la surface des particules et la hausse des nitrates suggérait que ces processus de surface dominaient la production de nitrate la nuit.
Quand le brouillard transforme l’azote en particules de soufre
À mesure que l’humidité augmentait encore et que le brouillard se formait, la chimie changeait. Le sulfate, formé à partir du dioxyde de soufre, commençait à croître rapidement et pouvait même dépasser le nitrate. Là encore, le dioxyde d’azote jouait un rôle central, mais d’une façon différente. À l’intérieur des gouttes de brouillard et des grosses gouttelettes, le dioxyde d’azote et ses produits de réaction oxydent le soufre dissous au travers d’une série de réactions en milieu aqueux. Un intermédiaire clé, une espèce réactive d’azote en équilibre avec l’acide nitreux, a été observée rester plus longtemps dans les gouttes plus grosses et moins acides que dans les particules minuscules et plus acides. Ce temps de résidence prolongé lui permet d’attaquer de manière répétée le soufre dissous, entraînant une production rapide de sulfate précisément lorsque le brouillard épais et la brume sont présents.
Quantifier l’invisible
Pour tester ces idées, les auteurs ont construit un « modèle boîte » informatique détaillé combinant la chimie en phase gazeuse, les réactions en phase aqueuse et les échanges entre l’air et les particules. Lorsqu’ils ont autorisé l’absorption du dioxyde d’azote par les particules humides et les gouttelettes de brouillard, le modèle a reproduit de façon étroite les augmentations observées de nitrate et de sulfate. Pendant les épisodes humides, l’absorption directe du dioxyde d’azote expliquait près de la moitié de tout le nitrate formé, et les oxydants à base d’azote (le dioxyde d’azote et ses produits aqueux) produisaient presque les deux tiers du sulfate. La nuit, la voie impliquant le dioxyde d’azote dépassait largement la voie plus familière faisant intervenir un autre oxydant nocturne, le pentoxyde de diazote. Le modèle montrait également que les gouttes de brouillard, par leur plus grande taille et leur pH plus élevé, sont des réacteurs particulièrement favorables à la chimie azote–soufre qui génère du sulfate.
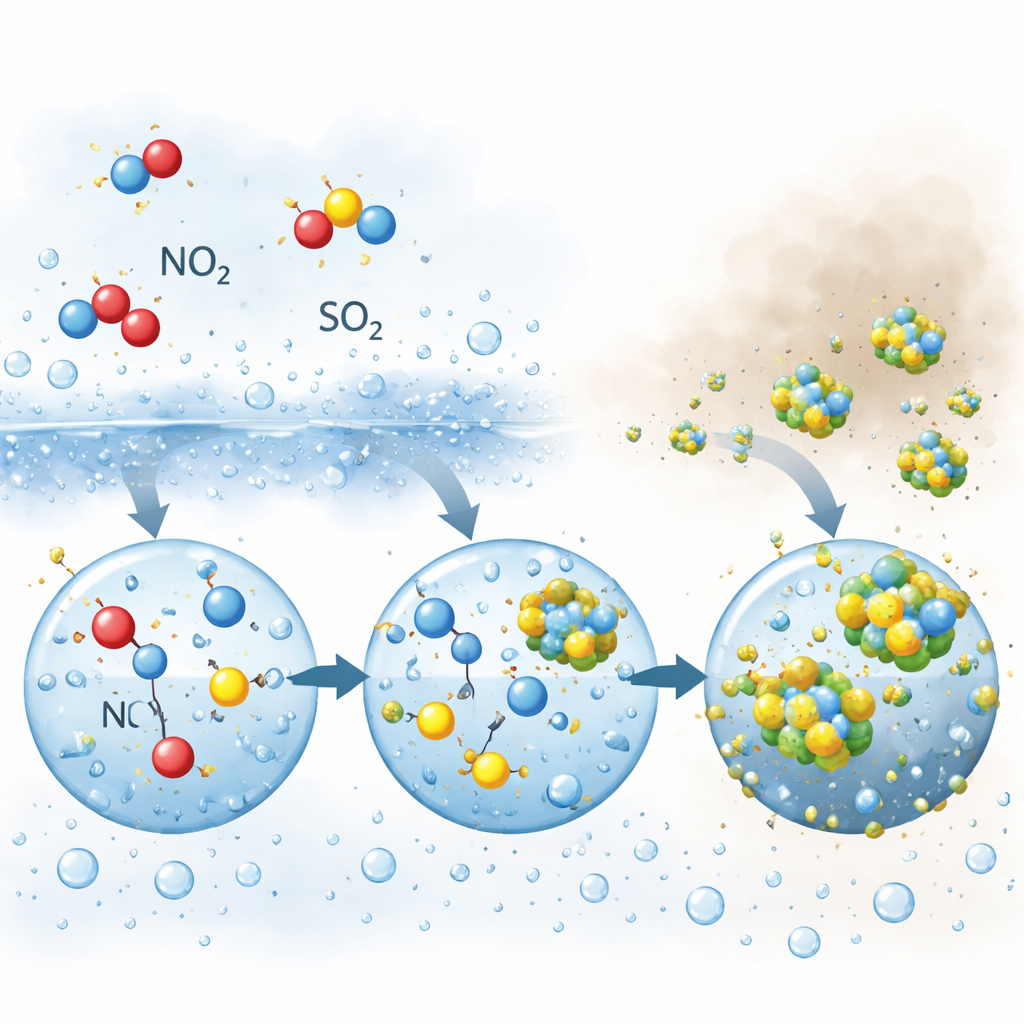
Ce que cela implique pour un air plus propre
L’étude conclut que le dioxyde d’azote fait bien plus que servir d’indicateur des émissions routières : dans des conditions très humides et stagnantes, il devient un puissant moteur de formation de particules fines. En accélérant la conversion de l’azote et du soufre gazeux en particules de nitrate et de sulfate, ces réactions aqueuses cachées contribuent à expliquer pourquoi les niveaux de particules n’ont pas diminué aussi rapidement que les émissions de gaz azotés et sulfurés en Chine. Les résultats suggèrent que le contrôle efficace du smog dans les régions côtières et humides doit prendre en compte non seulement les quantités de dioxyde d’azote émises, mais aussi la fréquence à laquelle l’atmosphère entre dans ces états collants et brumeux qui le transforment en une véritable usine chimique microscopique.
Citation: Lin, Z., Ji, X., Xu, L. et al. Enhanced NO2-driven multiphase formation of particulate nitrate and sulfate under high-humidity conditions. npj Clim Atmos Sci 9, 76 (2026). https://doi.org/10.1038/s41612-026-01352-5
Mots-clés: pollution de l’air, dioxyde d’azote, particules fines, haute humidité, chimie du brouillard