Clear Sky Science · fr
MiR-362-3p inhibe la prolifération, la migration et l’EMT des cellules du cancer gastrique en régulant la voie de signalisation DEP-1/ERK
Pourquoi cette recherche importe pour le cancer de l’estomac
Le cancer de l’estomac reste l’un des cancers les plus meurtriers au monde, en grande partie parce qu’il est souvent détecté tardivement et continue de se propager malgré la chirurgie et la chimiothérapie. Cette étude examine une toute petite molécule naturelle dans nos cellules qui joue un peu le rôle d’un interrupteur maître pour les cellules cancéreuses gastriques. En comprenant comment cet interrupteur ralentit la croissance et la mobilité tumorales, les chercheurs espèrent ouvrir de nouvelles voies pour un diagnostic plus précoce et des traitements plus ciblés et moins toxiques.
Un petit ARN aux grands effets
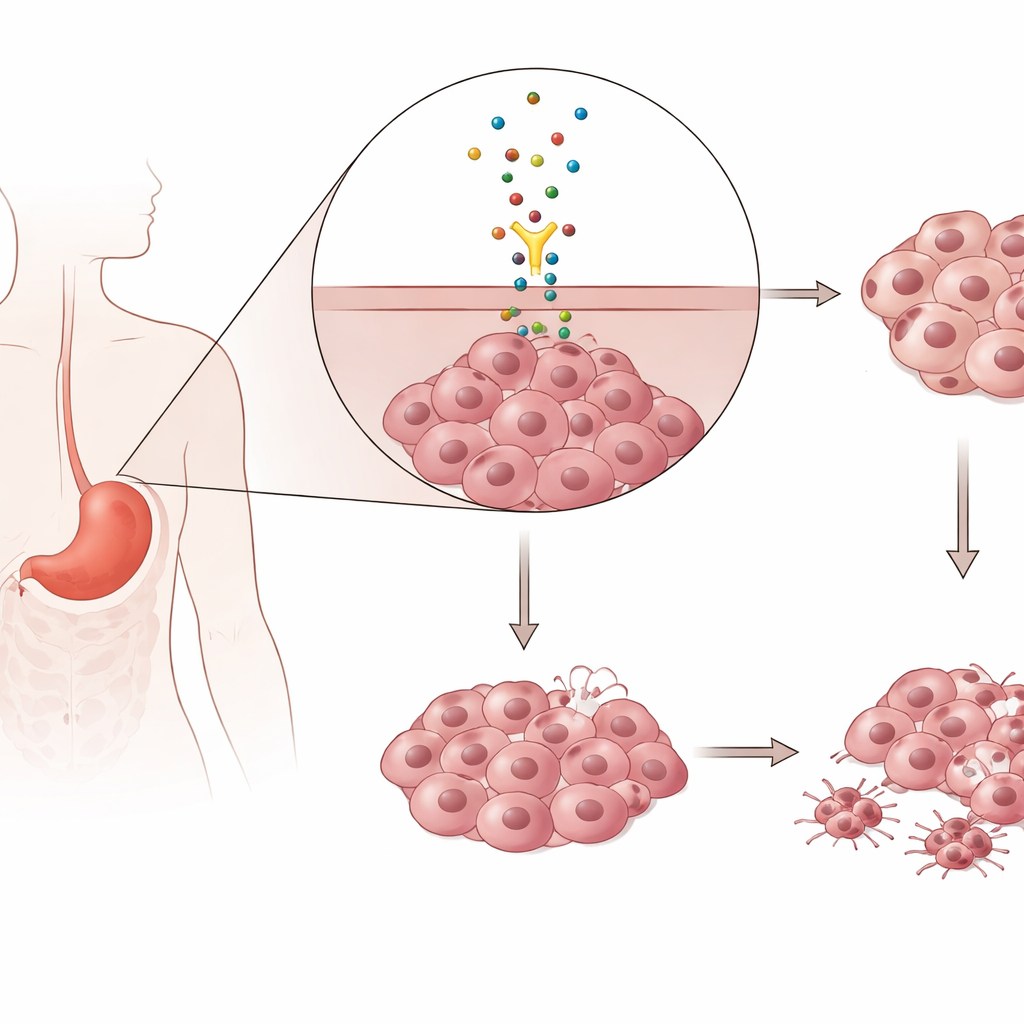
Nos cellules utilisent de courtes séquences d’acide nucléique appelées microARN comme des boutons de réglage fin de l’activité génique. Le microARN examiné ici, nommé miR-362-3p, avait déjà montré des comportements variables dans d’autres cancers, se comportant parfois comme un frein et parfois comme un accélérateur. Les auteurs ont voulu savoir ce qu’il fait dans le cancer gastrique. À l’aide de deux lignées cellulaires humaines de cancer de l’estomac cultivées en laboratoire, ils ont artificiellement augmenté ou diminué les niveaux de miR-362-3p puis observé le comportement des cellules en termes de croissance, de mobilité et de leur capacité à changer de forme et à devenir plus invasives.
Ralentir la croissance et la mobilité des cellules cancéreuses
Lorsque les chercheurs ont augmenté miR-362-3p dans les cellules du cancer gastrique, les cellules se sont divisées plus lentement et ont formé moins de colonies au fil du temps, montrant que ce microARN freine la prolifération cellulaire. Les cellules sont aussi devenues moins mobiles lors d’essais de cicatrisation et de migration, suggérant une moindre capacité à se propager. Au niveau moléculaire, l’ajout de miR-362-3p a modifié des marqueurs clés de l’identité cellulaire : les niveaux d’E-cadhérine, une protéine qui aide les cellules à rester groupées en une couche ordonnée, ont augmenté, tandis que la vimentine, associée à un état plus mobile et invasif, a diminué. Lorsque l’équipe a au contraire bloqué miR-362-3p, tous ces effets se sont inversés : croissance plus rapide, mobilité accrue et profil plus agressif, prédisposant aux métastases.
Identification de la cible moléculaire : DEP-1
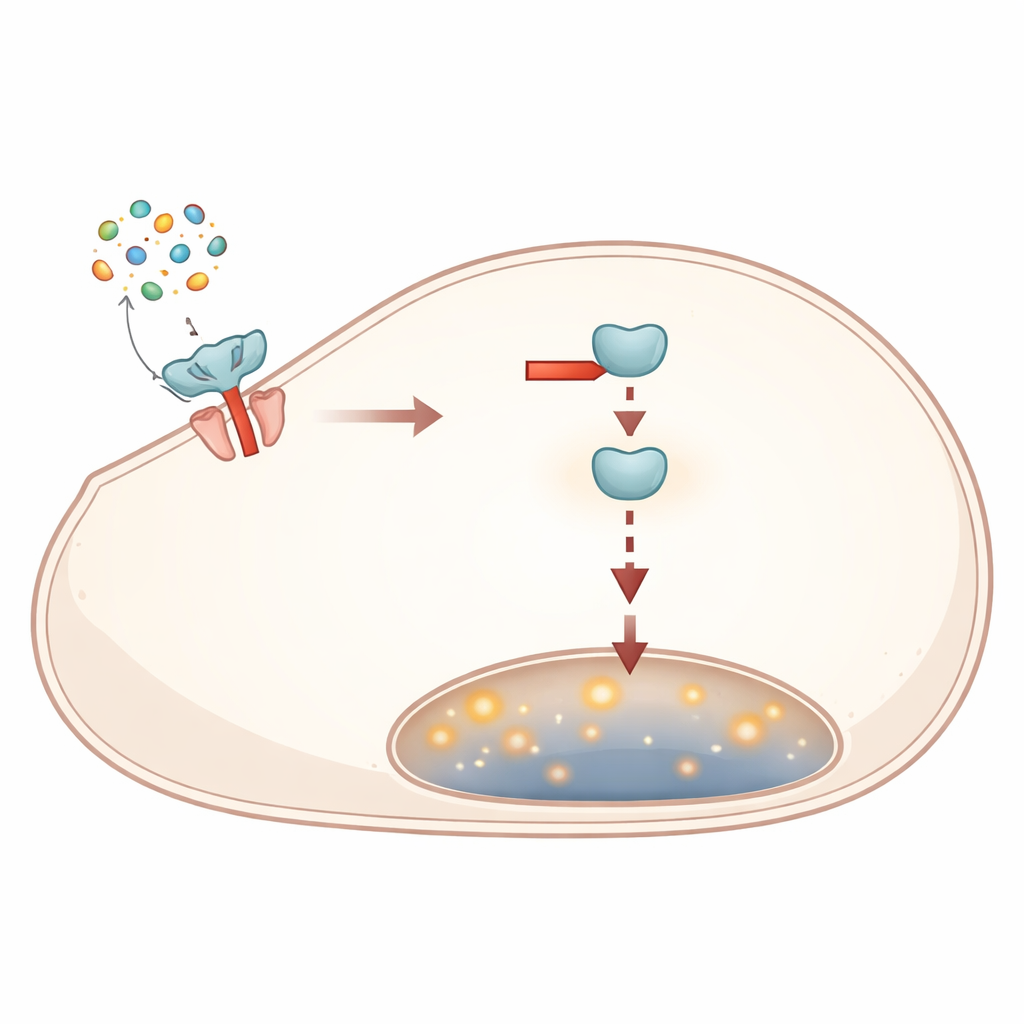
Pour expliquer comment un court brin d’ARN pouvait produire des effets aussi étendus, les scientifiques ont recherché dans des bases de données informatiques les gènes auxquels miR-362-3p pourrait se lier et silencier. Ils ont réduit la liste à une protéine appelée DEP-1, située à la surface cellulaire et qui relaie les signaux de croissance vers l’intérieur. Des expériences utilisant un système rapporteur ont montré que miR-362-3p se lie directement à l’extrémité 3’ du message génétique de DEP-1, réduisant ainsi sa production. Lorsque DEP-1 a été délibérément diminué par des outils génétiques, les cellules gastriques ont ralenti leur croissance et leur migration et ont présenté le même schéma d’augmentation d’E-cadhérine et de diminution de la vimentine observé avec des niveaux élevés de miR-362-3p. À l’inverse, forcer les cellules à produire plus de DEP-1 les a poussées à croître et à migrer de façon plus agressive, reproduisant ce qui se passe lorsque miR-362-3p est bloqué.
Perturbation d’une voie de signalisation clé de la croissance
DEP-1 est relié à une chaîne de signalisation interne connue sous le nom de voie ERK, que de nombreux cancers utilisent pour stimuler la division et la dissémination cellulaires. Les chercheurs ont mesuré la forme activée d’ERK dans leurs cellules de cancer gastrique et ont constaté que l’augmentation de miR-362-3p ou la diminution de DEP-1 atténuait l’activité d’ERK, tandis que la réduction de miR-362-3p ou l’augmentation de DEP-1 réactivait ERK. En aval, les niveaux de Cyclin D1 et c-Myc — des acteurs bien connus qui poussent les cellules à travers le cycle de division — ont également diminué lorsque miR-362-3p était élevé. Ensemble, ces résultats décrivent une logique simple : miR-362-3p réduit DEP-1, ce qui affaiblit la signalisation ERK et ses programmes pro-croissance, laissant les cellules cancéreuses moins aptes à se multiplier et moins enclines à se détacher et migrer.
Implications et perspectives
Pour le grand public, l’essentiel est que ce travail identifie un système de freinage cellulaire naturel — l’axe miR-362-3p/DEP-1/ERK — qui peut restreindre les cellules du cancer gastrique en culture. Bien que l’étude se soit limitée à des cultures cellulaires et n’ait pas encore testé l’approche chez l’animal ou le patient, elle suggère deux stratégies complémentaires : restaurer les niveaux de miR-362-3p ou bloquer l’activité de DEP-1 pourrait aider à empêcher les tumeurs gastriques de croître et de se propager. Avec des recherches et validations supplémentaires, cet interrupteur microscopique d’ARN pourrait devenir l’un des outils ciblés d’une nouvelle génération pour détecter et traiter le cancer gastrique plus tôt et plus efficacement.
Citation: Tu, F., Li, Z., Yao, L. et al. MiR-362-3p inhibits the proliferation, migration and EMT of gastric cancer cells by regulating the DEP-1/ERK signaling pathway. Sci Rep 16, 10667 (2026). https://doi.org/10.1038/s41598-026-46696-3
Mots-clés: cancer gastrique, microARN, signalisation cellulaire, migration tumorale, voie ERK