Clear Sky Science · fr
Cibler l’EGFR exprimé par les cancers avec un anticorps monoclonal humanisé
Détecter les drapeaux cachés du cancer
Les traitements du cancer peinent souvent à trouver l’équilibre entre attaquer les cellules tumorales et épargner les tissus sains. Cet article décrit un nouvel anticorps conçu en laboratoire, appelé A10, capable de distinguer les cellules cancéreuses portant une forme particulière d’un récepteur de signal de croissance des cellules normales. En ciblant une conformation qui apparaît surtout lorsque ce récepteur est modifié ou sursaturé à la surface des tumeurs, A10 ouvre la voie à des thérapies à la fois puissantes et plus sélectives que nombre d’options actuelles.
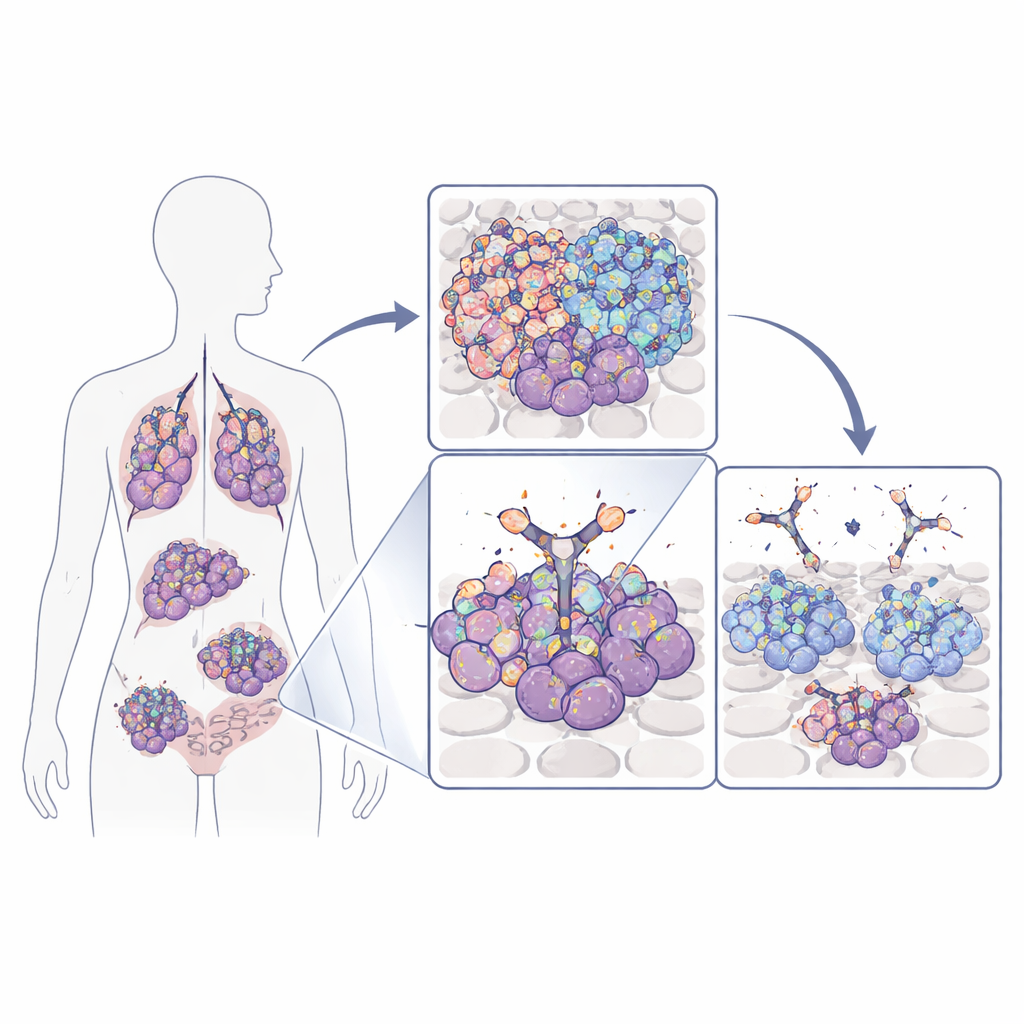
Pourquoi cet interrupteur de croissance est important
De nombreuses tumeurs, y compris les cancers agressifs du cerveau, du poumon, du sein et du côlon, dépendent d’une protéine de surface appelée récepteur du facteur de croissance épidermique (EGFR) pour croître et survivre. Les cellules tumorales peuvent augmenter l’activité de ce récepteur en amplifiant son gène, en le mutant, ou en produisant une version tronquée constamment activée connue sous le nom d’EGFRvIII. Les médicaments classiques qui bloquent l’EGFR touchent souvent à la fois les cellules cancéreuses et les tissus normaux, car ils reconnaissent des régions du récepteur présentes partout. L’équipe de cette étude s’est plutôt concentrée sur une petite boucle de l’EGFR qui devient clairement exposée principalement sur les cellules cancéreuses—soit parce que l’EGFR est présent en nombre anormalement élevé, soit parce que le récepteur est tronqué dans EGFRvIII. Cette boucle agit comme un « drapeau » spécifique au cancer qui peut, en principe, être ciblé de manière beaucoup plus sûre.
Transformer un anticorps de souris en médicament humain
Les chercheurs avaient précédemment découvert un anticorps de souris, 40H3, qui reconnaissait cette boucle exposée sur l’EGFR exprimé par les cancers. Les anticorps de souris peuvent toutefois provoquer des réactions immunitaires s’ils sont administrés de façon répétée aux patients. Pour surmonter ce problème, l’équipe a utilisé des méthodes de génie protéique pour greffer les segments de liaison clés de 40H3 sur des cadres d’anticorps humains, générant quatorze candidats « humanisés » ainsi qu’une molécule de référence chimérique. Lorsqu’ils ont testé ces variantes sur des cellules tumorales surexprimant l’EGFR, trois versions se sont révélées particulièrement attachantes, et une—A10—s’est distinguée comme la meilleure liaison tout en ignorant les cellules normales aux niveaux modestes d’EGFR. Sur un large panel de lignées tumorales présentant différentes mutations et nombres de copies d’EGFR, A10 a systématiquement montré une liaison supérieure à celle de l’anticorps de souris original et a conservé une forte préférence pour les cellules malignes.
Voir comment l’anticorps saisit sa cible
Pour comprendre pourquoi A10 est si sélectif, l’équipe a résolu la structure 3D haute résolution de la partie active de l’anticorps liée à la boucle de l’EGFR. La boucle se replie en une épingle compacte stabilisée par une liaison disulfure, et A10 berce cette conformation dans une gouttière formée entre ses deux bras, avec de nombreux contacts chargés la verrouillant en place. En comparant cette structure aux formes connues de la molécule complète de l’EGFR, les chercheurs ont obtenu un insight clé : tant dans la forme inactive « bridée » que dans la forme dimérique active de l’EGFR normal, la boucle est en grande partie enfouie ou partiellement masquée par des domaines voisins. Cela signifie qu’A10 ne peut pas atteindre facilement son site de liaison sur des récepteurs typiques exprimés à des niveaux modestes. En revanche, dans la variante spécifique au cancer EGFRvIII, la partie antérieure du récepteur est absente, laissant la boucle fortement exposée et accessible. Les données suggèrent qu’A10 reconnaît principalement l’EGFR lors de certaines conformations transitoires et dans des formes surpeuplées ou tronquées qui apparaissent préférentiellement sur les cellules tumorales.
Armer l’anticorps pour tuer les cellules tumorales
Reconnaître un drapeau spécifique au cancer est utile en soi, mais les chercheurs sont allés plus loin en transformant A10 en un conjugué anticorps‑médicament (ADC). Ils ont attaché chimiquement un composé cytotoxique puissant, le monométhyl auristatine E (MMAE), à A10 en utilisant un linker clivable à l’intérieur des cellules. Cet ADC A10‑MMAE se liait aux cellules cancéreuses aussi bien que l’anticorps non conjugué. Dans des essais en laboratoire sur de nombreuses lignées cellulaires, l’ADC était le plus efficace contre les tumeurs présentant des niveaux très élevés d’EGFR ou EGFRvIII, là où A10 disposait de nombreux sites de liaison. Dans ces cellules, de très faibles quantités du conjugué suffisaient à déclencher la mort cellulaire. Les lignées tumorales avec moins de cibles A10 ou une résistance intrinsèque au MMAE étaient moins affectées, et les fibroblastes normaux portant un EGFR sauvage restaient indemnes malgré leur sensibilité au MMAE libre. Les résultats montrent que la combinaison d’une liaison sélective et d’une libération intracellulaire du médicament peut concentrer nettement la toxicité sur les cellules cancéreuses.
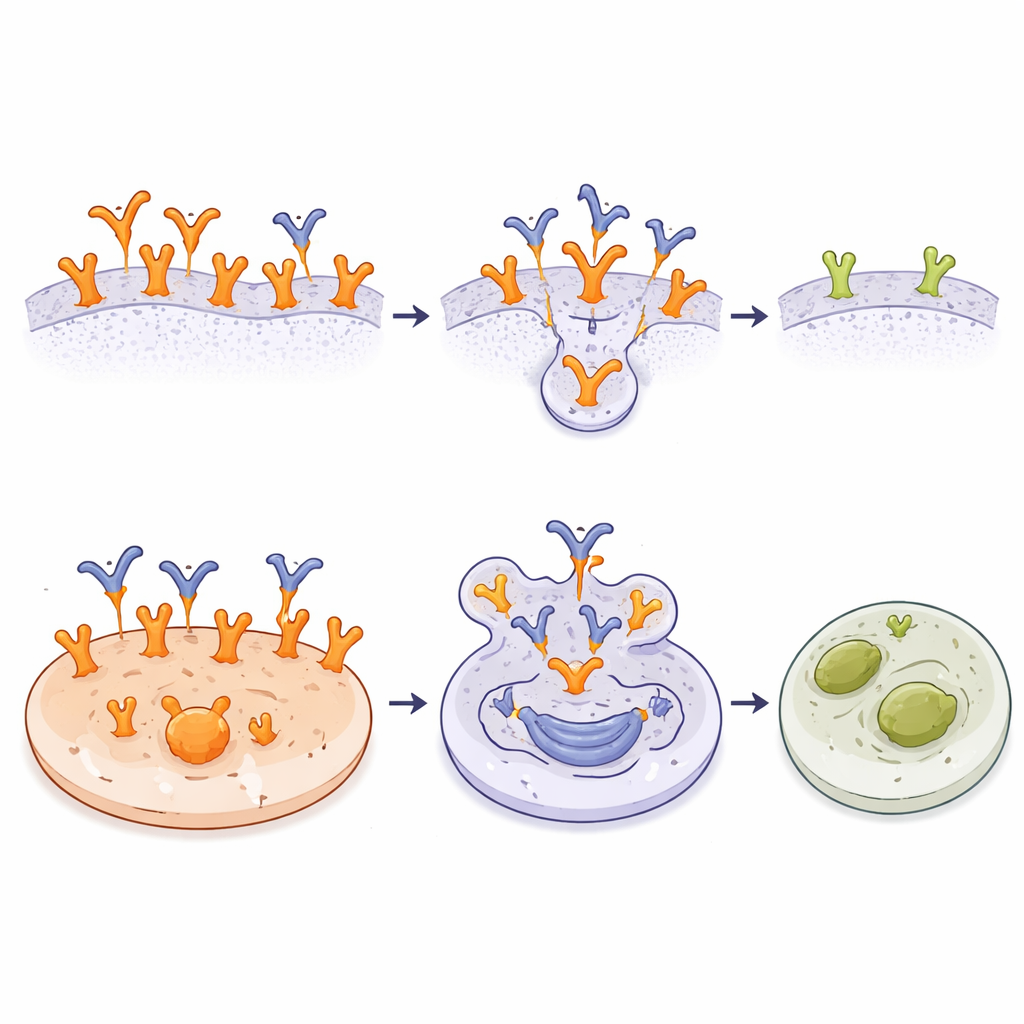
Ce que cela pourrait signifier pour les soins du cancer à venir
En termes simples, ce travail montre qu’il est possible de concevoir un anticorps qui « voit » l’EGFR uniquement lorsqu’il ressemble et se comporte comme un récepteur qui pilote le cancer, tout en ignorant pour l’essentiel sa forme courante dans les tissus sains. En cartographiant précisément la manière dont A10 saisit une boucle cachée de l’EGFR et en démontrant qu’un conjugué médicamenteux dérivé d’A10 peut tuer efficacement les cellules tumorales riches en récepteur tout en épargnant les cellules normales, l’étude fournit une base solide pour développer des thérapies très ciblées et plus sûres. Si ces résultats se traduisent chez les patients, les traitements futurs fondés sur A10 pourraient délivrer des médicaments puissants directement aux cancers dépendants de l’EGFR tout en laissant le reste de l’organisme largement indemne.
Citation: Costa, T.G.F., Sarnovsky, R., Zhan, J. et al. Targeting cancer expressed EGFR with a humanized monoclonal antibody. Sci Rep 16, 10814 (2026). https://doi.org/10.1038/s41598-026-46245-y
Mots-clés: EGFR, conjugué anticorps-médicament, thérapie ciblée contre le cancer, glioblastome, EGFRvIII