Clear Sky Science · fr
Aperçus structurels et mécanistiques du ciblage des intégrines α2β1 et α5β1 par des vésicules extracellulaires bioingénierées issues de cellules cancéreuses pulmonaires
Les messagers cachés du cancer
Le cancer du poumon est souvent détecté tardivement, lorsque les options thérapeutiques sont limitées. Une approche prometteuse consiste à n’administrer les médicaments qu’aux cellules tumorales, en épargnant les tissus sains. Cette étude explore un minuscule système naturel de livraison — les vésicules extracellulaires, ou VE — que les cellules cancéreuses utilisent déjà pour envoyer des messages. En réingénierant ces vésicules avec un court motif de ciblage, les chercheurs montrent comment elles peuvent se fixer à des points d’ancrage spécifiques des cellules tumorales, posant les bases de thérapies anticancéreuses plus précises et moins toxiques.
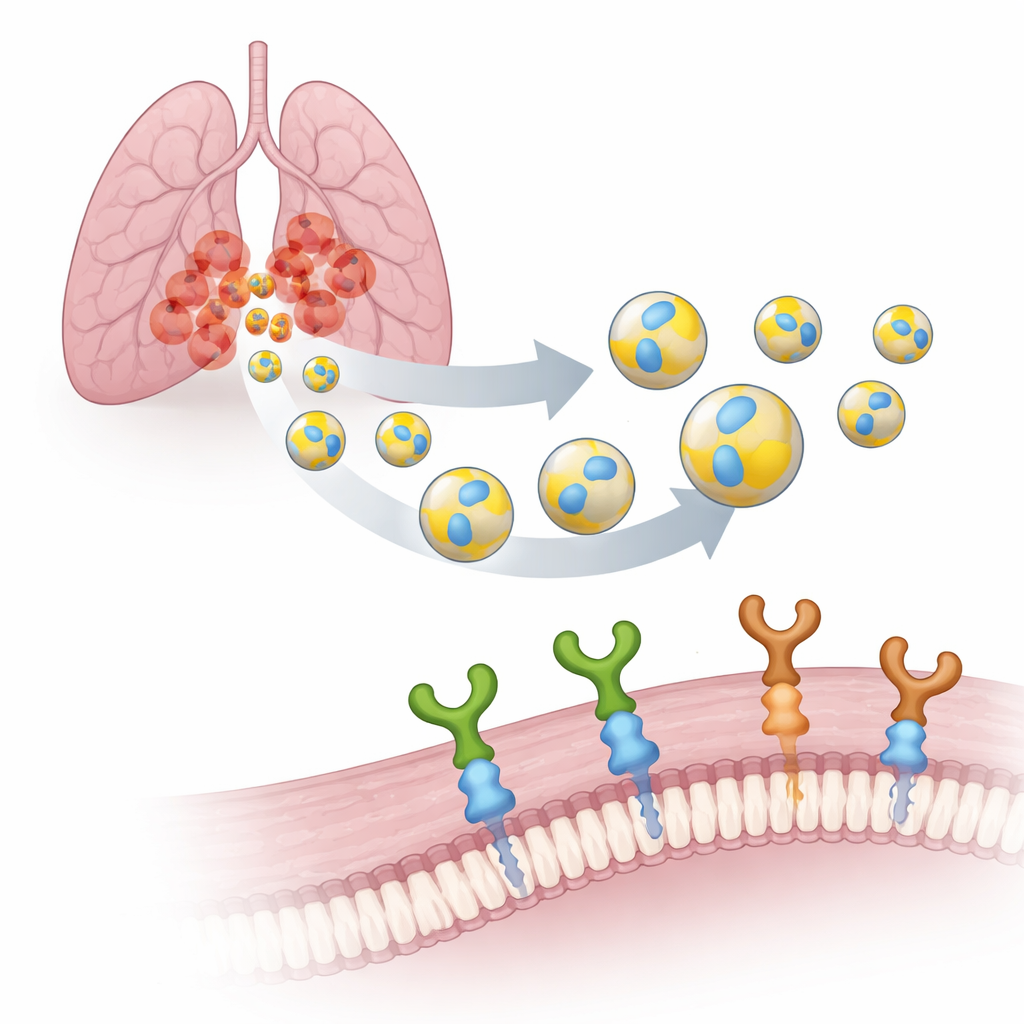
Transformer des paquets naturels en coursiers intelligents
Chaque cellule de notre organisme libère des VE : des bulles à l’échelle nanométrique entourées d’une membrane, un peu comme des bulles de savon microscopiques. Parce qu’elles sont produites par nos propres cellules, les VE sont biodégradables, traversent plus facilement les barrières biologiques et sont moins susceptibles de provoquer des effets indésirables que les vecteurs synthétiques. L’équipe s’est concentrée sur les VE produites par des cellules humaines de cancer du poumon (A549) et a décoré leur surface d’un petit motif de sept unités appelé PTHTRWA. Des expériences antérieures avaient montré que ce motif oriente les VE vers les cellules de cancer du poumon chez la souris, se liant bien plus fortement aux cellules tumorales qu’aux cellules pulmonaires normales tout en restant faiblement toxique.
Identifier les bons ports d’amarrage sur les cellules tumorales
Pour transformer ces vésicules marquées en outils véritablement ciblés, les chercheurs ont dû identifier quels « ports » sur les cellules cancéreuses elles reconnaissent. Ils ont examiné deux récepteurs de surface apparentés, les intégrines α2β1 et α5β1. Ce sont des grappins moléculaires qui aident les cellules à s’ancrer à leur environnement et à transmettre des signaux en leur sein. Dans les tumeurs pulmonaires, α5β1 est fortement associée à un comportement agressif, à la dissémination et à une survie réduite, tandis qu’α2β1 a été liée à la résistance à la chimiothérapie. À l’aide d’une technique sensible appelée résonance plasmonique de surface, l’équipe a comparé l’affinité des VE décorées de PTHTRWA pour ces deux intégrines. Ils ont observé que les vésicules sans le motif interagissaient à peine, alors que les VE marquées formaient des complexes serrés et stables avec les deux récepteurs dans des conditions proches de la physiologie.
Approche moléculaire de l’embrassade
Pour comprendre ce qui se passe atome par atome lorsque le motif rencontre les intégrines, les chercheurs ont eu recours à des simulations informatiques. Ils ont construit des modèles tridimensionnels du motif lié aux régions clés des intégrines et ont laissé ces systèmes évoluer en eau virtuelle pendant des centaines de nanosecondes. Les calculs ont montré que PTHTRWA s’insère confortablement dans une gouttière peu profonde du récepteur α2β1, formant un réseau de liaisons hydrogène et de contacts hydrophobes qui stabilisent le complexe. De manière cruciale, la liaison favorisait une conformation plus « ouverte » du récepteur — sa forme à haute affinité prête à signaler — plutôt que l’état « fermé » de repos. Lorsqu’ils ont testé des versions légèrement modifiées du motif, ils ont constaté que de petites retouches chimiques à une extrémité peuvent remodeler subtilement la façon dont le peptide se positionne dans la gouttière et son degré de préférence pour l’une ou l’autre intégrine.
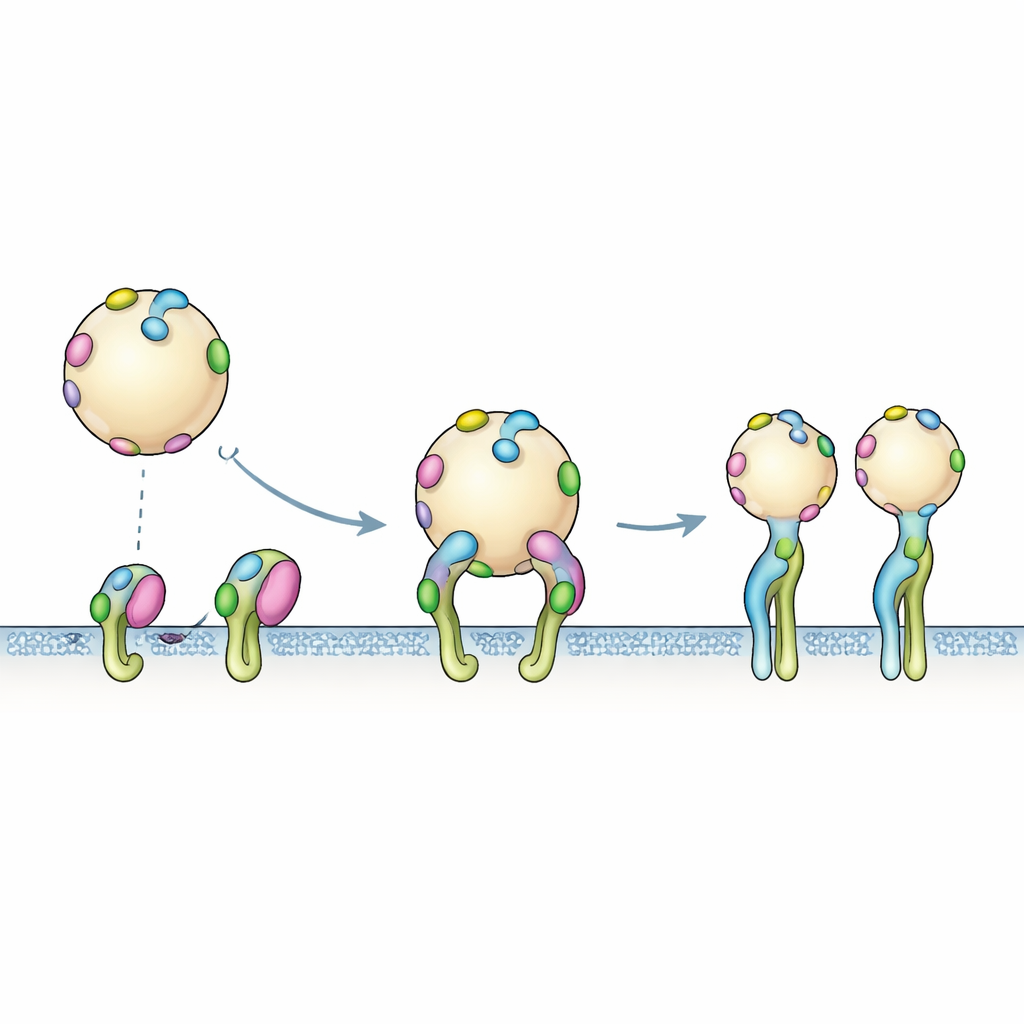
Du motif unique aux prises multivalentes
Les modèles informatiques décrivent un seul motif touchant un récepteur à la fois, mais la surface réelle d’une VE est couverte de nombreuses copies de PTHTRWA. Les expériences de liaison reflètent cette réalité multivalente : lorsqu’une vésicule marquée s’approche d’un patch d’intégrines, plusieurs motifs peuvent s’engager simultanément. Les données du capteur s’ajustent au mieux à un processus en deux étapes. D’abord, la vésicule s’amarre brièvement par des rencontres rapides et réversibles. Puis survient une réorganisation plus lente au cours de laquelle les intégrines basculent en conformation ouverte et l’accroche globale se renforce. Cette prise coopérative et à plusieurs mains explique pourquoi la force d’interaction apparente des vésicules entières est supérieure à celle prédite à partir d’un seul motif isolé.
Ce que cela pourrait signifier pour les traitements futurs
En termes simples, l’étude montre que des VE armées du motif PTHTRWA peuvent reconnaître sélectivement des intégrines hyperactives dans le cancer du poumon, et ce en poussant ces récepteurs vers une forme ouverte et fortement liée. En cartographiant ces interactions en détail, les chercheurs fournissent des règles de conception pour des transporteurs de nouvelle génération basés sur des vésicules, capables de délivrer des médicaments, des agents d’imagerie ou d’autres charges directement aux cellules malignes tout en épargnant en grande partie les tissus sains. Bien que des études complémentaires chez l’animal et chez l’humain restent nécessaires, cette stratégie de ciblage des intégrines rapproche d’un pas la vision d’une médecine oncologique personnalisée basée sur les VE.
Citation: Nowicka, A.M., Żołek, T., Kowalczyk, A. et al. Structural and mechanistic insights into α2β1 and α5β1 integrin targeting by bioengineered extracellular vesicles originating from lung cancer cells. Sci Rep 16, 10833 (2026). https://doi.org/10.1038/s41598-026-46071-2
Mots-clés: cancer du poumon, vésicules extracellulaires, intégrines, administration ciblée de médicaments, simulations moléculaires