Clear Sky Science · fr
Le composé fluoroquinolinique exerce des effets anti-érythroleucémiques en ciblant doublement GLUT1 et la voie de signalisation PI3K/AKT
Un nouvel angle sur un cancer du sang dangereux
Lérythroleucémie est une forme rare mais très agressive de cancer du sang, avec peu d’options thérapeutiques en dehors de la transplantation de cellules souches. Pour de nombreux patients, souvent âgés, cela signifie des traitements lourds, des coûts élevés et des perspectives peu encourageantes. Cette étude explore un composé conçu en laboratoire, nommé FKL-137, qui attaque les cellules d’érythroleucémie d’une manière inattendue : en coupant leur carburant préféré, le sucre, et en déclenchant leur autodestruction. Les travaux suggèrent une classe possible de médicaments ciblés exploitant la dépendance des cellules cancéreuses à un métabolisme de l’énergie altéré, tout en épargnant davantage les tissus sains.
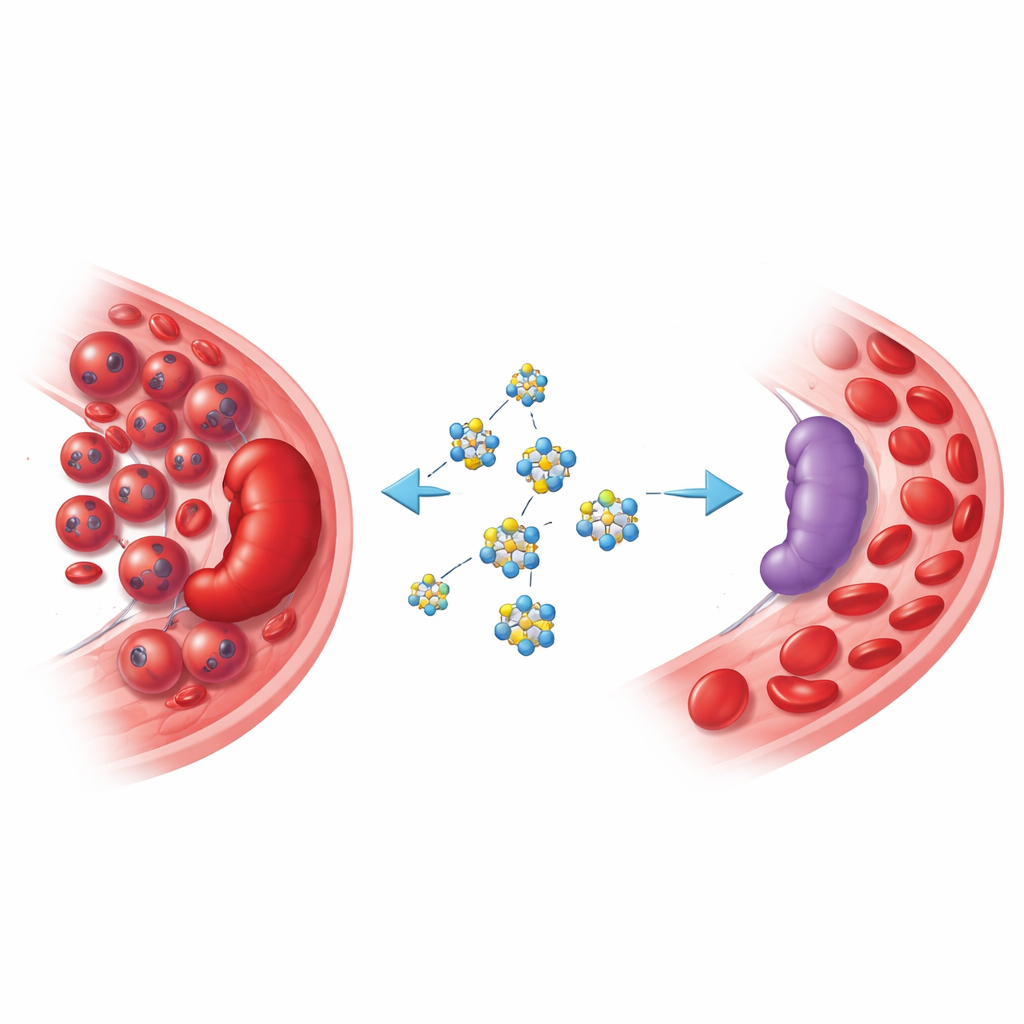
Quand les cellules sanguines déraillent
Dans l’érythroleucémie, des précurseurs immatures des globules rouges prolifèrent de façon incontrôlée dans la moelle osseuse et la rate. Les patients peuvent développer une anémie sévère, des splénomégalies menaçant de se rompre, et une dégradation rapide de l’état de santé. Les thérapies actuelles sont limitées et beaucoup de personnes sont trop fragiles pour des traitements agressifs. Parallèlement, les chercheurs ont montré que de nombreux cancers hématologiques reposent sur une utilisation réprogrammée du glucose : ils captent le glucose à des taux élevés et le convertissent rapidement en énergie et en éléments de construction, ce qui favorise leur multiplication et leur échappement au système immunitaire. Cibler cette « addiction » métabolique est devenu une stratégie attrayante pour de nouveaux médicaments.
Affamer les cellules cancéreuses en sucre
Les chercheurs se sont concentrés sur une petite molécule synthétique, FKL-137, dérivée d’une famille chimique déjà connue pour son activité anticancéreuse. En expérimentations in vitro, ils ont exposé deux lignées cellulaires humaines d’érythroleucémie à des doses croissantes de FKL-137. Le composé a considérablement ralenti la croissance cellulaire au fil du temps et a poussé les cellules vers la mort programmée, observée par des changements morphologiques classiques et l’activation des mécanismes internes d’apoptose. Fait important, FKL-137 s’est montré bien plus puissant contre les cellules leucémiques que contre des cellules hépatiques normales, et les évaluations de sécurité du médicament ont suggéré une toxicité relativement faible aux doses efficaces.
Frapper les portes du sucre du cancer
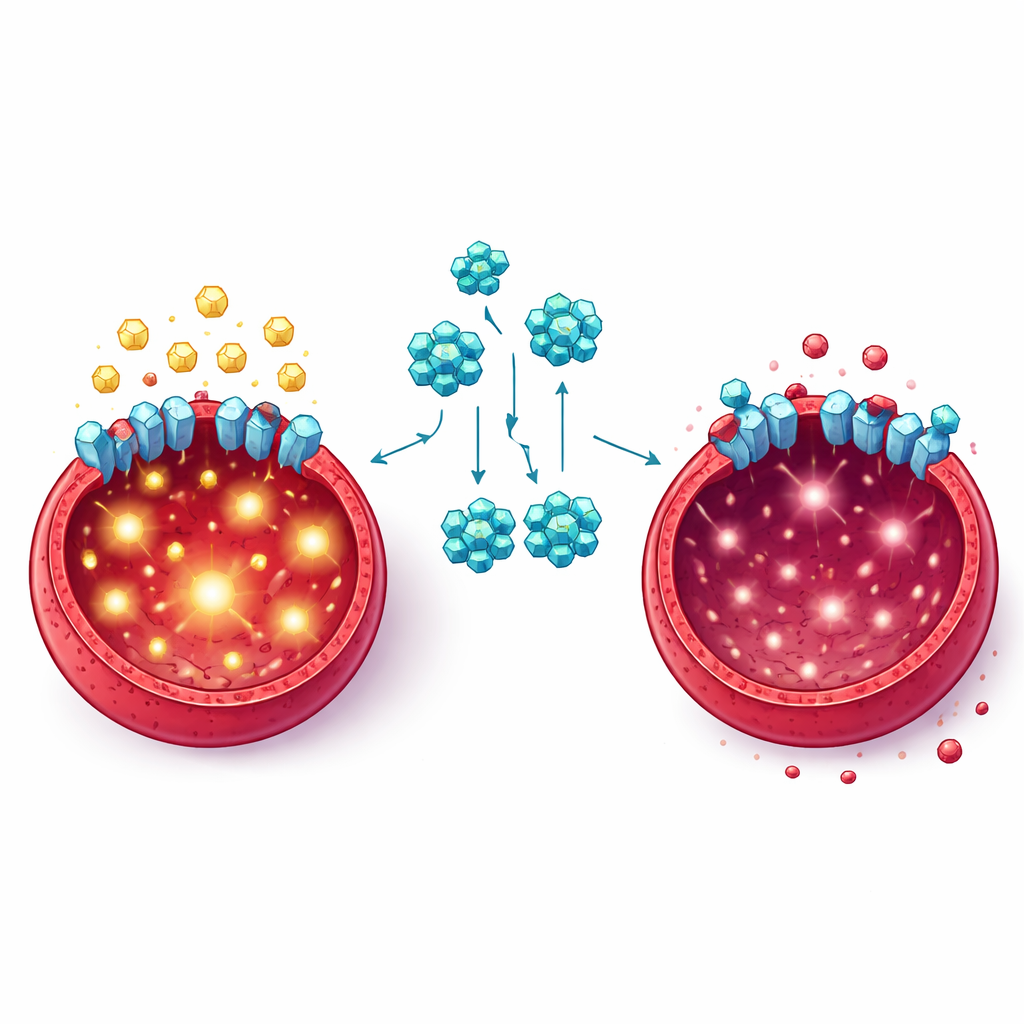
En approfondissant, l’équipe a cherché comment FKL-137 interfère avec le métabolisme tumorale. Ils ont constaté que les cellules leucémiques traitées absorbent moins de glucose et libèrent moins de lactate, sous-produit d’une intense combustion du sucre. Des protéines clés qui aident normalement à convertir le glucose en énergie et en précurseurs biosynthétiques étaient diminuées. À l’aide de modélisation informatique, de tests de stabilité thermique et d’imagerie, les chercheurs ont montré que FKL-137 se lie à GLUT1, une « porte » majeure à la surface cellulaire qui fait entrer le glucose. Lorsque les niveaux de GLUT1 ont été réduits par des méthodes génétiques, les cellules leucémiques ont poussé plus lentement et utilisé moins de sucre, et elles sont devenues encore plus sensibles à FKL-137. Cela a confirmé que GLUT1 est à la fois un moteur de la croissance des cellules d’érythroleucémie et une cible importante du médicament.
Déstabiliser une boucle de signalisation de croissance
L’étude a également mis au jour des effets au-delà de la porte du glucose elle-même. Les cellules d’érythroleucémie utilisent normalement une voie de signalisation connue sous le nom de PI3K/AKT pour favoriser la survie, la croissance et une forte consommation de glucose, en soutenant notamment GLUT1. Le traitement par FKL-137 a réduit les formes actives de protéines clé de cette voie, rompant une boucle d’amplification entre le transport du sucre et les signaux de croissance. Chez des souris infectées par un virus qui provoque de façon fiable l’érythroleucémie, le traitement par FKL-137 a amélioré les taux de globules rouges, réduit la taille des rates hypertrophiées, limité l’invasion des cellules cancéreuses dans les organes et corrigé le métabolisme du glucose anormal dans le tissu splénique — le tout sans dommages évidents au cœur, au foie, aux poumons ou aux reins.
Promesses, limites et étapes suivantes
Dans l’ensemble, les travaux présentent FKL-137 comme un candidat médicament à double action qui bloque à la fois la principale porte d’entrée du glucose des cellules d’érythroleucémie et atténue une voie de croissance puissante dépendante de ce carburant. En affamant d’abord les cellules tumorales, puis en les poussant vers la mort, le composé offre une approche conceptuellement élégante pour exploiter une faiblesse que les cellules normales ne partagent pas à la même intensité. Les auteurs soulignent toutefois que FKL-137 reste à optimiser : il présente une fenêtre thérapeutique relativement étroite, les cellules cancéreuses pourraient compenser en réorientant leur métabolisme, et les résultats obtenus sur lignées cellulaires et modèles murins doivent être confirmés sur des tissus humains. Néanmoins, l’étude renforce l’idée que cibler précisément la façon dont les cellules cancéreuses se nourrissent et croissent pourrait ouvrir un nouveau front dans le traitement de ce cancer du sang par ailleurs difficile à gérer.
Citation: Cheng, S., Zhao, W., Yu, J. et al. The fluoroquinoline compound exerts anti-erythroleukemic effects by dual-targeting GLUT1 and the PI3K/AKT signaling pathway. Sci Rep 16, 10916 (2026). https://doi.org/10.1038/s41598-026-45597-9
Mots-clés: érythroleucémie, métabolisme du cancer, inhibiteur de GLUT1, voie PI3K AKT, thérapie ciblée