Clear Sky Science · fr
Preuve de concept d'une extraction d'ADN circulant à partir du plasma basée sur un système aqueux à deux phases pour des applications de biopsie liquide
Pourquoi un test sanguin est important pour le cancer et d'autres maladies
De nombreux tests médicaux modernes recherchent de petits fragments d'ADN qui flottent librement dans notre sang. Ces fragments, appelés ADN circulant, peuvent indiquer si une tumeur libère du matériel génétique, si un organe greffé est en cours de rejet ou comment progresse une grossesse. Mais comme ces fragments sont rares, courts et mélangés à une soupe de protéines et d'autres molécules, les isoler proprement et rapidement est étonnamment difficile. Cette étude présente une nouvelle méthode plus simple pour extraire ces fragments du plasma sanguin en utilisant une séparation douce à base d'eau, ce qui pourrait rendre les tests avancés de « biopsie liquide » plus accessibles et abordables.
Le défi de pêcher de minuscules morceaux d'ADN
Les médecins et les chercheurs utilisent les biopsies liquides pour lire des indices génétiques à partir d'une simple prise de sang au lieu de pratiquer une biopsie tissulaire. Le problème est que l'ADN circulant dans le plasma existe généralement à seulement quelques dizaines de nanogrammes par millilitre et est fragmenté en courtes séquences. Une petite fraction de ce matériel peut provenir d'une tumeur ou d'un organe greffé, de sorte que chaque fragment compte. Les kits d'extraction standard capturent l'ADN en le faisant adhérer à des surfaces de silice en présence de sels forts, suivis de plusieurs étapes de lavage et de centrifugation. Ces kits fonctionnent bien mais prennent du temps, nécessitent un équipement spécialisé et peuvent être coûteux. Ils peuvent aussi éprouver des difficultés à récupérer les plus courts fragments et entraîner la co-purification de longs segments d'ADN génomique normal qui peuvent masquer des signaux rares liés à la maladie.
Une astuce à deux couches à base d'eau pour capturer l'ADN
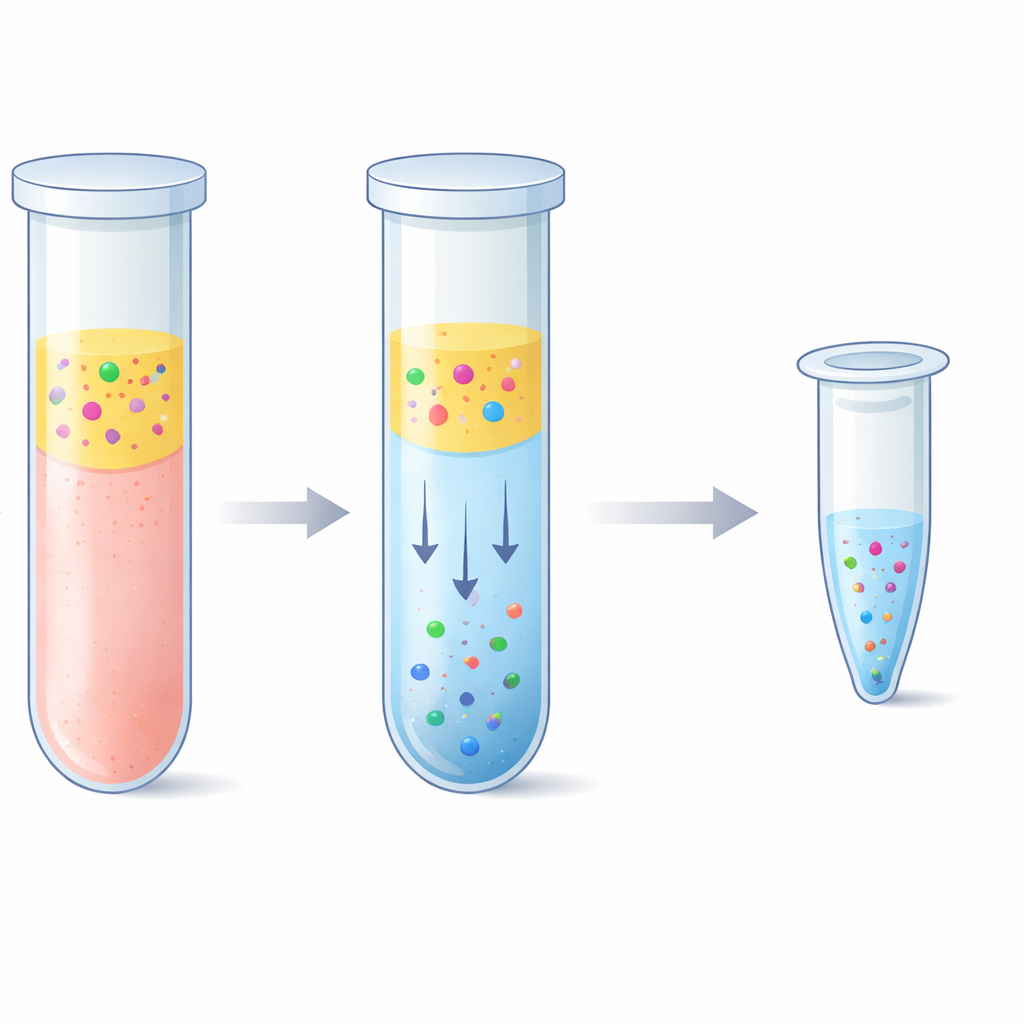
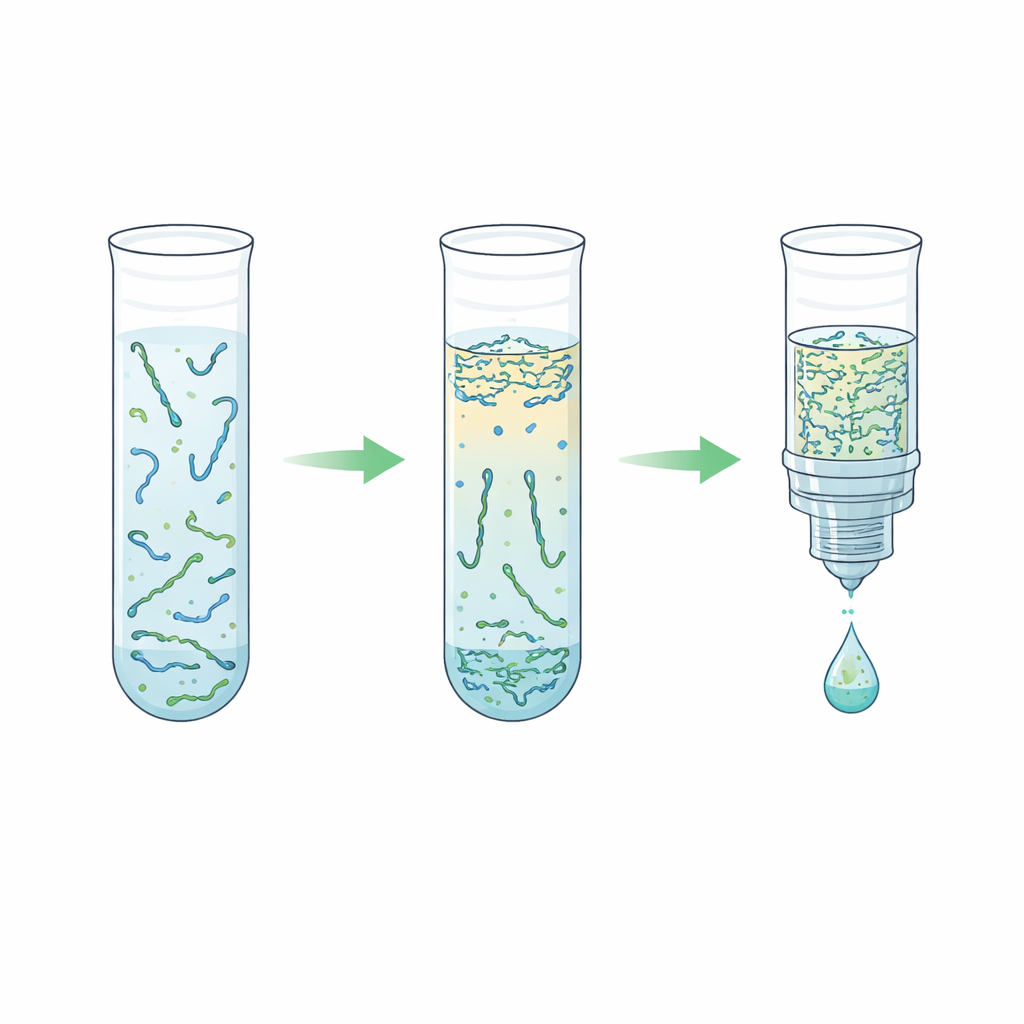
L'équipe a exploré une alternative basée sur un « système aqueux à deux phases » — en termes simples, deux liquides riches en eau qui ne se mélangent pas complètement, comme de l'huile et du vinaigre mais tous deux majoritairement constitués d'eau. En combinant le plasma à un polymère appelé polyéthylène glycol et à des sels phosphates simples, le mélange s'est naturellement séparé en une couche supérieure et une couche inférieure. Fait remarquable, les courts fragments d'ADN préféraient fortement la couche inférieure riche en sel, tandis que la plupart des protéines sanguines et les longues molécules d'ADN restaient dans la couche supérieure ou à l'interface. Les chercheurs ont ajusté précisément la recette pour que cette couche inférieure reste assez petite pour concentrer l'ADN mais suffisamment douce pour ne pas l'endommager. Ils ont ensuite associé cette étape à une purification par « élution inversée », qui pousse la couche salée inférieure à travers une matrice poreuse pour éliminer le sel et réduire le volume final, aboutissant à une solution d'ADN plus propre et plus concentrée.
Affiner le procédé pour une utilisation réelle
Après de nombreux essais, les auteurs ont ajusté l'équilibre du polymère et du sel, les vitesses de centrifugation, les volumes et des étapes de lyse optionnelles qui dissocient les complexes protéine–ADN. Ils ont constaté qu'augmenter la teneur en polymère selon certaines lignes de composition doublait la concentration d'ADN sans nuire au rendement, et qu'un conditionnement plus poussé lors de l'élution inversée multipliait approximativement par quatre la concentration par rapport à leur travail antérieur. Fait surprenant, ils ont découvert que sauter la lyse agressive avant la séparation en deux phases fonctionnait souvent mieux ; la lyse avait tendance à perturber les phases et à réduire le rendement. Un flux de travail rationalisé, largement sans lyse, a éliminé environ 99,7 % des protéines du plasma tout en récupérant jusqu'à environ les deux tiers de l'ADN court initial dans un volume réduit d'un facteur quatre, le tout en environ dix minutes de traitement total et seulement quelques minutes d'intervention manuelle.
Comment la nouvelle méthode se compare
Les chercheurs ont comparé leur approche à un kit de silice commercial largement utilisé. Le kit standard produisait des rendements d'ADN totaux légèrement supérieurs et une concentration plus forte car il élue dans des volumes très réduits. Cependant, la méthode à deux phases a montré des récupérations constantes supérieures à 60 % sur une gamme d'apports d'ADN, même avec des quantités initiales très faibles, et nécessitait beaucoup moins d'étapes manuelles et d'équipement. Surtout, le nouveau procédé agissait comme un filtre intégré pour la longueur des fragments : il enrichissait les courts ADN de type circulant tout en excluant en grande partie les longues chaînes provenant de cellules sanguines rompues. Des tests par PCR quantitative ont montré que les extraits purifiés n'inhibaient pas l'amplification en aval. Lorsque l'équipe a utilisé un échantillon de référence commercial contenant des mutations connues liées au cancer, l'ADN récupéré par leur méthode a pu être transformé en bibliothèques de séquençage, séquencé sur une plateforme à haut débit et utilisé pour détecter toutes les variantes attendues aux fréquences correctes.
Ce que cela pourrait signifier pour les futurs tests sanguins
En termes simples, ce travail montre qu'une séparation relativement simple à base d'eau peut remplacer une chimie de surface solide plus complexe pour préparer l'ADN circulant à partir du plasma. Bien que la nouvelle méthode fournisse actuellement un peu moins d'ADN que les meilleurs kits commerciaux, elle offre un traitement rapide, une forte élimination des protéines et des longs brins d'ADN indésirables, et une compatibilité directe avec la PCR et le séquençage de nouvelle génération. Si elle est validée davantage sur des échantillons de patients réels et adaptée à l'automatisation, cette approche pourrait réduire les coûts et simplifier les flux de travail en laboratoire, contribuant à rendre les tests sanguins précis, basés sur la génétique, pour le cancer, la transplantation et d'autres affections, plus largement accessibles au quotidien.
Citation: Meutelet, R., Buerfent, B.C., Hess, T. et al. Proof of concept for aqueous two-phase system-based extraction of cell-free DNA from plasma for liquid biopsy applications. Sci Rep 16, 11232 (2026). https://doi.org/10.1038/s41598-026-45585-z
Mots-clés: biopsie liquide, ADN circulant, test sanguin du cancer, extraction d'ADN, séquençage nouvelle génération