Clear Sky Science · fr
L’interféron-β et le FTY720 atténuent l’inflammation progressive du SNC via une signalisation astrocytaire associée à SOCS1
Pourquoi cette recherche compte pour les personnes atteintes de sclérose en plaques
Pour de nombreuses personnes atteintes de sclérose en plaques (SEP), la plus grande crainte n’est pas liée aux poussées initiales mais à la perte lente et continue de fonctions qui peut suivre. Dans cette phase progressive tardive, les lésions dans le cerveau et la moelle épinière se poursuivent même lorsque les traitements standards visant le système immunitaire sanguin font leur effet. Cette étude explore une façon d’atteindre cette inflammation « cachée » en combinant un comprimé existant pour la SEP avec une forme d’un médicament ancien administrée directement vers le cerveau.
Une maladie cérébrale de longue durée avec peu d’options
La SEP est une maladie auto-immune dans laquelle les propres cellules immunitaires de l’organisme attaquent l’isolation des fibres nerveuses, entraînant des troubles visuels, une faiblesse et d’autres symptômes neurologiques. Au début, les symptômes ont tendance à apparaître et à disparaître. Avec le temps, de nombreux patients entrent dans une phase progressive marquée par un handicap progressif, souvent irréversible. À ce stade, la barrière hémato-encéphalique devient plus difficile à franchir pour les médicaments, et l’activité nocive des cellules résidentes du cerveau appelées glies — en particulier les astrocytes et les microglies — prend un rôle croissant. Les traitements actuels, qui agissent principalement en bloquant les cellules immunitaires dans le sang, apportent une aide limitée une fois que ce stade est établi.
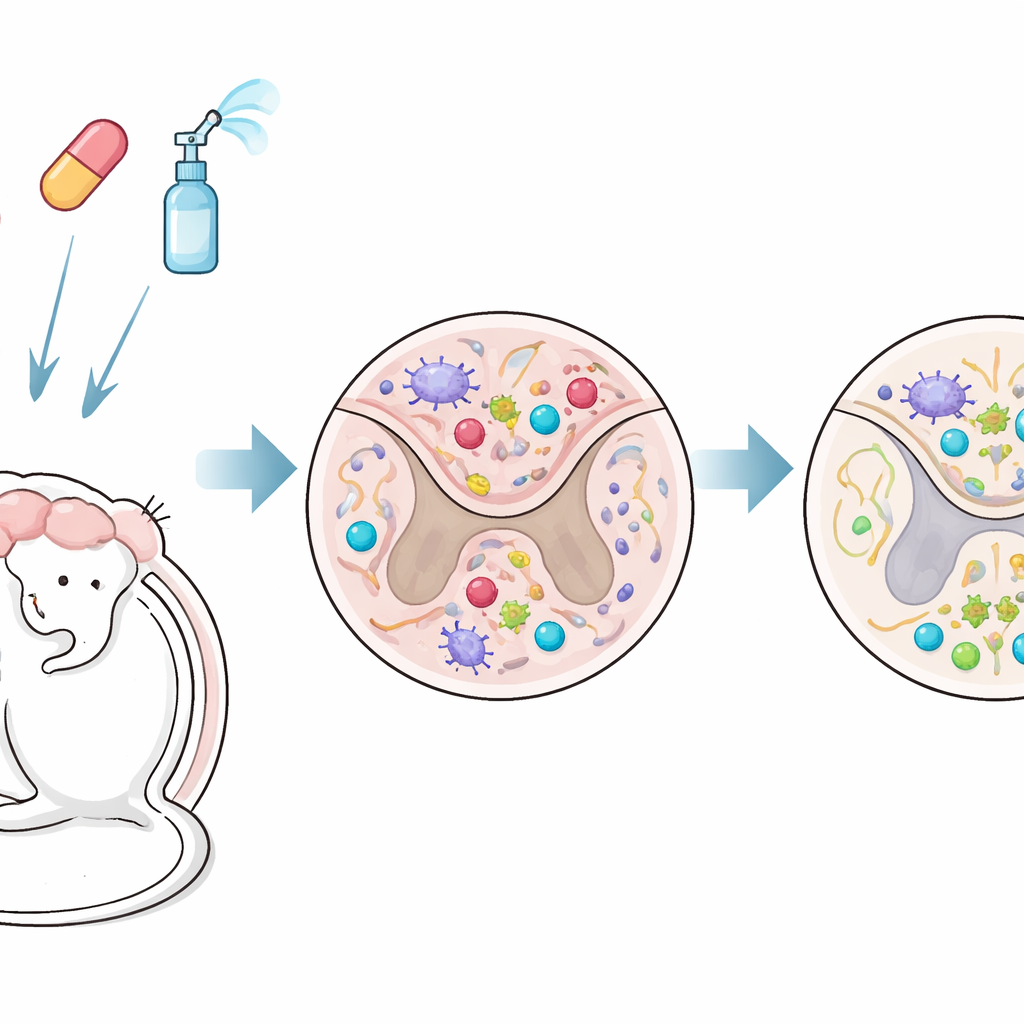
Associer deux médicaments pour atteindre à la fois le sang et le cerveau
Les chercheurs ont testé un traitement combiné dans un modèle murin qui reproduit fidèlement la SEP progressive. Un médicament, le fingolimod (FTY720), est un comprimé qui piège les cellules immunitaires dans les ganglions lymphatiques et peut aussi pénétrer dans le cerveau. L’autre, l’interféron‑β, est une thérapie de longue date pour la SEP qui agit normalement en dehors du cerveau car elle ne traverse pas facilement la barrière hémato-encéphalique. Dans cette étude, l’interféron‑β a été administré par voie intranasale — par le nez — pour contourner cette barrière et atteindre plus directement le système nerveux central. Le traitement a commencé après que les souris eurent déjà développé des troubles neurologiques chroniques, reflétant une phase où les lésions sont typiquement plus difficiles à inverser.
Moins de dégâts et une activité immunitaire plus calme
Les souris ayant reçu la combinaison fingolimod plus interféron‑β intranasal ont présenté de meilleurs résultats que celles traitées par fingolimod seul. Leurs scores de maladie se sont davantage améliorés et certains déficits neurologiques existants ont diminué. Lors de l’examen des moelles épinières, les chercheurs ont observé une myéline mieux préservée, moins de signes de lésions axonales et moins de cellules immunitaires infiltrantes. Les lymphocytes T et les monocytes pro-inflammatoires ont été réduits, et les lymphocytes T restants ont produit moins de molécules messagères délétères comme l’interféron‑gamma et l’IL‑17. Fait important, la thérapie combinée a également atténué les signaux nocifs émanant des astrocytes et des microglies, ces cellules gliales qui contribuent à façonner l’environnement local du cerveau et de la moelle épinière.
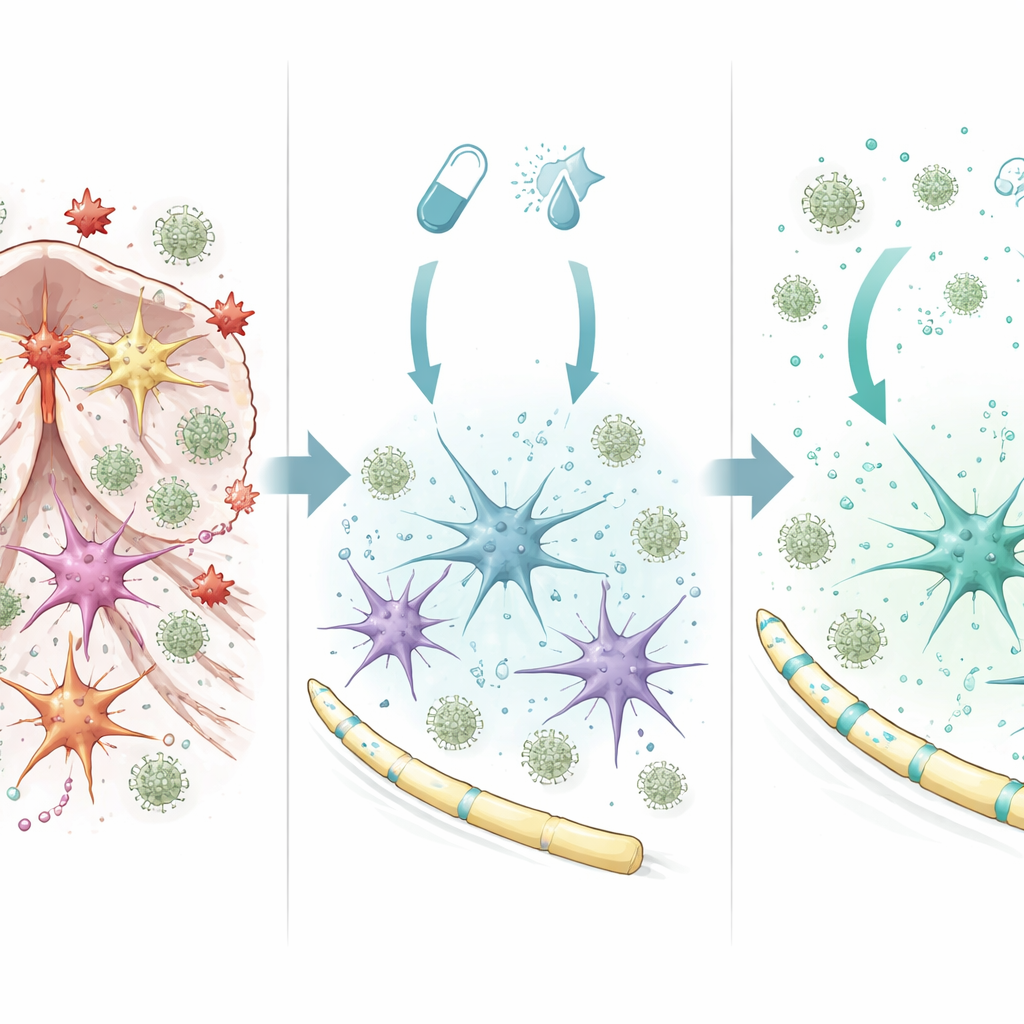
Les astrocytes passent d’un comportement nuisible à protecteur
Pour comprendre comment la combinaison agit dans le cerveau, l’équipe a étudié des astrocytes purifiés en culture. Lorsqu’ils ont été exposés au fingolimod et à l’interféron‑β, les astrocytes ont activé un large ensemble de gènes liés à la survie cellulaire, à la réduction de l’inflammation et à une myélinisation plus saine. Un acteur clé était un régulateur appelé SOCS1, qui agit comme un frein sur la signalisation inflammatoire. Bloquer SOCS1 dans les astrocytes effaçait une grande partie du profil génique protecteur et amenait ces cellules à libérer davantage de facteurs inflammatoires attirant les cellules immunitaires. À l’inverse, lorsque SOCS1 était actif, les astrocytes produisaient davantage de signaux de croissance et de réparation et libéraient un mélange de molécules réduisant la migration des monocytes inflammatoires. Des changements protecteurs similaires ont été observés dans des lignées cellulaires humaines d’astrocytes et de microglies traitées par la combinaison médicamenteuse, suggérant que le mécanisme est pertinent au-delà de la souris.
Ce que cela pourrait signifier pour les thérapies futures de la SEP
Cette étude montre qu’associer le fingolimod à l’interféron‑β administré par voie nasale peut faire plus que simplement bloquer les cellules immunitaires dans le sang. Cela peut aussi reprogrammer les astrocytes à l’intérieur du système nerveux central vers un état plus calme et protecteur, SOCS1 jouant le rôle de nœud de contrôle central. Bien que le travail ait été réalisé chez la souris et en cultures cellulaires, et que l’interféron‑β seul n’ait pas été testé de manière parallèle dans toutes les expériences, les résultats pointent vers une stratégie prometteuse : cibler à la fois le système immunitaire périphérique et les cellules de soutien du cerveau en même temps. Si des effets similaires peuvent être obtenus et prouvés sûrs chez l’humain, de telles approches combinées et centrées sur le cerveau pourraient aider à ralentir ou partiellement inverser les dommages silencieux qui alimentent la SEP progressive.
Citation: Tsaktanis, T., Beyer, T., Nirschl, L. et al. Interferon-β and FTY720 ameliorate progressive CNS inflammation via SOCS1-associated astrocyte signaling. Sci Rep 16, 9851 (2026). https://doi.org/10.1038/s41598-026-45303-9
Mots-clés: sclérose en plaques progressive, fingolimod, interféron bêta, astrocytes, neuroinflammation