Clear Sky Science · fr
Données cristallographiques de la dolichylphosphate mannose synthase de Pyrococcus furiosus suggèrent que l’enzyme pourrait faire basculer son produit glycolipidique
Comment les microbes thermophiles entretiennent leur couche cellulaire
De nombreux microbes qui prospèrent dans des environnements bouillants survivent grâce à une couche protectrice de sucres à la surface cellulaire. La construction de cette couche nécessite des molécules graisse–sucre particulières qui doivent être synthétisées d’un côté de la membrane cellulaire puis déplacées de l’autre. Cette étude dissèque l’une de ces enzymes productrices de molécules et suggère que, de manière remarquable, la même protéine pourrait aussi aider à faire basculer son produit à travers la membrane — assurant ainsi deux fonctions à la fois.
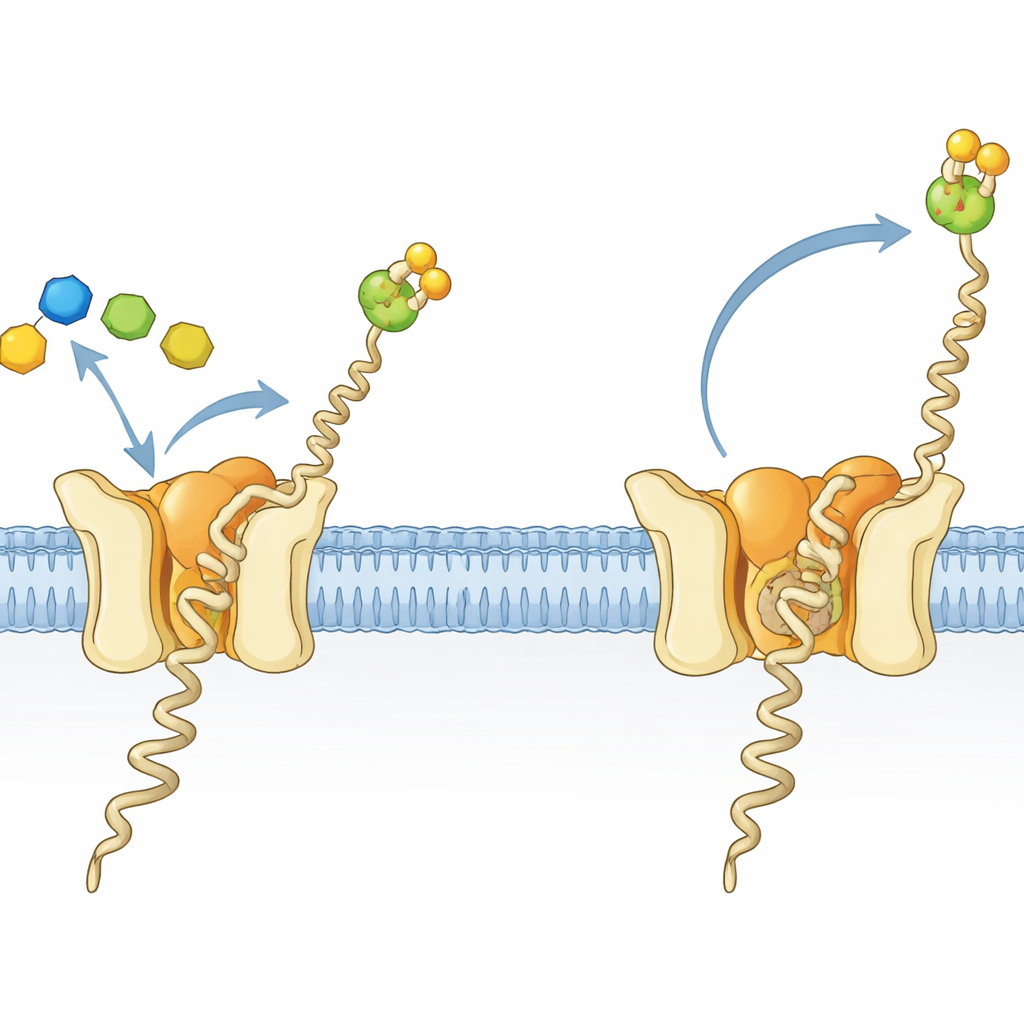
Une petite usine pour une molécule sucre–lipide essentielle
Les cellules de tous les domaines du vivant décorent de nombreuses protéines de chaînes de sucres, un processus essentiel pour le repliement correct, la stabilité et la communication intercellulaire. Chez les archées et les eucaryotes, un élément clé de ces décorations est une molécule sucre–lipide appelée dolichylphosphate mannose (Dol-P-Man). Elle comprend une longue queue hydrophobe ancrée dans la membrane et une tête sucre–phosphate qui émerge dans le milieu aqueux environnant. Le Dol-P-Man est synthétisé par l’enzyme dolichylphosphate mannose synthase (DPMS), qui transfère un sucre mannose depuis un donneur soluble sur un lipide lié à la membrane. Chez l’archée hyperthermophile Pyrococcus furiosus, la DPMS est une protéine monocaténaire, dite DPMS de type III, avec une région catalytique soluble attachée à une section transmembranaire en bundle de quatre hélices dont le rôle était jusqu’ici peu clair.
Saisir l’enzyme en action
Les chercheurs ont cristallisé la DPMS de P. furiosus avec ses substrats et suivi la réaction par cristallographie aux rayons X. Leur nouvelle structure, combinée à trois structures antérieures, capture une série d’instantanés autour du moment où le sucre est transféré. Dans un état, la molécule donneuse (GDP-mannose) et un accepteur de type Dol-P sont liés dans une géométrie précise qui place le carbone réactif du mannose directement en face du groupe phosphate du Dol-P — une configuration « pré-transfert » idéale. Des boucles de l’enzyme agissent comme des portes avant et arrière : elles se ferment pour maintenir le donneur et l’ion métallique en place, puis se réarrangent pour ouvrir un passage permettant au Dol-P d’entrer et au GDP vidé de sortir une fois le sucre transféré. Ces détails éclairent la manière dont l’enzyme assure un transfert de sucre efficace et précis à la surface membranaire.
Un produit renversé caché dans la membrane
Plus surprenant fut un second état distinct observé dans les mêmes cristaux. Ici, la molécule Dol-P-Man finie n’est pas au site actif mais logée plus profondément dans la partie transmembranaire de la protéine, dans une orientation « renversée ». Sa tête sucre–phosphate repose dans une poche polaire entre deux paires d’hélices (TMD1 et TMD2), tandis que la queue hydrophobe longe une gouttière formée par les hélices. Un acide aminé clé, une phénylalanine, semble agir comme une porte pouvant bloquer ou ouvrir l’accès à cette poche. La qualité de la densité électronique et la manière dont la protéine s’empile dans le cristal suggèrent que ce Dol-P-Man basculé n’est pas un artefact de contacts cristallins, mais un état authentique et bien peuplé que l’enzyme peut adopter.
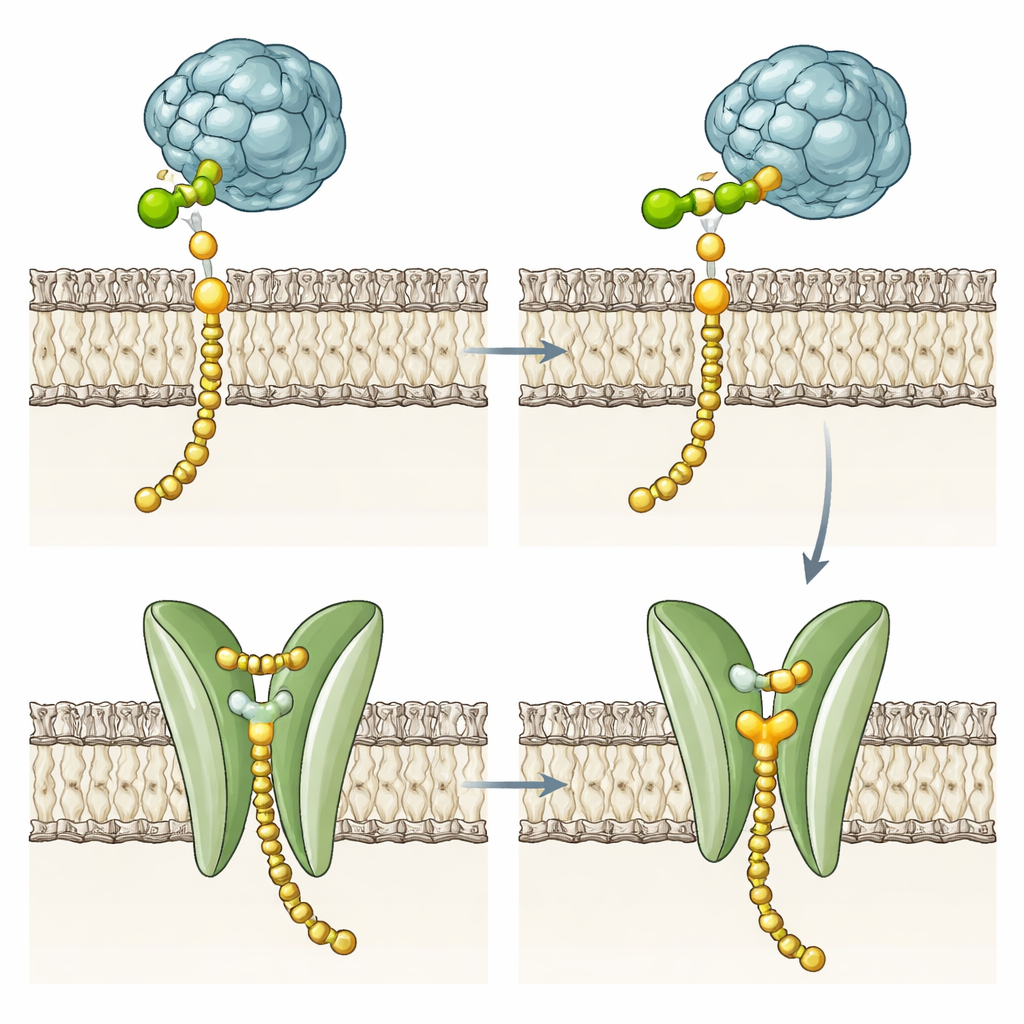
Des enzymes mutantes suggèrent une seconde fonction
Pour tester si le domaine transmembranaire est nécessaire à la chimie du transfert de sucre, l’équipe a conçu de multiples variantes. Ils ont supprimé la plupart ou la totalité des hélices, les ont remplacées par un segment membranaire différent provenant de la DPMS de levure, ou ont modifié des résidus clés de la poche et la phénylalanine portière. De façon remarquable, ces mutants produisaient encore du Dol-P-Man à des vitesses similaires à l’enzyme intacte, bien que certains soient légèrement moins stables dans la membrane. Cela montre que la chimie centrale réside dans la région catalytique soluble et que le faisceau de quatre hélices n’est pas nécessaire pour attacher le mannose au Dol-P. En revanche, sa poche polaire conservée, la gouttière et le résidu de fermeture suggèrent un rôle spécialisé dans la gestion du produit fini, en particulier chez les archées hyperthermophiles dont les membranes rigides rendent le basculement spontané des lipides coûteux en énergie.
Pourquoi une enzyme à double fonction est importante
En mettant ensemble les preuves structurales et mutationnelles, les auteurs proposent que la DPMS de type III soit une protéine « moonlighting ». D’abord elle synthétise le Dol-P-Man sur la face interne de la membrane plasmique archéale ; ensuite son domaine transmembranaire pourrait aider à faire basculer la molécule sucre–lipide afin que le groupe tête apparaisse à l’extérieur de la cellule, prêt à être utilisé par d’autres enzymes qui construisent la couche de sucres de la cellule. L’évolution semble avoir favorisé ce design chimérique principalement chez les archées extrêmement thermophiles, où rapprocher le site de synthèse d’une gouttière dédiée au basculement pourrait minimiser les pertes et les dommages thermiques. Bien que ce travail ne démontre pas encore directement une activité de basculement, il fournit un modèle structural concret expliquant comment une enzyme peut à la fois créer et repositionner un intermédiaire lipidique vital à travers une barrière membranaire sévère.
Citation: Gandini, R., Keskitalo, M.M., Reichenbach, T. et al. Crystallographic data for Pyrococcus furiosus dolichylphosphate mannose synthase suggest that the enzyme could flip its glycolipid product. Sci Rep 16, 9076 (2026). https://doi.org/10.1038/s41598-026-44343-5
Mots-clés: dolichylphosphate mannose, flippase lipidique, archées, glycosylation des protéines, enzymes membranaires