Clear Sky Science · fr
Analyse des prothèses valvulaires aortiques par imagerie cardiovasculaire avancée — une approche translationnelle inversée spécifique au patient
Pourquoi le choix des valves cardiaques compte
À mesure que davantage de personnes vivent assez longtemps pour développer des valves cardiaques usées, les médecins remplacent ces petites portes du cœur par des dispositifs artificiels. Aujourd’hui, de nombreux patients reçoivent des valves introduites par voie vasculaire, évitant ainsi une chirurgie à cœur ouvert, tandis que d’autres bénéficient de nouvelles valves chirurgicales « à déploiement rapide » conçues pour accélérer l’intervention. Cependant, ces dispositifs ne se valent pas tous. Cette étude examine en détail quatre prothèses aortiques largement utilisées pour déterminer comment elles modifient réellement l’écoulement sanguin, en utilisant un modèle grandeur nature imprimé en 3D de l’aorte d’un patient et des outils d’imagerie de pointe.
Construire un banc d’essai réaliste
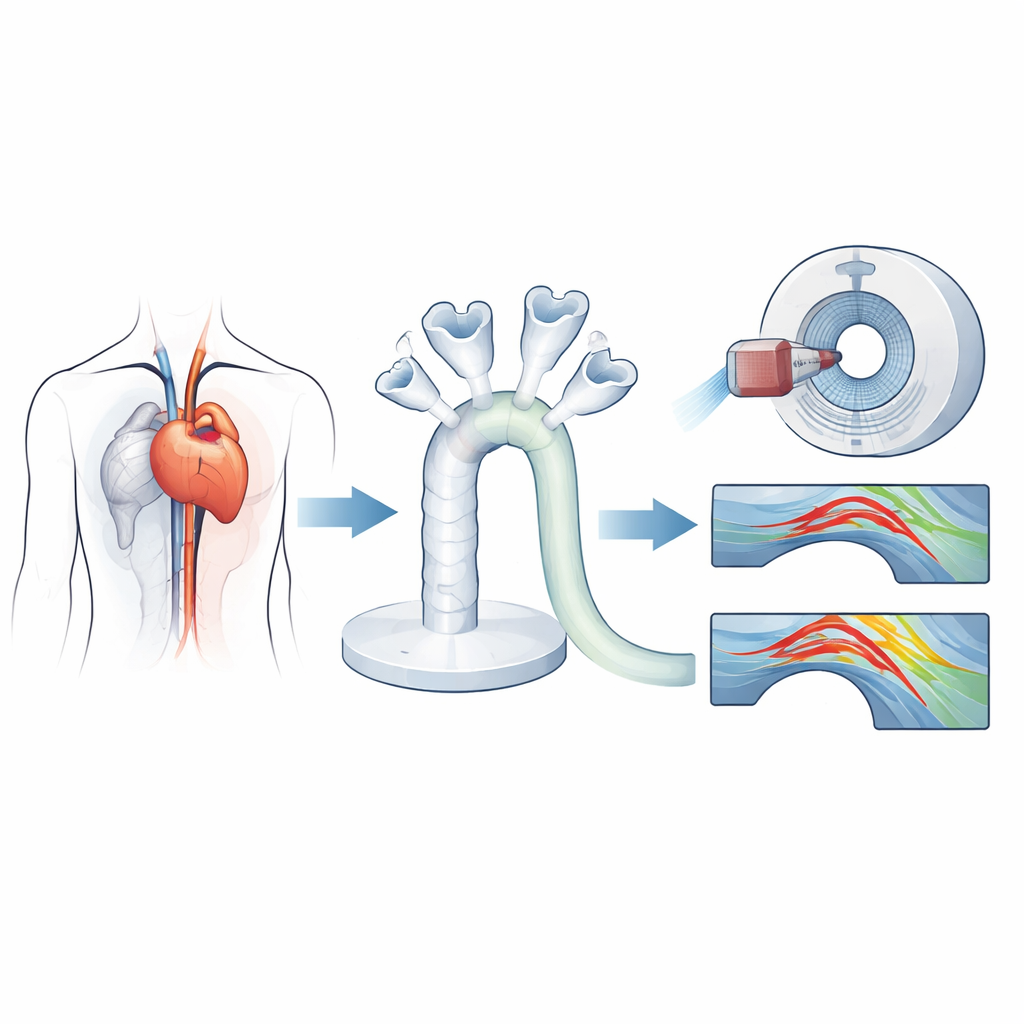
Les chercheurs ont commencé par un scanner CT haute résolution d’une femme dont la valve aortique naturelle nécessitait un remplacement et dont l’orifice valvulaire était plutôt petit — une situation fréquente et cliniquement délicate. À partir de ce scan, ils ont reconstruit numériquement sa racine aortique et son arc, puis imprimé en 3D un modèle flexible et transparent de son aorte. Dans des copies identiques de ce fantôme, ils ont implanté quatre valves biologiques modernes : deux valves chirurgicales à déploiement rapide et deux valves délivrées par cathéter, comme en remplacement valvulaire aortique transcathéter. Une pompe commandée par ordinateur a poussé un fluide simulant du sang à travers ce système, reproduisant un battement cardiaque normal, la pression et le débit, afin que chaque prothèse puisse être testée dans les mêmes conditions réalistes.
Observer le mouvement du sang en quatre dimensions
Pour voir comment chaque valve remodelait l’écoulement sanguin, l’équipe a combiné deux méthodes d’imagerie avancées. L’échographie vectorielle a fourni des cartes en temps réel de la vitesse et de la direction du fluide à des sections transversales clés de l’aorte ascendante. L’IRM 4D flow a ensuite capturé les motifs d’écoulement tridimensionnels au fil du temps, permettant aux chercheurs de calculer des grandeurs détaillées telles que la contrainte de cisaillement pariétale (la friction du sang glissant le long de la paroi), les pertes de charge le long de l’aorte, la perte d’énergie cinétique et la surface d’ouverture effective par laquelle le sang passait réellement. Ensemble, ces mesures ont révélé non seulement si le sang passait à travers la valve, mais aussi à quel point il circulait de manière fluide ou turbulente en aval.
Valves différentes, histoires d’écoulement différentes
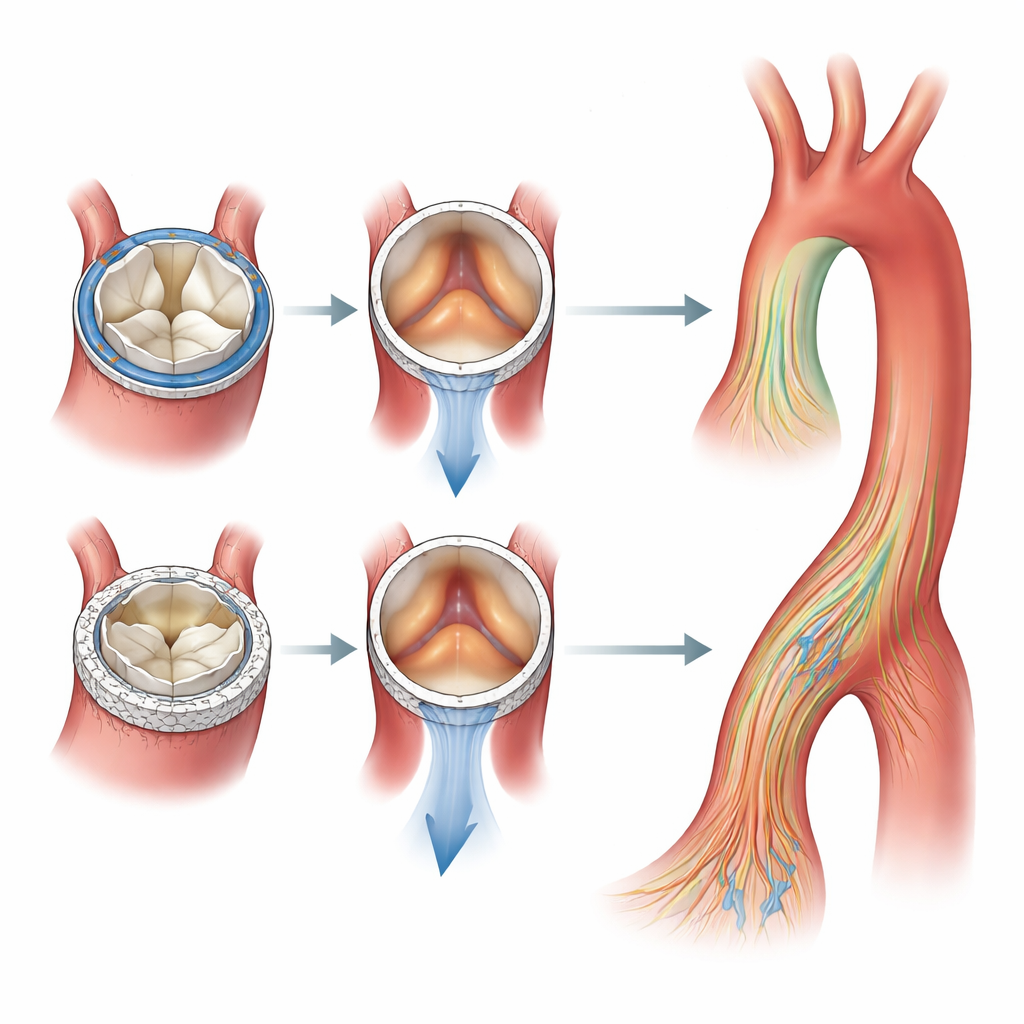
L’étude a montré que les deux valves délivrées par cathéter et les deux valves chirurgicales à déploiement rapide produisaient des comportements d’écoulement sensiblement différents, bien qu’elles aient toutes été formellement dimensionnées pour la même anatomie du patient. En général, les valves à déploiement rapide ont généré des vitesses d’écoulement moyennes plus élevées que les valves cathéter, tandis que ces dernières avaient tendance à produire un jet d’ouverture en forme plus triangulaire. Un modèle à déploiement rapide a présenté une perte d’énergie cinétique et des gradients de pression particulièrement élevés le long de l’aorte, ce qui signifie qu’une plus grande part d’énergie était dissipée pour propulser le sang à travers et au-delà de la valve. En revanche, une autre valve à déploiement rapide, avec une aire d’ouverture effective légèrement plus grande, a permis au sang de passer avec moins de résistance et une perte d’énergie plus faible, malgré un marquage pour le même diamètre d’annulus nominal.
Motifs d’écoulement subtils et contraintes sur le vaisseau
Lorsque l’équipe a examiné les forces agissant sur la paroi vasculaire, elle a observé des poches de contrainte de cisaillement élevée à des sites prévisibles : près de la racine aortique, le long de la courbure externe de l’aorte ascendante, autour de l’arc et dans certaines parties de l’aorte descendante. Ces points chauds sont apparus pour les quatre valves, et il n’y avait pas de différences spectaculaires dans leur localisation entre dispositifs chirurgicaux et cathéter. Néanmoins, la répartition et l’amplitude des jets d’écoulement et des zones tourbillonnaires différaient d’une manière qui pourrait avoir des conséquences à long terme, influençant potentiellement la façon dont la paroi vasculaire se remodèle ou la tolérance d’un patient particulier à une prothèse donnée.
Vers une sélection de valves plus personnalisée
Pour les non-spécialistes, le message clé est que choisir une valve cardiaque n’est pas aussi simple que d’assortir une taille indiquée à une ouverture mesurée. Dans ce modèle spécifique au patient et soigneusement contrôlé, des valves destinées à la même anatomie se sont comportées de manière assez différente, une valve à déploiement rapide s’avérant la plus efficace énergétiquement et la plus douce pour le vaisseau dans l’ensemble. Ces travaux montrent que les aortes imprimées en 3D combinées à l’imagerie avancée peuvent servir de piste d’essai pour les valves nouvelles et existantes, aidant les médecins à anticiper la performance d’un dispositif dans un corps particulier. À terme, ce type d’approche pourrait conduire à des normes plus claires pour le dimensionnement et la sélection des valves, réduire les inadéquations entre valves et patients, et faciliter l’ajustement des thérapies valvulaires salvatrices à chaque individu.
Citation: Grefen, L., Herz, C., Flexeder, J. et al. Analysis of aortic valve prostheses using advanced cardiovascular imaging—a patient-specific reversed translational approach. Sci Rep 16, 9334 (2026). https://doi.org/10.1038/s41598-026-44295-w
Mots-clés: remplacement de la valve aortique, prothèse valvulaire cardiaque, aorte imprimée en 3D, IRM 4D flow, valve transcathéter