Clear Sky Science · fr
Modélisation de la pathogénie des toxines de Clostridioides difficile et protection par antisérum sur une plateforme intestin‑sur‑puce immunocompétente
Pourquoi ce modèle d’infection intestinale est important
Les antibiotiques sauvent des vies, mais ils peuvent aussi rendre l’intestin vulnérable à des infections dangereuses. L’un des coupables les plus redoutables est Clostridioides difficile, une bactérie pouvant provoquer une diarrhée sévère et une inflammation du côlon menaçant le pronostic vital, en particulier chez les patients hospitalisés. Cette étude présente un « intestin sur puce » miniature qui recrée des éléments clés de l’intestin humain, y compris des vaisseaux sanguins et des cellules immunitaires, pour observer en temps réel comment les toxines de C. difficile endommagent l’intestin et comment des traitements par anticorps peuvent prévenir ces lésions.
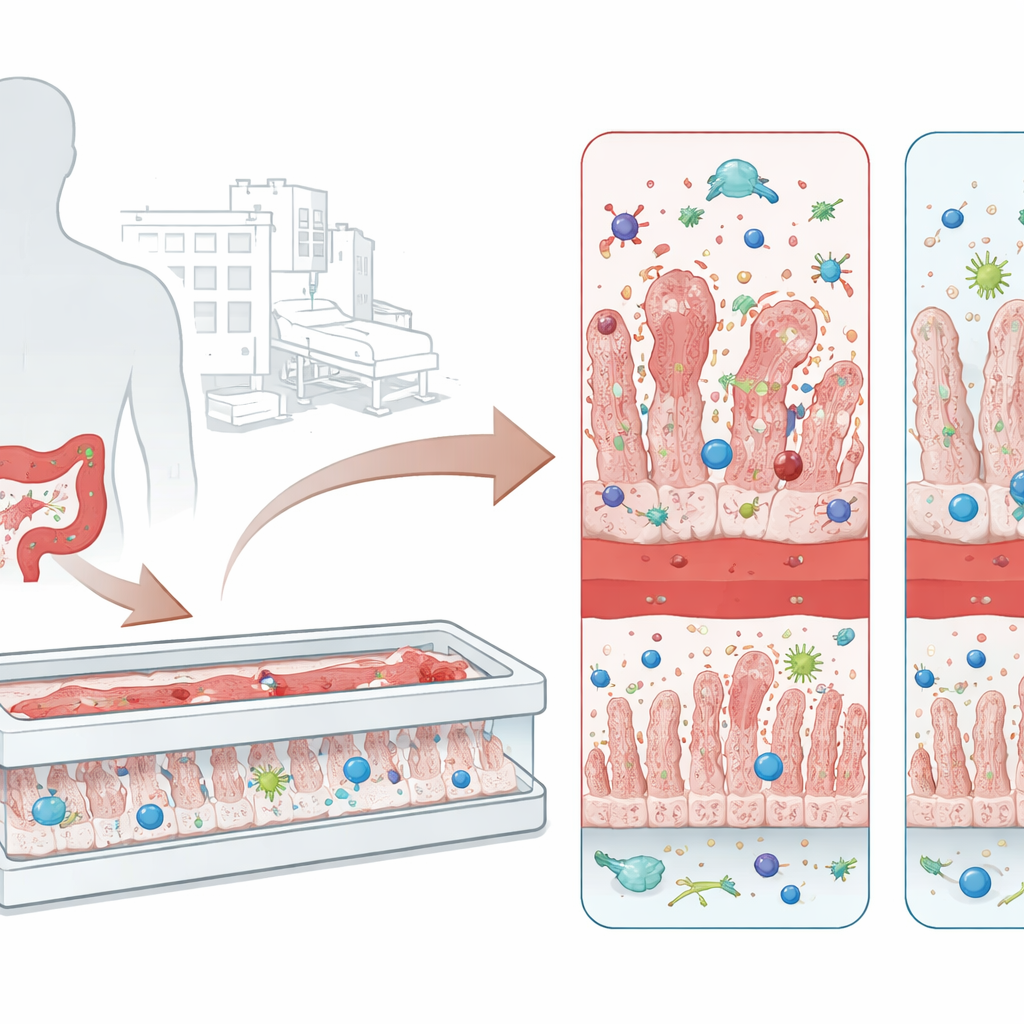
D’un germe hospitalier tenace aux lésions intestinales
C. difficile prospère chez les personnes dont la flore intestinale normale a été perturbée, souvent après un traitement par antibiotiques à large spectre. Le microbe survit à des conditions difficiles sous forme de spores robustes et, une fois établi dans le côlon, libère deux toxines majeures connues sous les noms de TcdA et TcdB. Ces toxines attaquent les cellules intestinales, relâchent les jonctions entre elles et déclenchent des vagues d’inflammation. Les conséquences vont d’une diarrhée persistante à une colite pseudomembraneuse, caractérisée par des plaques de tissu nécrosé et d’accumulation de cellules immunitaires tapissant la paroi intestinale. Les traitements actuels reposent principalement sur d’autres antibiotiques et parfois sur des transplantations fécales, pourtant de nombreux patients subissent des réinfections, ce qui souligne le besoin de meilleures méthodes pour étudier la maladie et tester des thérapies bloquant les toxines.
Construire un petit intestin vivant sur une puce
Les modèles de laboratoire traditionnels cultivent une couche plate de cellules intestinales dans une boîte de culture. Utile, cette culture bidimensionnelle n’inclut toutefois ni vaisseaux sanguins, ni cellules immunitaires, ni l’écoulement doux de fluide qui caractérise l’intestin réel. Les chercheurs ont donc utilisé un dispositif micro‑ingénierie « intestin‑sur‑puce » comportant deux canaux parallèles séparés par une membrane poreuse. Un côté est tapissé de cellules intestinales qui se développent en crêtes semblables à des villosités et forment une barrière étanche. Le côté opposé contient des cellules endothéliales de vaisseaux sanguins humains. Dans ce tissu miniature, l’équipe a ajouté des macrophages dérivés de monocytes qui s’installent dans la paroi intestinale et des neutrophiles circulants capables de traverser le canal vasculaire et d’infiltrer le tissu, créant ainsi un intestin‑sur‑puce immunocompétent (i‑IoC) qui reproduit plus fidèlement l’intestin vivant.
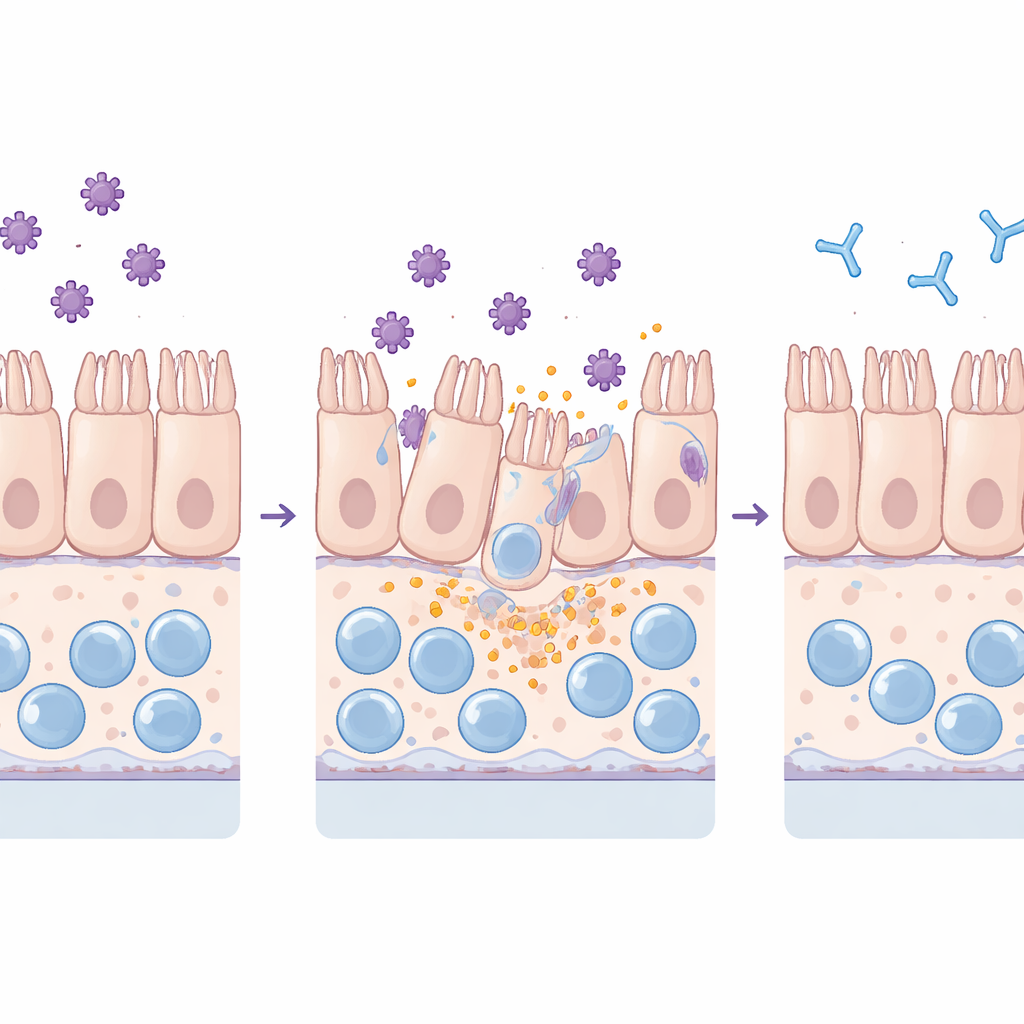
Observer les toxines attaquer la barrière
L’équipe a exposé à la fois des cultures plates standard et le modèle sur puce aux toxines purifiées TcdA et TcdB. Ils ont suivi la capacité de la barrière intestinale à retenir un colorant fluorescent, examiné les protéines de jonction qui lient les cellules voisines et mesuré les molécules inflammatoires ainsi que les marqueurs de lésion cellulaire dans le fluide environnant. Les deux toxines ont endommagé les tissus, mais de façons distinctes : la TcdA a principalement perturbé les jonctions serrées et provoqué un arrondi des cellules, tandis que la TcdB a entraîné une perte étendue de cellules de la couche. Crucialement, la puce a détecté ces effets à des concentrations de toxine bien plus faibles que les cultures plates, reflétant sa sensibilité supérieure et un comportement plus proche de la physiologie sous flux continu.
Les cellules immunitaires amplifient l’inflammation — et peuvent être protégées
L’ajout de macrophages et de neutrophiles sur la puce a amplifié la réponse aux toxines. Les macrophages ont augmenté la libération de médiateurs inflammatoires clés tels que l’IL‑6 et l’IL‑8 mais ont eux‑mêmes été épuisés, cohérent avec une forme de mort cellulaire inflammatoire. Les neutrophiles se sont adhérés à la paroi vasculaire et ont migré dans le tissu intestinal, rappelant l’afflux de cellules immunitaires observé chez les patients. Une exposition prolongée aux toxines a endommagé non seulement la muqueuse intestinale mais aussi, finalement, la couche vasculaire. Lorsque les chercheurs ont pré‑mélangé les toxines avec des sérums d’anticorps neutralisants, néanmoins, les dommages structurels, les fuites de barrière, les pics de cytokines, la perte de macrophages et l’infiltration des neutrophiles ont été fortement réduits. Dans des expériences prolongées, les tissus lésés par la TcdB ont pu récupérer partiellement une fois les toxines retirées, alors que la TcdA laissait des dommages plus persistants, suggérant des capacités de réparation différentes selon la toxine.
Ce que cela signifie pour les patients et les thérapies
Pour un lecteur non spécialiste, le message principal est que ce petit modèle d’intestin vivant peut reproduire de façon réaliste la manière dont les toxines de C. difficile blessent l’intestin et activent le système immunitaire, tout en montrant l’efficacité des anticorps antitoxines pour protéger le tissu. Comparé aux couches cellulaires simples, l’intestin‑sur‑puce est plus sensible, inclut vaisseaux et cellules immunitaires, et peut fonctionner pendant plusieurs jours pour capter à la fois les dommages précoces et les tentatives de récupération. Cela en fait une plateforme prometteuse pour tester des traitements et des vaccins de nouvelle génération qui neutralisent les toxines sans perturber davantage le microbiote intestinal, et potentiellement un outil pour personnaliser les thérapies à partir de cellules dérivées de patients à l’avenir.
Citation: Wegner, V.D., Warschinke, M., Brahim, I.B. et al. Modeling Clostridioides difficile toxin pathogenesis and antiserum protection in an immunocompetent intestine-on-chip platform. Sci Rep 16, 9233 (2026). https://doi.org/10.1038/s41598-026-44170-8
Mots-clés: Clostridioides difficile, intestin‑sur‑puce, infection intestinale, anticorps neutralisants, modèles organes‑sur‑puce