Clear Sky Science · fr
Absence du gène de la luciférase dans le génome du poisson bioluminescent kleptoprotéique Parapriacanthus ransonneti
Les poissons qui volent leur éclat
Quand nous pensons aux animaux lumineux, nous imaginons généralement des organismes qui produisent leur propre lumière grâce à des gènes spécifiques. Cette étude renverse cette idée. Le petit poisson de récif Parapriacanthus ransonneti brille dans l’obscurité, mais au lieu de porter la recette génétique de son outil producteur de lumière, il semble emprunter la protéine achevée aux petits crustacés dont il se nourrit. À la lecture de ce travail, un non-spécialiste peut entrevoir la souplesse du vivant — et voir comment l’évolution choisit parfois la stratégie « utilise-le plutôt que de le fabriquer ».
Une lumière empruntée à de minuscules proies
Les chercheurs savaient déjà que ce poisson éclaire grâce à la même protéine photogénique, appelée luciférase, qu’un ostracode bioluminescent, un petit crustacé planctonique. Des travaux antérieurs avaient montré que la luciférase trouvée chez le poisson est une correspondance exacte de la version de l’ostracode, et que les poissons perdent leur lumière s’ils sont maintenus pendant des mois sans proies lumineuses. Les alimenter avec un autre ostracode lumineux remplace la protéine dans les organes lumineux du poisson par celle-ci. Ces indices suggéraient que le poisson ne fabrique pas la luciférase lui-même mais la stocke à partir de son alimentation — un processus que les auteurs appellent « kleptoprotéinisme », littéralement le vol de protéines. Restait toutefois la possibilité que des gènes cachés de luciférase se dissimulent dans le génome du poisson au-delà de la portée des méthodes précédentes.

Lire le plan génétique du poisson
Pour trancher, les chercheurs ont construit une carte génétique de haute qualité, ou génome, pour Parapriacanthus ransonneti. Ils ont élevé soigneusement des poissons avec une nourriture non lumineuse pendant plus d’un an pour éviter toute contamination par l’ADN des proies, puis ont extrait et séquencé l’ADN du poisson lui‑même en utilisant une technologie de lectures longues de pointe. Le génome assemblé faisait environ 625 millions de « lettres », en accord avec des estimations indépendantes de taille et présentant très peu d’écarts. Ils ont ensuite prédit des dizaines de milliers de gènes et vérifié la qualité globale avec des référentiels standards, confirmant que presque tous les gènes de poisson attendus étaient présents. En d’autres termes, il s’agissait d’une carte solide et presque complète sur laquelle un gène de luciférase, s’il existait, devrait être visible.
À la recherche d’un gène disparu
Muni de ce génome, l’équipe s’est lancée dans une chasse ciblée. Ils ont comparé des séquences de luciférase connues provenant de plusieurs ostracodes lumineux aux protéines prédites du poisson, à ses chromosomes assemblés, et même aux lectures d’ADN brutes non assemblées. Plusieurs outils de recherche aux forces complémentaires ont été utilisés pour éviter les angles morts. À maintes reprises, aucune correspondance véritable de luciférase n’est apparue. Quelques gènes du poisson présentaient une similarité lointaine, mais une inspection plus poussée a révélé qu’ils appartenaient à une famille commune de protéines liées au système immunitaire, pas à des enzymes productrices de lumière, et leurs arbres évolutifs reflétaient l’histoire ordinaire des poissons plutôt que tout signe d’un emprunt récent aux crustacés. L’absence de luciférase non seulement dans le génome poli mais aussi dans les données brutes de séquençage rend extrêmement improbable que le gène se cache simplement dans un coin non assemblé.
Vérifier d’autres raccourcis génétiques
Les scientifiques se sont aussi demandé si le poisson avait pu discrètement importer d’autres gènes utiles d’ostracodes, par exemple ceux impliqués dans la gestion de la molécule photogène luciférine. À l’aide d’outils rapides de comparaison à grande échelle, ils ont scanné chaque protéine prédite du poisson contre des bases de données de protéines de poissons et d’ostracodes et ont signalé les cas où un gène de poisson ressemblait davantage à un gène d’ostracode qu’à ceux d’autres poissons. Environ vingt candidats sont apparus, mais des arbres évolutifs détaillés ont montré que ces gènes restaient bien regroupés avec les poissons, et non dans des branches d’ostracodes. En bref, il n’y avait aucun signe convaincant que des gènes, y compris ceux qui traitent la luciférine, aient sauté latéralement des crustacés vers l’ADN de ce poisson.
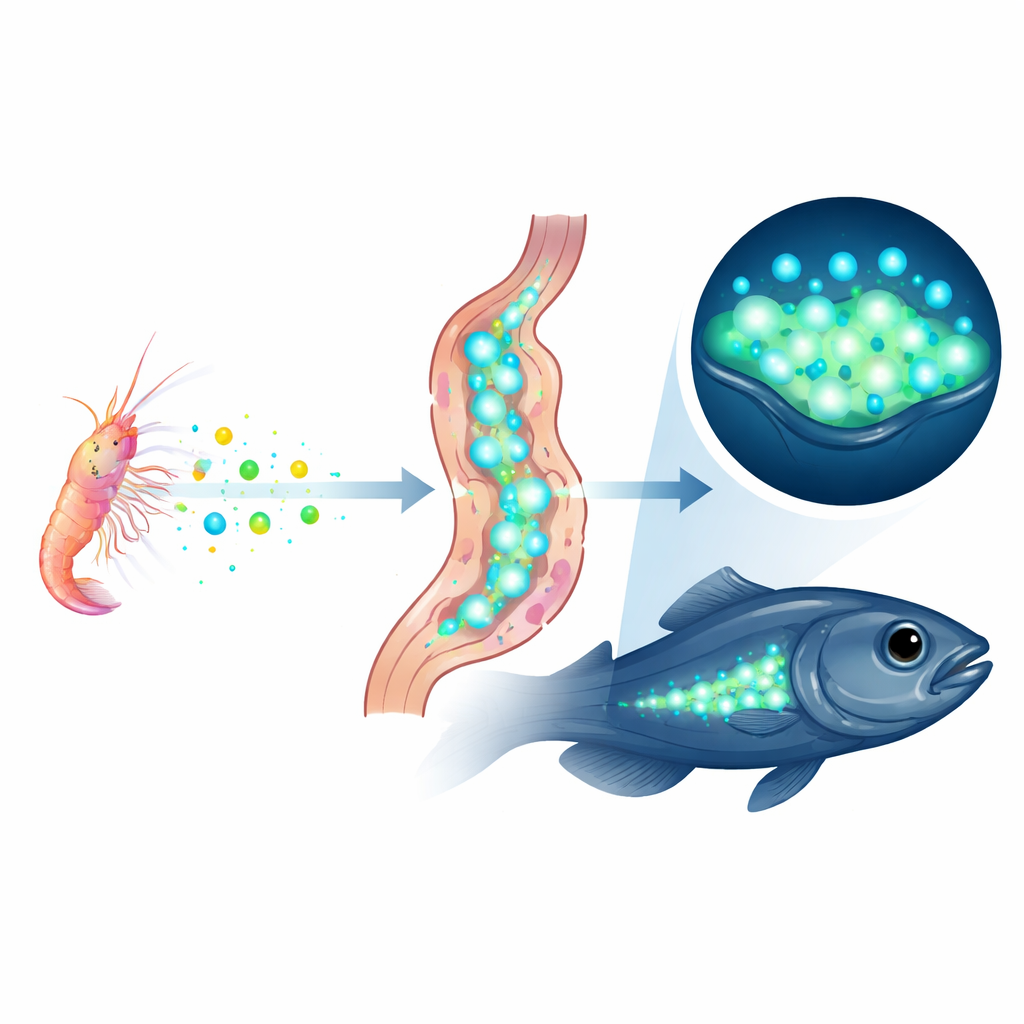
Une nouvelle façon de briller
Pris ensemble, les éléments de preuve convergent vers une conclusion frappante : Parapriacanthus ransonneti éclaire sans posséder les instructions génétiques pour son enzyme clé de production de lumière. À la place, il capture des protéines luciférases prêtes à l’emploi des ostracodes qu’il mange et les stocke dans ses organes lumineux, un exemple vivant du « tu es ce que tu manges » poussé au niveau moléculaire. Cela montre que les animaux peuvent acquérir des capacités complexes non seulement en évoluant ou en important de nouveaux gènes, mais aussi en réutilisant directement les pièces fonctionnelles d’autres espèces. Le génome nouvellement assemblé offre désormais une plateforme pour des travaux futurs visant à découvrir comment le poisson transporte, protège et contrôle ces protéines volées — et à quelle fréquence la nature emploie des astuces similaires chez d’autres organismes lumineux.
Citation: Bessho-Uehara, M., Yamaguchi, K., Koeda, K. et al. Absence of the luciferase gene in the genome of the kleptoprotein bioluminescent fish Parapriacanthus ransonneti. Sci Rep 16, 9211 (2026). https://doi.org/10.1038/s41598-026-43942-6
Mots-clés: poisson bioluminescent, séquestration de protéines, kleptobiologie, luciférase, séquençage du génome