Clear Sky Science · fr
Élucider la relation entre affinité et puissance dans l’efficacité des IgE thérapeutiques
Retourner les anticorps allergiques contre le cancer
Les personnes souffrant d’allergies connaissent la puissance des anticorps IgE — les molécules qui déclenchent les yeux qui piquent et les éternuements soudains. Cette étude pose une question surprenante : cette même biologie puissante peut‑elle être réorientée pour combattre le cancer, et si oui, comment faut‑il exactement ajuster ces anticorps pour qu’ils fonctionnent au mieux ? Les chercheurs se sont focalisés sur les cancers du sein exprimant la protéine HER2, y compris les cas où HER2 est présent à de très faibles niveaux et où les traitements actuels échouent souvent.
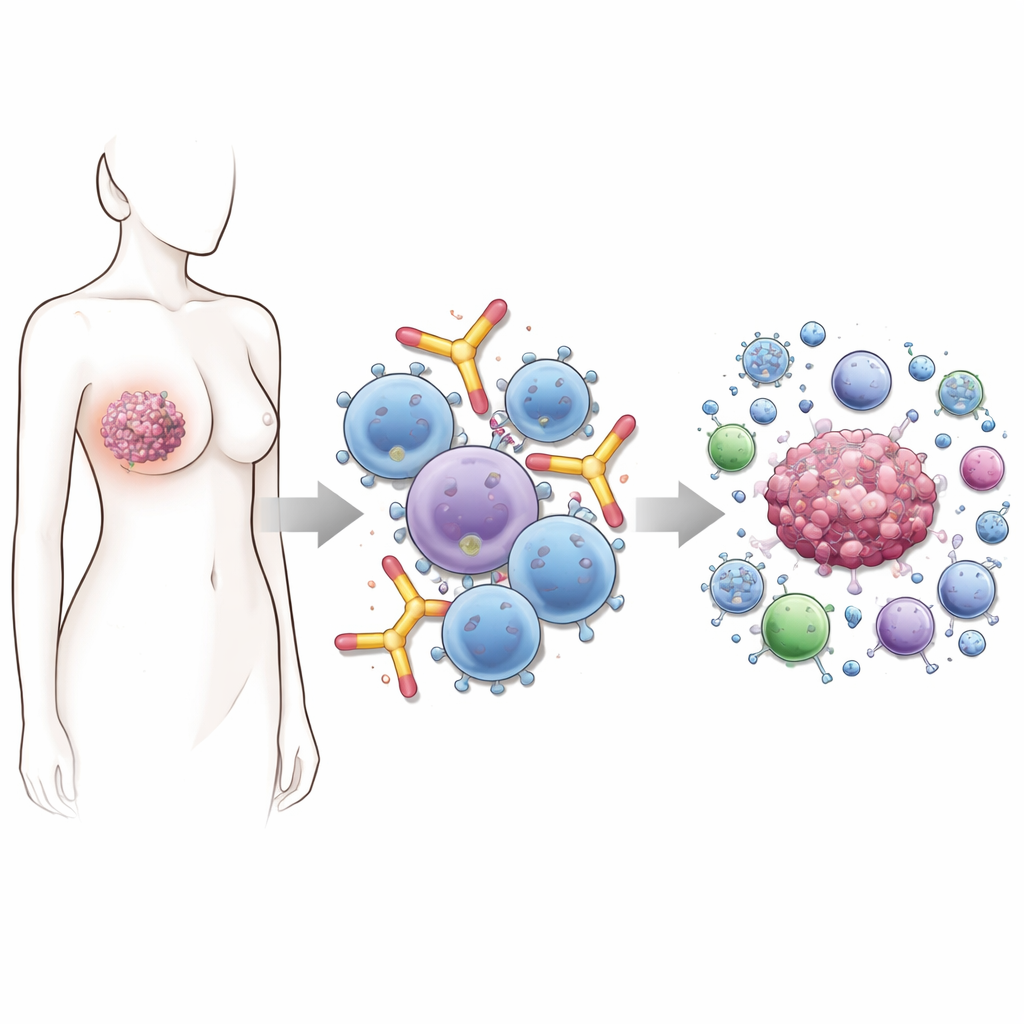
Pourquoi cette classe d’anticorps est si particulière
La plupart des anticorps thérapeutiques sur le marché appartiennent à la classe IgG. Ce sont les chevaux de trait de la thérapie anticancéreuse moderne, mais ils ont des limites — notamment lorsque les tumeurs échappent à l’attaque en réduisant la quantité de protéine cible à leur surface. Les IgE sont différentes. Elles se lient naturellement très fortement à des cellules immunitaires comme les mastocytes, les basophiles, les monocytes et les macrophages, les préparant à des réponses rapides. Dans les allergies, cela se traduit par des réactions explosives au pollen ou à certains aliments. Dans le cancer, la même architecture pourrait permettre des attaques rapides et ciblées sur les cellules tumorales dès que l’IgE reconnaît sa cible à la surface tumorale.
Concevoir une IgE plus précise pour traquer le cancer
L’équipe avait précédemment créé un anticorps IgE, nommé EPS 226, qui reconnaît HER2 sur les cellules du cancer du sein et peut ralentir la croissance tumorale dans des modèles expérimentaux. Dans ce nouveau travail, ils ont cherché à répondre à une question subtile mais cruciale de conception : augmenter l’affinité de l’anticorps pour HER2 améliore‑t‑elle réellement sa capacité à mobiliser le système immunitaire, ou l’avidité naturelle « multi‑points » de l’IgE fait‑elle déjà l’essentiel du travail ? Pour explorer cela, ils ont utilisé une approche de mutagenèse ciblée et de sélection en bactérie pour générer des millions de petites variantes de la région de liaison à HER2, puis ont isolé 12 nouvelles variantes d’IgE qui se liaient à HER2 plus fortement que l’anticorps d’origine.
Évaluer la puissance sur cellules et animaux
Ces anticorps améliorés ont ensuite été soumis à une série d’expériences cellulaires exigeantes. Lorsqu’ils étaient chargés sur des mastocytes et exposés à des cellules cancéreuses HER2‑positives, la plupart des IgE à liaison renforcée ont déclenché une dégranulation plus importante — une réponse d’activation qui libère des médiateurs immunitaires puissants. Une variante, rebaptisée EPS 232, s’est distinguée par sa capacité à activer les cellules tout en se liant efficacement à HER2 sur des cellules tumorales humaines et de rat. Des tests supplémentaires ont montré que EPS 232 mieux outillait les cellules immunitaires pour tuer le cancer : elle augmentait la cytotoxicité des basophiles et favorisait une phagocytose plus efficace des cellules tumorales HER2‑positives par des cellules immunitaires modifiées et par des macrophages humains primaires. Il est intéressant de noter que l’augmentation de l’affinité n’a aidé que jusqu’à un certain point ; les variantes à affinité extrêmement élevée ne surpassaient pas EPS 232, ce qui suggère l’existence d’un « point optimal » où la liaison est suffisamment forte pour être efficace sans nuire à la capacité d’engagement simultané de multiples anticorps et cellules immunitaires par cellule tumorale.
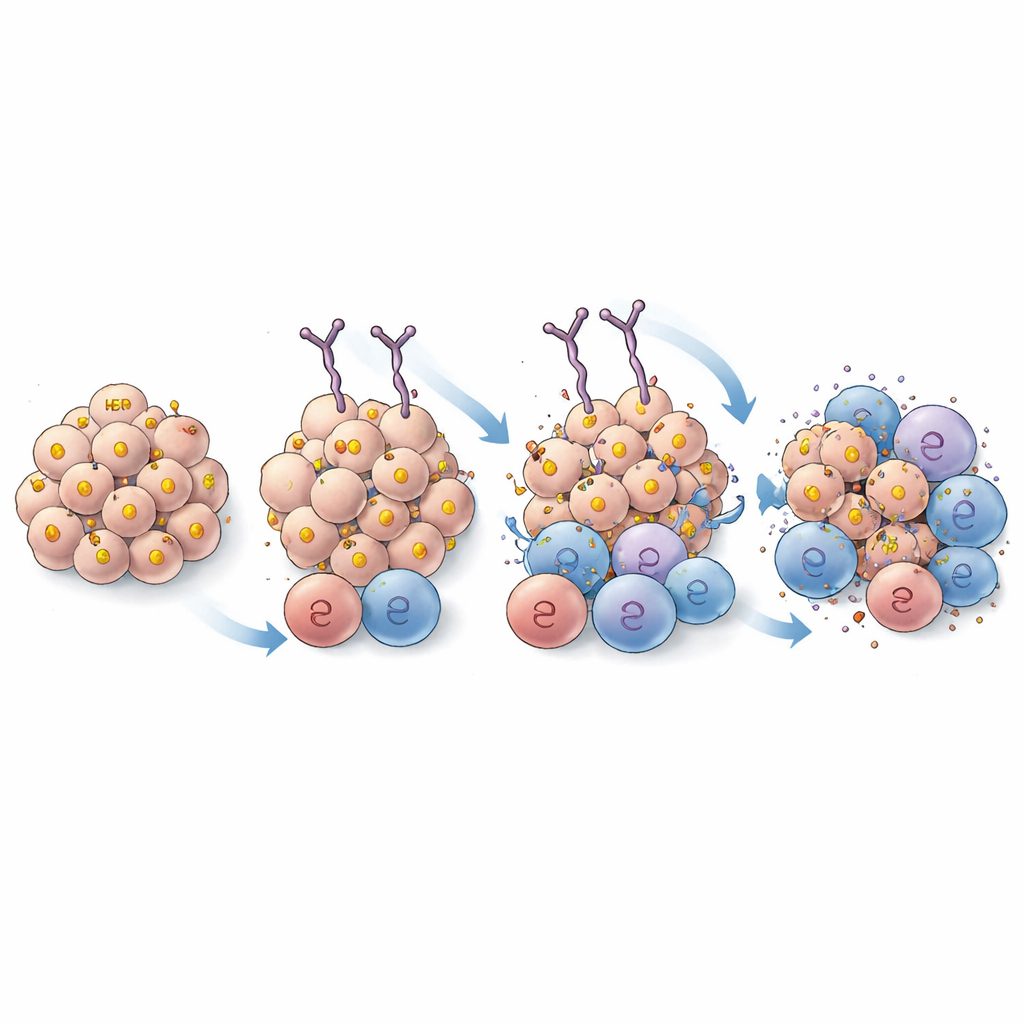
Approfondir la manière dont l’anticorps se lie
Pour s’assurer que les gains provenaient d’une affinité accrue plutôt que de la reconnaissance d’un nouvel épitope de HER2, les scientifiques ont utilisé la cryo‑microscopie électronique à haute résolution pour visualiser comment EPS 232 et l’EPS 226 originale se positionnent sur la protéine HER2. Les structures ont montré que les deux anticorps se fixent sur la même région de HER2 et utilisent des points de contact très similaires, avec seulement des différences subtiles qui ne devraient pas modifier le site de liaison global. Cela étaye l’idée que l’amélioration des performances d’EPS 232 provient d’une affinité accrue plutôt que d’un changement de cible.
Du laboratoire au contrôle tumoral
Le véritable test a eu lieu dans des modèles animaux. Chez des souris porteuses de tumeurs mammaires humaines et dotées de cellules immunitaires humaines, EPS 232 a freiné la croissance tumorale plus efficacement et à des doses plus faibles que EPS 226. Chez des rats porteurs d’un modèle agressif de cancer du sein exprimant des niveaux ultra‑faibles de HER2 — similaire à certains cancers du sein triple négatif — une version adaptée d’EPS 232 pour le rat a non seulement ralenti davantage la croissance tumorale que sa prédécesseure, mais a aussi prolongé la survie. Les tumeurs d’animaux traités montraient une plus forte infiltration de lymphocytes T et de macrophages, indiquant que l’anticorps amélioré remodelait mieux le microenvironnement tumoral en faveur d’une attaque immunitaire.
Ce que cela signifie pour les thérapies anticancéreuses futures
Pour le lecteur général, le message principal est que peaufiner la force avec laquelle un anticorps IgE saisit sa cible tumorale peut réellement modifier son efficacité, même si l’IgE établit déjà de nombreux contacts simultanés avec les cellules. L’étude identifie EPS 232 comme un candidat IgE prometteur contre les cancers du sein HER2‑positifs et HER2‑faibles, y compris des formes aujourd’hui difficiles à traiter. Plus largement, elle montre que les anticorps « dans le style des allergies » peuvent être conçus avec le juste équilibre d’affinité pour transformer un système hyper‑réactif provoquant des éternuements en un outil qui aide le système immunitaire à repérer et éliminer les tumeurs.
Citation: Marano, F., McKenzie, C., Birtley, J.R. et al. Elucidating the relationship between affinity and potency in the performance of therapeutic IgE. Sci Rep 16, 10555 (2026). https://doi.org/10.1038/s41598-026-43772-6
Mots-clés: IgE thérapeutique, cancer du sein HER2, affinité d’anticorps, immunothérapie contre le cancer, cancer du sein triple négatif