Clear Sky Science · fr
La stratification par dose prescrite améliore la prédiction par apprentissage profond des doses VMAT pour le NSCLC localement avancé
Pourquoi des plans de radiothérapie plus intelligents comptent
Lorsque les médecins traitent un cancer du poumon avancé par radiation, ils naviguent sur une corde raide : délivrer suffisamment d’énergie pour contrôler la tumeur tout en préservant des organes sensibles à proximité. Concevoir ces plans est lent, complexe et dépend fortement de l’expertise du planificateur. Cette étude explore comment l’intelligence artificielle peut prédire la distribution de dose dans la poitrine et, surtout, montre que former l’IA avec des niveaux de dose regroupés de façon judicieuse rend ses prédictions plus précises et plus utiles en clinique.
Comment le cancer du poumon est traité par faisceaux focalisés
La plupart des personnes atteintes d’un carcinome pulmonaire non à petites cellules localement avancé ne peuvent pas bénéficier d’une résection chirurgicale. Elles reçoivent souvent une chimiothérapie associée à des faisceaux de radiation très conformés qui balayent la poitrine en arcs, une technique connue sous le nom de VMAT. L’objectif est d’irradier la tumeur avec une dose élevée et homogène tout en limitant l’exposition des poumons, du cœur, de l’œsophage et de la moelle épinière. Atteindre cet équilibre nécessite généralement plusieurs itérations d’essais et d’ajustements, qui prennent du temps et peuvent retarder les décisions thérapeutiques. Si les médecins pouvaient estimer rapidement quel schéma de dose est réalistement atteignable pour un patient donné, ils pourraient choisir plus tôt la meilleure stratégie de traitement.
Apprendre à un algorithme à repérer les schémas de dose
Les chercheurs se sont tournés vers l’apprentissage profond, une forme d’IA qui apprend les motifs directement à partir des images. Ils ont collecté les scanners (CT) et les plans de traitement finalisés de 72 patients atteints de cancer du poumon traités par VMAT. Pour chaque patient, ils ont recalculé comment le même dispositif de faisceaux délivrerait trois doses totales différentes : 50, 54 et 60 gray (Gy), les unités standard de radiothérapie. Chaque cas a été converti en une grille tridimensionnelle indiquant la tumeur, les organes clés et l’image CT sous-jacente. Ces neuf canaux d’information ont été fournis à un 3D U-Net, une architecture de réseau de neurones courante capable d’apprendre comment la dose a tendance à se répartir dans le corps en fonction de l’anatomie.
Pourquoi regrouper par dose prescrite est important
Une question centrale était la manière de gérer le fait que les patients reçoivent des doses totales différentes. L’équipe a construit quatre modèles d’IA par ailleurs identiques. Trois étaient des modèles « à prescription unique », chacun entraîné uniquement sur des plans d’un niveau de dose (50, 54 ou 60 Gy). Le quatrième modèle mélangeait des cas à 50 et 60 Gy sans indiquer au réseau quelle prescription il voyait. Lors des tests sur de nouveaux patients, les modèles spécifiques à la prescription ont mieux reproduit la dose réelle dans la tumeur, préservant à la fois la couverture et les points chauds proches des plans cliniques, généralement à quelques Gy près. En revanche, le modèle mixte a commis des erreurs sensiblement plus importantes dans les régions de dose maximale de la tumeur et autour de la moelle épinière, où la dose doit rester en dessous de limites de sécurité strictes.
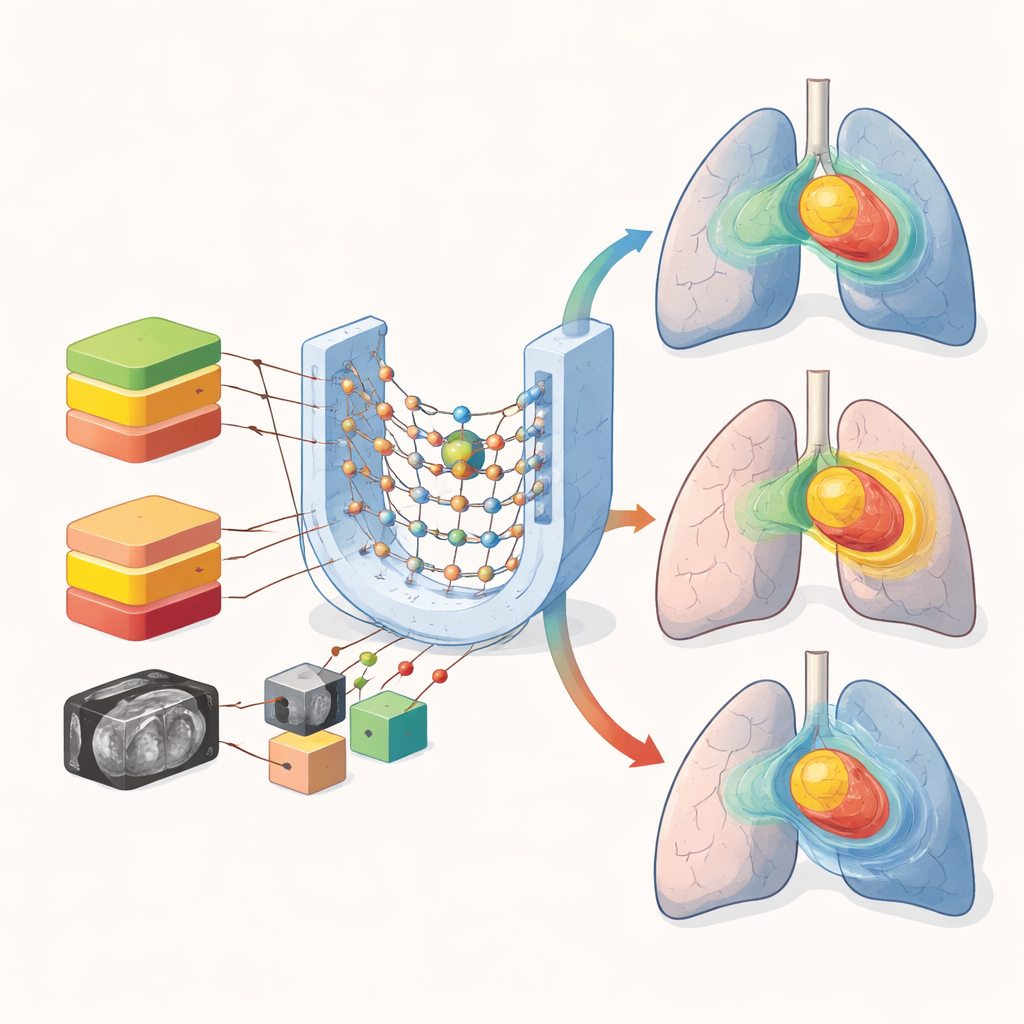
Protéger les organes vitaux tout en accélérant la planification
De manière intéressante, pour de nombreux organes tels que les poumons, le cœur et l’œsophage, les modèles mixtes et stratifiés ont des performances similaires. Les erreurs moyennes de dose pour ces structures plus étendues sont restées modestes quelle que soit l’approche. La principale faiblesse du mélange des prescriptions est apparue dans les petites structures sensibles comme la moelle épinière, où une chute rapide de dose est essentielle. Les contrôles visuels des cartes de dose prédites ont montré que tous les modèles capturaient la forme générale de la région à haute dose dans la tumeur, mais que le mélange des prescriptions entraînait davantage de flou dans les gradients raides et les zones de faible dose des poumons. Ces différences, bien que subtiles sur le plan numérique, peuvent avoir de l’importance quand les médecins jugent si une prescription plus élevée est sûre.
Ce que cela signifie pour les patients et les services
Pour les patients, ce travail ne remplace pas les calculs de dose précis déjà réalisés par les systèmes cliniques, mais il pourrait aider à concentrer le temps et les efforts sur des plans véritablement réalisables et sûrs. En montrant que regrouper les données d’entraînement par dose prescrite affine significativement les prédictions de l’IA—en particulier pour la couverture tumorale et la protection de la moelle épinière—l’étude met en évidence un choix de conception pratique qui peut rendre l’aide informatique plus fiable. Avec des tests complémentaires sur des cohortes plus larges et diversifiées, de tels modèles pourraient devenir des outils quotidiens offrant aux médecins un aperçu rapide, fondé sur l’anatomie, des compromis probables en radiothérapie, et soutenant une planification de traitement meilleure et plus cohérente.
Citation: Chaipanya, T., Nimjaroen, K., Chamchod, S. et al. Prescription‑dose stratification improves deep learning‑based VMAT dose prediction in locally advanced NSCLC. Sci Rep 16, 8707 (2026). https://doi.org/10.1038/s41598-026-43192-6
Mots-clés: radiothérapie du cancer du poumon, prédiction de dose par apprentissage profond, planification VMAT, optimisation du plan de traitement, organes à risque