Clear Sky Science · fr
Les schémas alimentaires influencent la capacité in silico de production de GABA de Bifidobacterium adolescentis HD17T2H et d’autres bactéries intestinales humaines
Pourquoi votre dîner peut influencer votre humeur
Beaucoup ont entendu dire que l’intestin est comme un « second cerveau », mais on comprend encore mal de quelle manière notre alimentation façonne ce monde microbien caché et, par ricochet, notre santé mentale et digestive. Cette étude examine un messager clé, l’acide gamma‑aminobutyrique (GABA), une substance qui calme l’activité nerveuse et est produite non seulement dans le cerveau mais aussi par des bactéries intestinales. Les chercheurs ont posé une question apparemment simple : si vous changez votre régime alimentaire, comment cela modifie‑t‑il la capacité des microbes intestinaux à produire du GABA ?
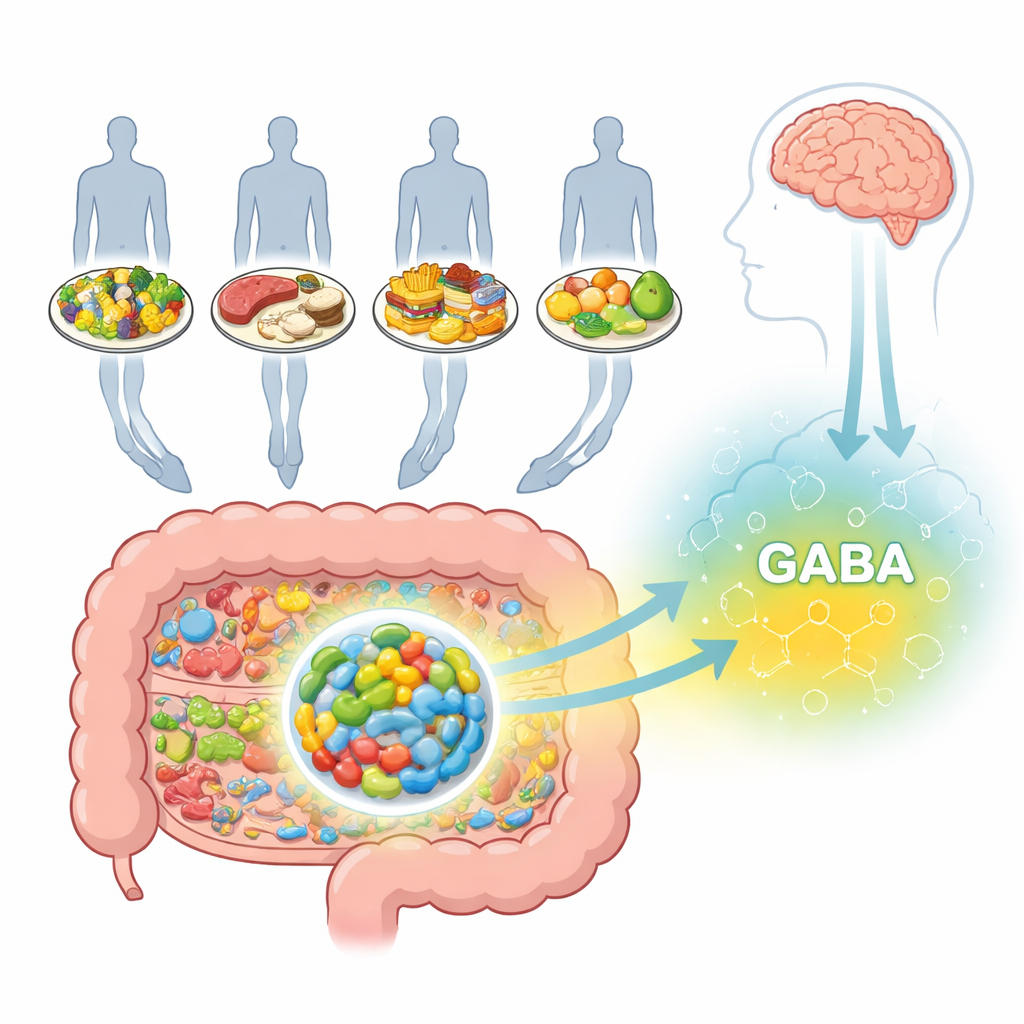
Un composé calmant fabriqué dans l’intestin
Le GABA est surtout connu comme un signal apaisant dans le cerveau, où il empêche les cellules nerveuses de devenir excessivement actives et a été associé à l’anxiété et à la dépression. Mais le GABA agit aussi directement dans l’intestin, où il influence le mouvement intestinal, la sécrétion de fluides et la libération d’hormones. Certaines bactéries intestinales peuvent transformer des nutriments courants en GABA via des voies biochimiques bien caractérisées. L’une d’elles, Bifidobacterium adolescentis HD17T2H, se distingue comme productrice de GABA et fait partie d’un groupe de bactéries souvent présentes dans les produits probiotiques. Jusqu’à présent, cependant, les scientifiques ne disposaient pas d’un tableau systématique de la façon dont différents modes d’alimentation pourraient modifier la capacité de cette bactérie à produire du GABA.
Utiliser des modèles informatiques comme intestin virtuel
Plutôt que de réaliser des dizaines d’expériences laborieuses en laboratoire, l’équipe a construit un modèle informatique détaillé de B. adolescentis sur la base de son génome. Ils ont ensuite « nourri » ce microbe virtuel avec onze régimes journaliers réalistes tirés d’une base de données nutritionnelle, incluant des régimes végétarien, végan, riche en protéines, européen moyen, méditerranéen, pauvre en glucides et cétogène. Grâce à des outils mathématiques estimant les flux de nutriments dans le métabolisme, les chercheurs ont calculé quelle quantité de GABA la bactérie pouvait théoriquement sécréter sous chaque régime, tout en continuant de croître. Ils ont aussi effectué des milliers de tests virtuels de « supplémentation », ajoutant in silico des quantités supplémentaires de nutriments individuels pour voir lesquels augmentaient le plus la production de GABA.
Comment différents régimes modèlent le potentiel de GABA
Les simulations ont révélé des différences marquées entre les schémas alimentaires. Dans les conditions de base, un régime végétarien offrait le potentiel de production de GABA le plus élevé pour cette bactérie, suivi de près par un régime riche en protéines et par un régime conçu pour le diabète de type 2. À l’autre bout, un plan cétogène très pauvre en glucides donnait le rendement de GABA de base le plus faible, un régime végan se situant aussi dans la partie basse. Lorsque l’équipe a augmenté artificiellement l’apport de composés individuels, deux grandes classes de nutriments ont systématiquement stimulé la production de GABA : les glucides et les molécules riches en azote, en particulier les acides aminés. Dans les régimes pauvres en glucides, l’ajout de composés similaires aux sucres avait l’effet maximal, suggérant que l’énergie carbonée constituait le facteur limitant. En revanche, dans des régimes riches en glucides tels que végétarien et végan, des acides aminés supplémentaires et des sources d’azote apparentées avaient l’impact le plus fort, indiquant que l’azote devenait alors le goulot d’étranglement.
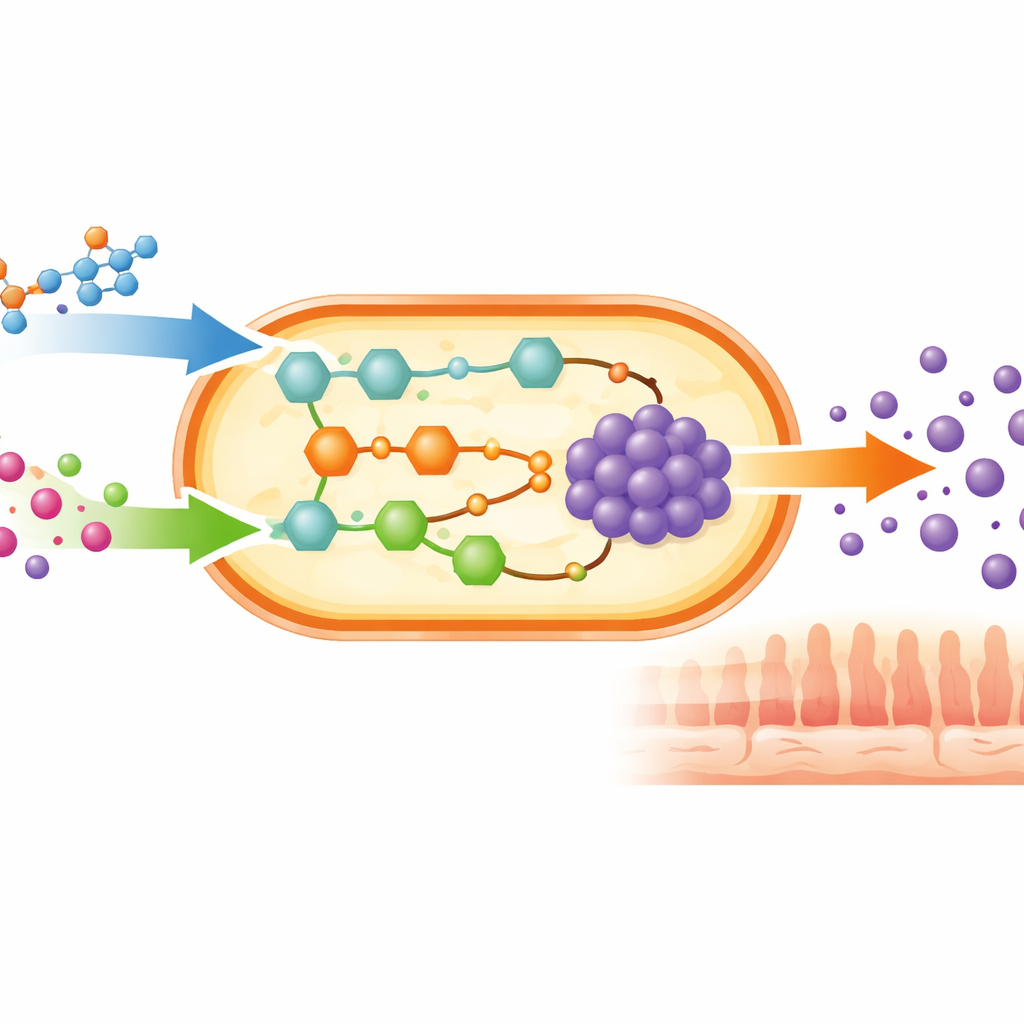
Au‑delà d’une seule bactérie
Pour évaluer comment ces observations pourraient se traduire chez des personnes réelles, les chercheurs ont utilisé des dossiers alimentaires détaillés de plus d’un millier d’adultes de la cohorte de Kiel. Pour chaque individu, ils ont calculé la quantité théorique de GABA que sa population personnelle de B. adolescentis pourrait produire à partir de l’apport nutritionnel déclaré. Une approche d’apprentissage automatique a confirmé que les acides aminés étaient de loin les principaux facteurs alimentaires, suivis d’autres composés contenant de l’azote, de certains sucres, d’acides gras et de vitamines B qui facilitent l’action des enzymes. L’équipe a ensuite étendu sa modélisation aux communautés microbiennes complètes de la même cohorte, en utilisant une vaste bibliothèque de modèles de microbes intestinaux. Ils ont identifié 87 souches bactériennes réparties en 47 genres capables de fabriquer du GABA, comprenant à la fois des résidents « amicaux » et des pathogènes potentiels, ce qui souligne que la production de GABA est une stratégie de survie répandue dans l’écosystème intestinal plutôt qu’un trait limité à quelques microbes « bénéfiques ».
Ce que cela signifie pour la santé et la recherche future
Dans l’ensemble, l’étude montre que la capacité des bactéries intestinales à produire du GABA est très sensible à l’alimentation, et que les nutriments limitants clés dépendent du schéma alimentaire global : des sucres riches en carbone dans les contextes pauvre en glucides et des éléments azotés riches en blocs de construction dans les régimes riches en glucides. Cela ne signifie pas que l’on devrait se ruer sur le sucre ou les protéines pour augmenter le GABA — les régimes riches en sucres, par exemple, sont associés à des risques sanitaires et peuvent aggraver les troubles de l’humeur malgré tout effet microbien. En revanche, ce travail fournit une carte mécaniste des nutriments qui comptent le plus pour la production microbienne de GABA et met en évidence que de nombreuses espèces intestinales, pas seulement les probiotiques classiques, peuvent contribuer à ce composé calmant. Des études expérimentales et cliniques seront nécessaires pour vérifier comment ces observations in silico se traduisent par des changements réels de la fonction intestinale et cérébrale, et si des régimes ou des compléments conçus avec soin peuvent exploiter en toute sécurité la production microbienne de GABA pour soutenir la santé mentale et digestive.
Citation: Homscheid, A., Moors, K.A., Nap, B. et al. Dietary patterns influence the in silico GABA production capacity of Bifidobacterium adolescentis HD17T2H and other human gut bacteria. Sci Rep 16, 8961 (2026). https://doi.org/10.1038/s41598-026-43006-9
Mots-clés: microbiome intestinal, GABA, schémas alimentaires, Bifidobacterium adolescentis, axe intestin‑cerveau