Clear Sky Science · fr
PGE2 régule la ferroptose et l’ostéogenèse des cellules MC3T3-E1 via NOS2
Pourquoi l’alignement des dents affecte vos os
Les appareils et les gouttières transparentes font plus que déplacer les dents : ils sollicitent l’os autour de chaque dent pour qu’il se remodelle. Ce lent chantier biologique explique en partie pourquoi un traitement orthodontique peut durer des années. Cette étude examine l’intérieur des cellules formatrices d’os pour comprendre comment un signal inflammatoire courant, la prostaglandine E2, pourrait à la fois accélérer le mouvement et affaiblir discrètement le nouvel os, ouvrant la voie à des stratégies futures pour rendre les soins orthodontiques plus rapides et plus stables.
Les signaux libérés lorsque les dents sont poussées
Quand un orthodontiste applique une force sur une dent, le ligament et l’os autour de la racine subissent une lésion contrôlée. Les cellules de cette zone libèrent des messagers chimiques, dont la prostaglandine E2, qui aident à coordonner la résorption osseuse d’un côté et la reconstruction de l’autre. Les auteurs se sont concentrés sur les cellules formatrices d’os appelées ostéoblastes, en utilisant une lignée cellulaire murine standard comme modèle. Ils cherchaient à savoir comment la prostaglandine E2 influence deux résultats clés au sein de ces cellules : leur capacité à construire un os minéralisé et leur tendance à subir une forme de mort cellulaire dépendante du fer récemment décrite, la ferroptose.
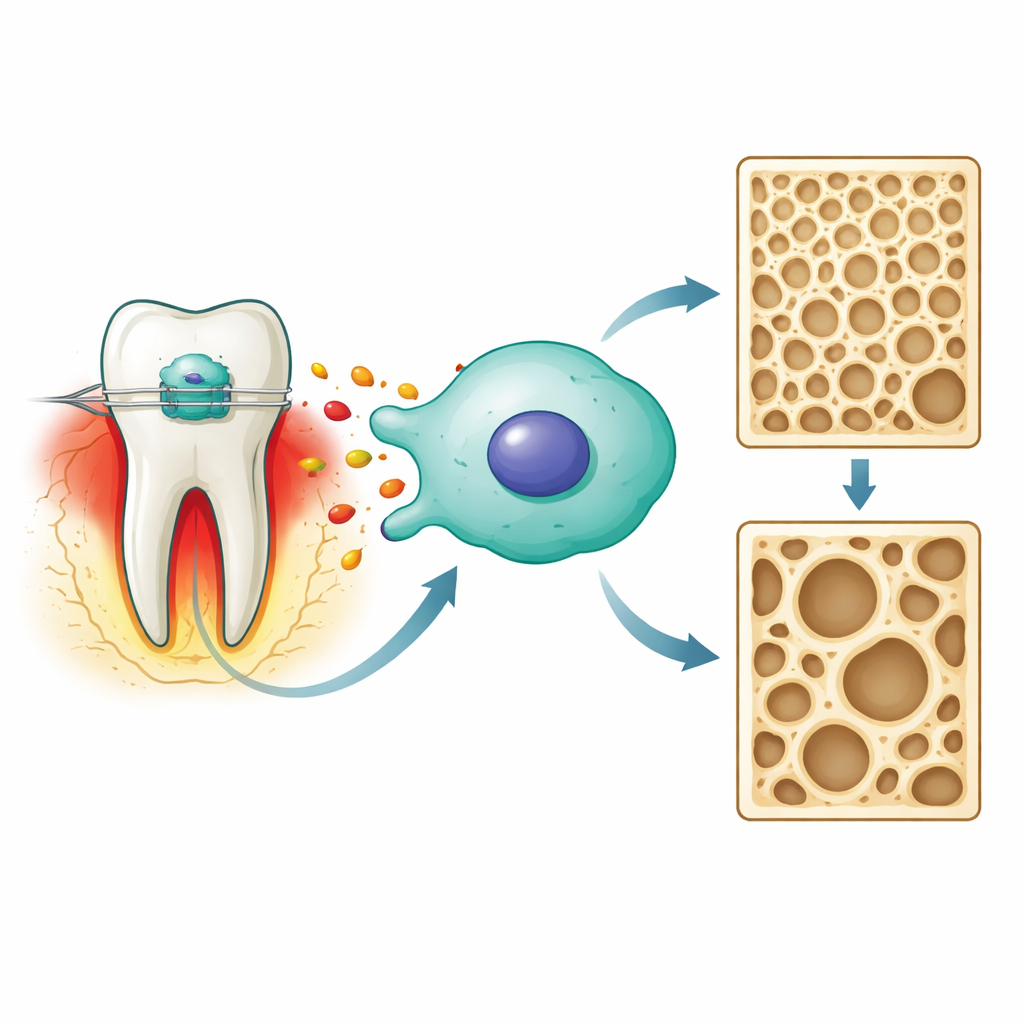
Une voie de stress centrée sur une enzyme unique
En utilisant des données génétiques de rats soumis à un déplacement dentaire, l’équipe a d’abord recherché des molécules liées à la fois à la force orthodontique et à la ferroptose. Un candidat, une enzyme appelée synthase de l’oxyde nitrique 2 (NOS2), est ressorti comme un nœud central. In vitro, exposer des cellules ostéoblastiques à une dose cliniquement pertinente de prostaglandine E2 a créé un état d’inflammation « stérile »—sans germe, uniquement du stress mécanique. Sous ce signal, les niveaux de NOS2 ont augmenté, tout comme d’autres marqueurs de stress et des molécules réactives d’oxygène nocives, tandis que les protéines antioxydantes et celles gérant le fer diminuaient. Ensemble, ces changements sont des signes annonciateurs du déclenchement de la ferroptose à l’intérieur de la cellule.
Quand les constructeurs d’os s’éteignent
Le même traitement par prostaglandine E2 a aussi réduit la capacité des cellules à se comporter comme des ostéoblastes. Les marqueurs classiques de formation osseuse ont baissé, et les tests visualisant les premières minéralisations osseuses ainsi qu’une enzyme clé, la phosphatase alcaline, ont montré une coloration plus faible et moins de dépôt minéral. Lorsque les chercheurs ont ajouté le ferrostatin-1, un médicament connu pour bloquer la ferroptose, une grande partie de ces dommages a été inversée : le stress oxydatif a diminué, les signaux de ferroptose se sont calmés et l’activité ostéogénique a repris. Cela suggère que, du moins dans ce modèle, le signal inflammatoire nuit à la formation osseuse en poussant en partie les cellules vers la ferroptose.
Régler NOS2 comme un interrupteur
Pour déterminer si NOS2 est simplement un spectateur ou un acteur, l’équipe a modulé génétiquement son expression. Réduire NOS2 dans les cellules traitées par prostaglandine a atténué les marqueurs de ferroptose, réduit les dommages oxydatifs et restauré le comportement de formation osseuse à des niveaux proches de la normale. La surexpression de NOS2 a eu l’effet inverse : elle a intensifié le stress et supprimé davantage les caractéristiques de construction osseuse. De manière frappante, augmenter NOS2 à lui seul—sans ajouter de prostaglandine E2—suffisait à déclencher des changements ressemblant à la ferroptose et à réduire l’ostéogenèse. Cela montre que NOS2 ne se contente pas de répondre à l’inflammation ; il peut lui-même pousser les ostéoblastes à s’éloigner de la formation d’un os minéralisé solide.
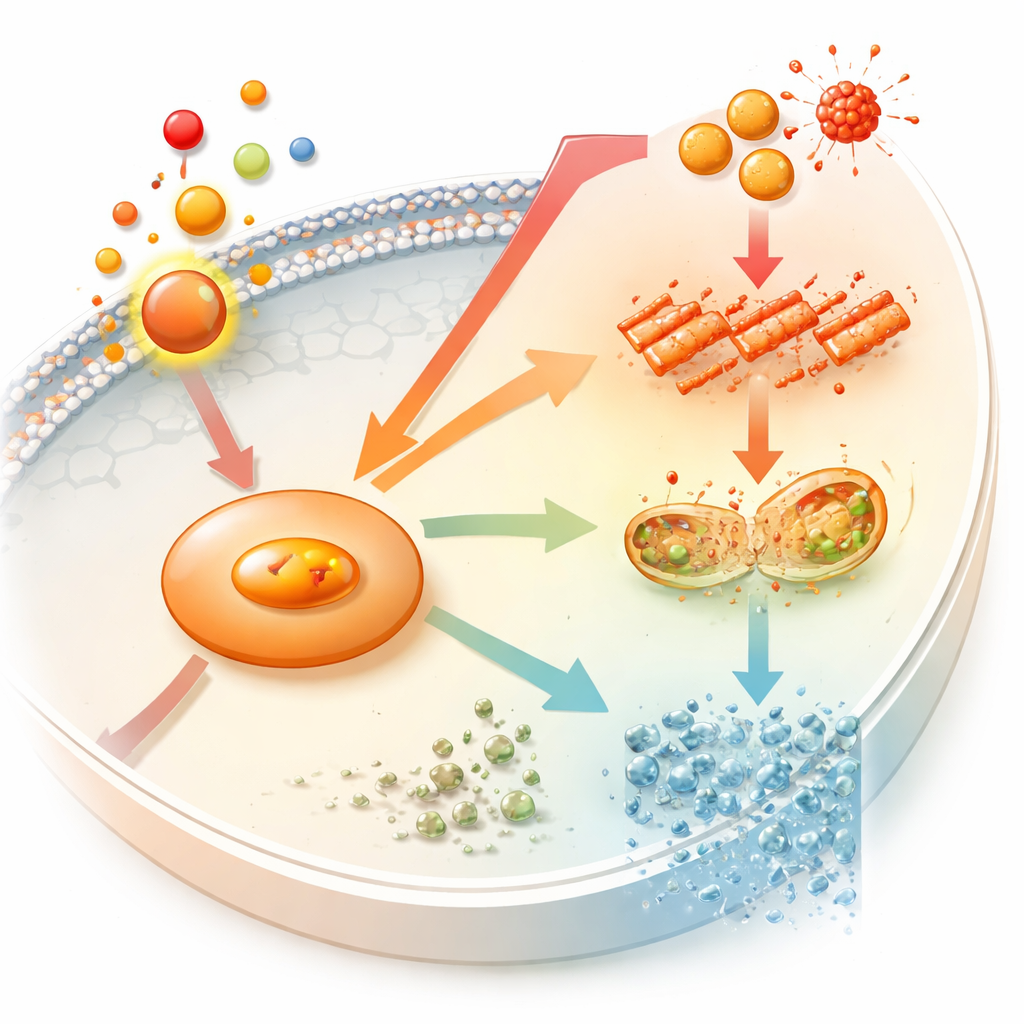
Ce que cela implique pour les futurs appareils orthodontiques
Ensemble, ces expériences dessinent un nouvel axe en biologie osseuse pendant le déplacement dentaire : la prostaglandine E2 élève NOS2, NOS2 alimente les dommages oxydatifs et la ferroptose, et la capacité formatrice d’os décline. Pour les patients, cela ne signifie pas que les appareils sont dangereux, mais explique pourquoi le traitement peut nécessiter un équilibre délicat entre déplacer les dents rapidement et préserver un os solide autour d’elles. À terme, des médicaments ou des matériaux qui ajustent finement l’activité de NOS2 ou protègent les ostéoblastes contre la ferroptose pourraient aider les orthodontistes à raccourcir les temps de traitement tout en maintenant, ou même en améliorant, la qualité et la stabilité de l’os de soutien.
Citation: Sun, M., Yang, Y., Pang, L. et al. PGE2 regulates ferroptosis and osteogenesis of MC3T3-E1 cells via NOS2. Sci Rep 16, 8893 (2026). https://doi.org/10.1038/s41598-026-43001-0
Mots-clés: déplacement orthodontique des dents, remodelage osseux, ferroptose, oxyde nitrique synthase, fonction des ostéoblastes