Clear Sky Science · fr
Explorer le double rôle des vésicules extracellulaires dans la coagulation et la modulation immunitaire du glioblastome
Pourquoi les caillots sanguins comptent dans le cancer du cerveau
Les personnes diagnostiquées d’un glioblastome, la forme la plus agressive de cancer du cerveau, affrontent souvent un danger inattendu : des caillots sanguins dangereux dans les jambes ou le cerveau. Ces caillots peuvent raccourcir la survie et compliquer des traitements déjà exigeants. Cette étude pose une question simple mais cruciale : qu’est‑ce qui, dans les cellules de glioblastome, rend le sang environnant si susceptible de coaguler, et comment de minuscules particules qu’elles libèrent dans le sang remodelent‑elles aussi les défenses immunitaires de l’organisme ?
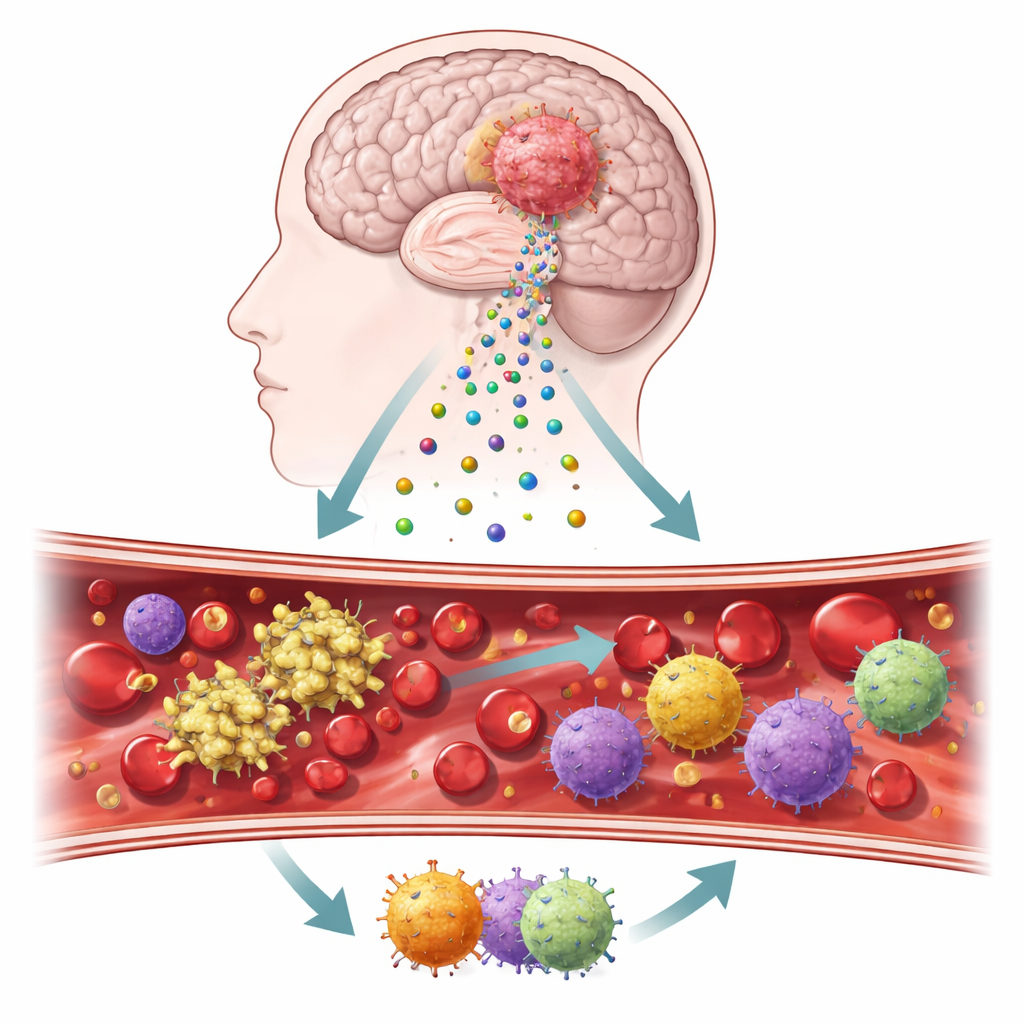
De minuscules messagers quittant une tumeur cérébrale
Les chercheurs se sont concentrés sur de microscopiques bulles appelées vésicules extracellulaires, qui bourgeonnent des cellules tumorales et circulent dans le sang et les tissus cérébraux. Ces vésicules portent à leur surface deux protéines clés, le facteur tissulaire et la podoplanine, connues pour déclencher la formation de caillots et influencer l’inflammation. À partir d’échantillons tumoraux, de sang prélevé lors des interventions et de cultures cellulaires dérivées des tumeurs des patients, l’équipe a mis au point un workflow étape par étape pour suivre le comportement de ces molécules chez de vrais patients et dans des tests de laboratoire contrôlés. Ils ont également comparé le tissu tumoral au cerveau normal pour évaluer l’intensité de ces signaux liés à la coagulation.
Une circulation sanguine discrète mais une zone tumorale prête à coaguler
Les tests hospitaliers standard laissaient entendre qu’avant la chirurgie, le sang de nombreux patients paraissait étonnamment normal : les temps de coagulation habituels et la fermeté des caillots se situaient pour l’essentiel dans les plages de référence. Pourtant, l’examen des tumeurs a révélé un autre paysage. Le tissu de glioblastome montrait de façon constante des niveaux élevés de facteur tissulaire et de podoplanine et des niveaux très faibles d’un frein naturel appelé inhibiteur de la voie du facteur tissulaire. Les lignées cellulaires tumorales dérivées des patients gardaient en grande partie ce profil en culture, confirmant que cette signature « pro‑caillot » est une caractéristique intrinsèque des cellules cancéreuses. Lorsque ces cellules, ou les vésicules qu’elles libéraient, étaient mêlées au plasma en laboratoire, les caillots se formaient plus rapidement, en particulier via la voie dite extrinsèque qui dépend du facteur tissulaire.
Différentes cellules tumorales, différentes stratégies de coagulation
Tous les glioblastomes ne se comportaient pas de la même façon. Certaines lignées cellulaires dérivées de patients présentaient un facteur tissulaire très élevé, d’autres contenaient davantage de podoplanine, et certaines avaient peu de l’un comme de l’autre. Les cellules riches en facteur tissulaire réduisaient le plus fortement le temps de coagulation, tandis que les cellules riches en podoplanine contribuaient de façon plus modeste via des effets sur les plaquettes. Lorsque une telle lignée a été triée en sous‑groupes exprimant uniquement le facteur tissulaire, uniquement la podoplanine, les deux ou aucun des deux, ces profils ne restaient pas stables longtemps. Sur trois semaines, ils ont tendance à revenir vers des profils mixtes, révélant un degré élevé de plasticité. Ce remodelage dynamique s’accompagnait de variations du stress oxydatif dans les cellules, suggérant que le stress chimique présent dans la tumeur peut pousser les cellules vers des états plus pro‑coagulants.
Les vésicules comme façonneuses de l’immunité cérébrale et sanguine
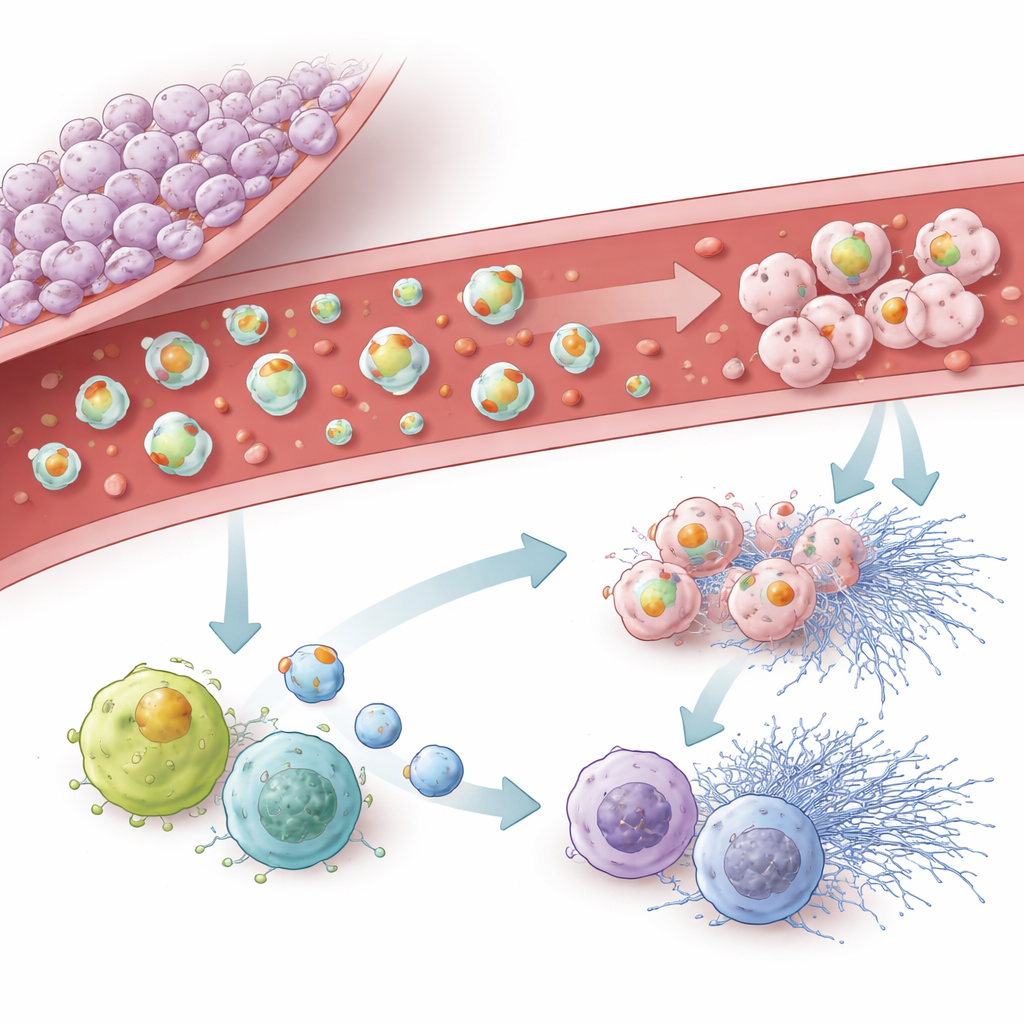
L’équipe a ensuite étudié de près la manière dont les vésicules d’origine tumorale influencent les propres cellules immunitaires du cerveau, appelées microglies, ainsi que les globules blancs circulants et les neutrophiles. Les vésicules issues de lignées tumorales fortement pro‑coagulantes étaient facilement captées par les microglies et ralentissaient leur migration, tout en les orientant vers un état plus inflammatoire de type « M1 » et vers des signes de vieillissement cellulaire. Dans le sang, les vésicules riches en facteur tissulaire activaient les leucocytes, augmentaient la production d’espèces réactives de l’oxygène et favorisaient le relargage de structures collantes en forme de filet par les neutrophiles, connues sous le nom de pièges extracellulaires. Les vésicules porteuses de podoplanine étaient moins puissantes pour déclencher ces réactions immunitaires explosives mais encourageaient fortement un programme de type sénescence, où les cellules immunitaires cessent de se diviser et modifient leur comportement. Même des vésicules dépourvues des deux protéines clés pouvaient encore provoquer une certaine sénescence, ce qui implique que d’autres cargaisons jouent aussi un rôle.
Ce que cela signifie pour les patients et les soins futurs
Au total, les résultats montrent que le glioblastome n’épaissit pas simplement le sang de façon globale. Au contraire, la tumeur et les vésicules qu’elle libère créent une zone localisée et hautement complexe où coagulation et inflammation s’amplifient mutuellement. Le facteur tissulaire apparaît comme le principal moteur de la formation des caillots et de l’activation inflammatoire, tandis que la podoplanine apporte sa propre influence sur les plaquettes, le vieillissement immunitaire et le comportement des microglies. Parce que ces vésicules circulent et reflètent l’état de la tumeur, elles pourraient servir de futurs marqueurs sanguins pour identifier les patients à risque particulièrement élevé de caillots. Elles pourraient aussi orienter des stratégies de prévention plus ciblées visant la machinerie pro‑coagulante de la tumeur sans affiner largement le sang.
Citation: Wolff, A., Waitz, G., Kaps, P. et al. Exploring the dual role of extracellular vesicles in coagulation and immune modulation in glioblastoma. Sci Rep 16, 9534 (2026). https://doi.org/10.1038/s41598-026-42867-4
Mots-clés: glioblastome, caillots sanguins, vésicules extracellulaires, microenvironnement tumoral, réponse immunitaire