Clear Sky Science · fr
Étude clinique et histopathologique multicentrique des lésions du spectre du myxome odontogène par pathologie quantitative
Pourquoi cela compte pour les patients et les dentistes
Au cœur de l’os mandibulaire, des tumeurs rares peuvent croître silencieusement pendant des mois ou des années avant d’être détectées. Ces formations, appelées myxomes et myxofibromes odontogènes, ne sont pas des cancers, mais elles peuvent s’étendre, fragiliser l’os et compliquer la chirurgie. Pendant des décennies, les pathologistes les ont évaluées principalement à l’œil nu, ce qui a entraîné des différences dans la façon dont les hôpitaux décrivent et classent un même type de lésion. Cette étude apporte de puissants outils d’analyse d’images à la lame de microscope, montrant comment l’intelligence artificielle (IA) peut aider les médecins à voir ces tumeurs plus clairement et de manière plus cohérente.
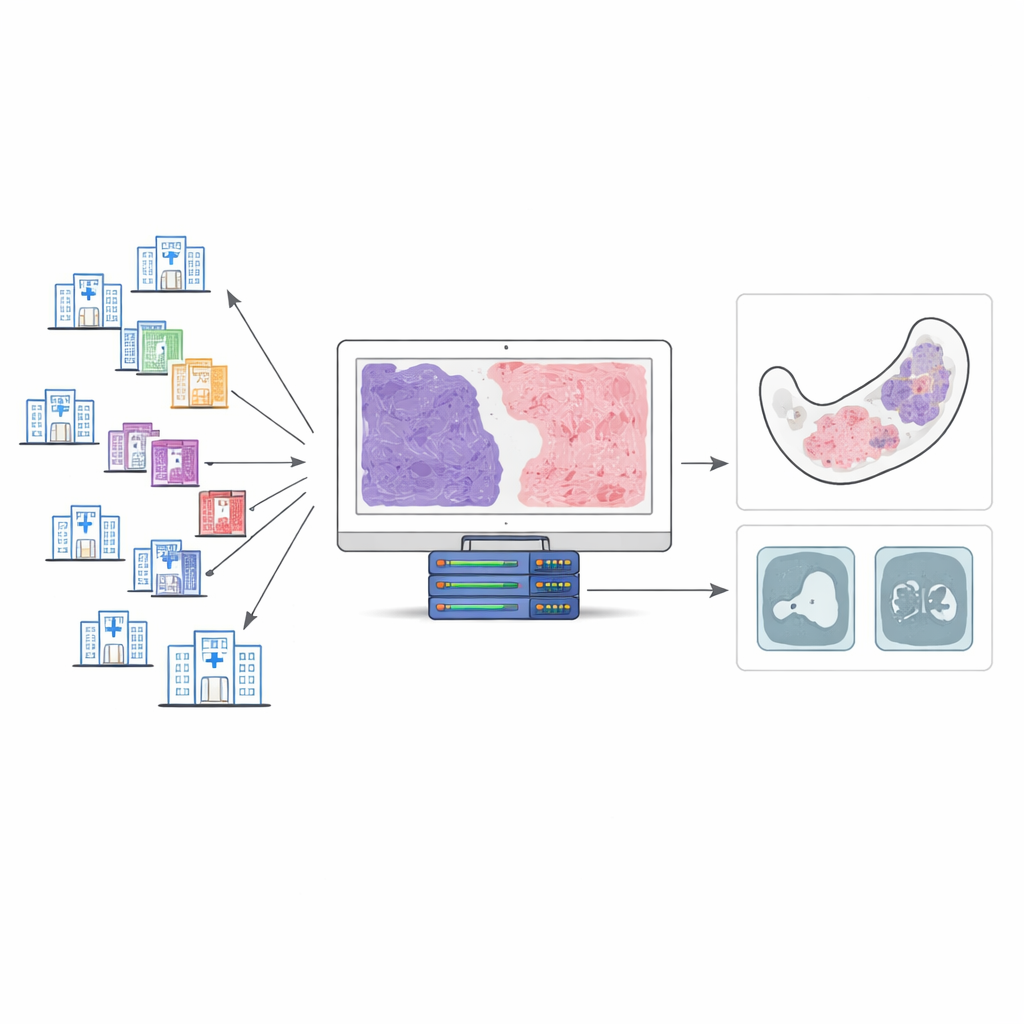
Tumeurs rares de la mâchoire d’apparence trompeuse
Le myxome odontogène et le myxofibrome odontogène proviennent des tissus impliqués dans la formation des dents. Les deux sont des tumeurs molles, à consistance gélatineuse, qui siègent dans l’os de la mâchoire. Au microscope, elles présentent un mélange de zones lâches, myxoïdes, et de bandes fibreuses plus denses. Traditionnellement, les pathologistes ont tenté de les distinguer en estimant la proportion de tissu fibreux par rapport au composant myxoïde. Mais ces tumeurs sont rares, et il n’existe pas de règles universellement acceptées sur la quantité de tissu fibreux nécessaire pour faire basculer le diagnostic d’une étiquette à l’autre. En conséquence, différents hôpitaux peuvent attribuer des noms différents à des lésions très similaires, même lorsque les patients présentent des symptômes et des résultats d’imagerie comparables.
Transformer les lames de microscope en nombres
L’équipe de recherche a rassemblé 143 échantillons tissulaires de patients traités dans 34 hôpitaux sur deux décennies, en se concentrant finalement sur 100 cas répondant à des critères de qualité stricts. Tous les échantillons ont été colorés avec une teinte spéciale (trichrome de Masson) qui colore le tissu fibreux différemment du reste de la tumeur. Deux pathologistes bucco‑dentaires experts ont soigneusement revu chaque cas et estimé le pourcentage de tissu fibreux par paliers de 10 %. Ces estimations d’experts ont servi de référence pour entraîner un système d’IA à effectuer la même tâche automatiquement, mais de façon entièrement quantitative.
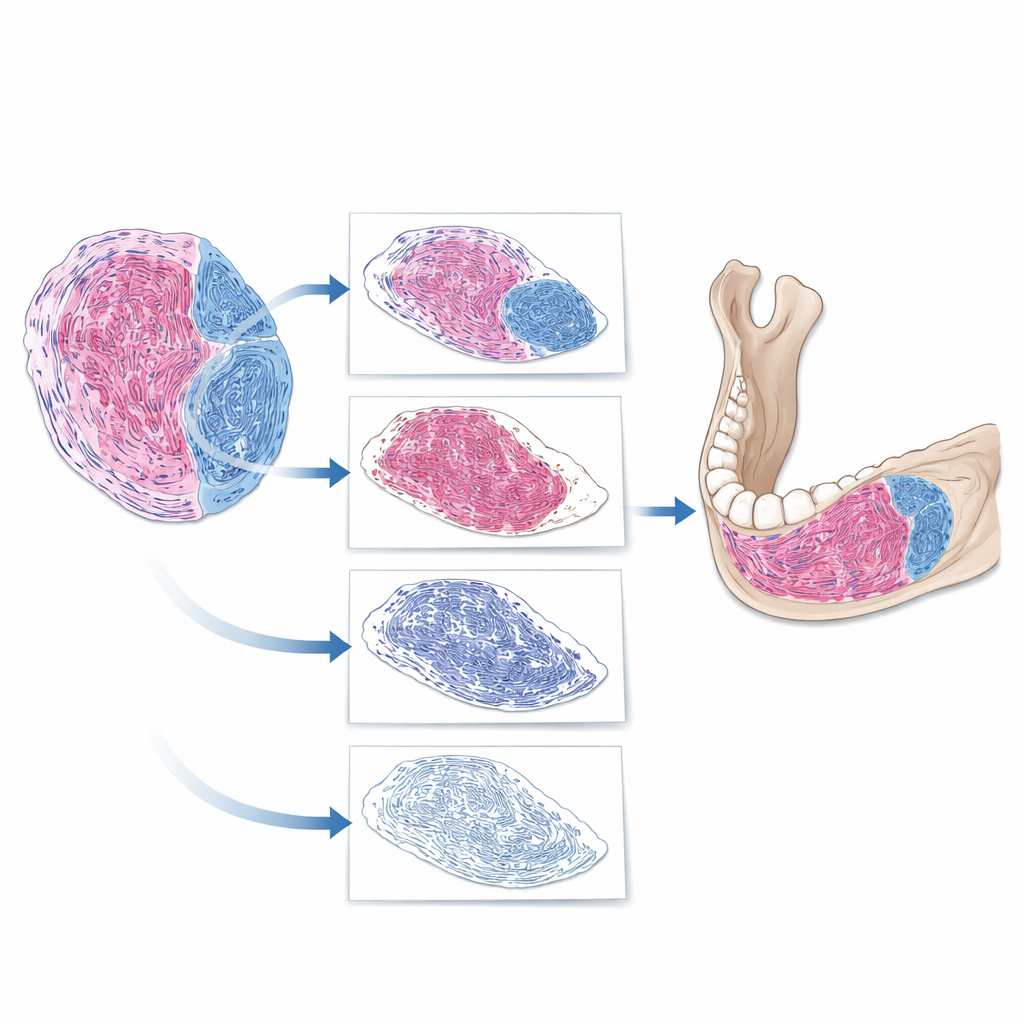
Comment l’IA « lit » une lame tumorale
L’équipe a construit une chaîne de traitement numérique étape par étape pour analyser les images de lames entières. D’abord, le logiciel a séparé le véritable tissu de l’arrière‑plan vide de la lame. Ensuite, il a isolé la tumeur des structures voisines comme l’os et les dents. Enfin, au sein de la tumeur, il a retiré les noyaux cellulaires et s’est concentré sur le matériau restant, identifiant les régions qui avaient pris la coloration fibreuse. À partir de cela, l’IA a calculé une proportion de tissu fibreux : la surface de tissu fibreux divisée par la surface tumorale totale. Lorsque les chercheurs ont comparé les valeurs générées par l’IA avec leurs propres évaluations d’experts, l’accord était solide, avec une divergence d’environ dix points de pourcentage dans la plupart des cas individuels. Cela suggère que l’IA peut reproduire de façon fiable le jugement des experts, tout en l’exprimant par des mesures précises plutôt que par des impressions approximatives.
Ce que la composition fibreuse révèle de l’apparence tumorale
Munis de ces mesures, les chercheurs ont examiné comment la teneur en fibres se rapportait aux caractéristiques cliniques et radiologiques. Ils ont constaté que la quantité de tissu fibreux variait fortement selon les établissements, reflétant des différences dans la manière dont les pathologistes avaient initialement étiqueté les tumeurs. En étudiant les caractéristiques d’imagerie, un schéma s’est détaché : les tumeurs apparaissant comme une cavité unique sur les images (lésions uniloculaires) avaient tendance à présenter une proportion plus élevée de tissu fibreux que celles présentant plusieurs compartiments (lésions multiloculaires). Cela concorde avec l’idée que des tissus plus fibreux et denses peuvent former une masse plus solide et monobloc, tandis que des tissus plus lâches et riches en fluide se fragmentent en plusieurs espaces.
Ce que cela implique pour le diagnostic et la prise en charge futurs
L’étude ne vise pas à renommer les maladies ni à remplacer les pathologistes par des machines. Elle montre plutôt que la pathologie quantitative basée sur l’IA peut fournir une règle de mesure commune pour les tumeurs rares de la mâchoire entre de nombreux hôpitaux. En transformant les textures subtiles du tissu tumoral en nombres reproductibles, cette approche met au jour la part d’appréciation subjective qui pèse sur les diagnostics quotidiens et propose un moyen de réduire cette variabilité. Pour les patients, une interprétation plus cohérente de ces lésions pourrait favoriser des décisions thérapeutiques plus claires et une meilleure comparaison des résultats entre centres. À mesure que des méthodes similaires seront étendues à d’autres tumeurs rares, la microscopie assistée par IA pourrait discrètement remodeler la manière dont les pathologistes voient la maladie — rendant leurs évaluations plus comparables et, en fin de compte, plus utiles, quel que soit le lieu de prise en charge du patient.
Citation: Harazono, Y., Fukawa, Y., Iwasaki, T. et al. Multicenter clinicopathological study of odontogenic myxoma spectrum lesions using quantitative pathology. Sci Rep 16, 11221 (2026). https://doi.org/10.1038/s41598-026-42019-8
Mots-clés: myxome odontogène, tumeurs de la mâchoire, pathologie numérique, intelligence artificielle, proportion de tissu fibreux