Clear Sky Science · fr
Analyse des vésicules extracellulaires dérivées des cellules épithéliales bronchiques par cytométrie en flux conventionnelle, d’imagerie et nanoscale
Pourquoi de minuscules bulles dans les poumons comptent
Nos poumons sont tapissés de cellules qui communiquent en permanence avec le système immunitaire, surtout lorsque nous inhalons poussières, polluants ou microbes. Une grande partie de cette « conversation » se fait via de minuscules bulles appelées vésicules extracellulaires — des colis de lipides et de protéines libérés par les cellules. Ces vésicules peuvent aggraver ou atténuer les maladies pulmonaires, et elles pourraient un jour servir de signaux d’alerte précoces pour des affections telles que l’asthme, la maladie pulmonaire obstructive chronique (MPOC) et la fibrose. Cette étude explore les meilleures façons de mesurer ces particules insaisissables à l’aide de différents types d’instruments laser avancés, en gardant à l’esprit la volonté de rendre ces mesures pratiques pour la recherche et de futures applications cliniques.
Messages invisibles des cellules des voies respiratoires
Les vésicules extracellulaires (VE) sont de petits paquets entourés de membrane libérés par presque toutes les cellules dans des fluides tels que le sang, l’urine et le mince film liquide qui tapisse nos voies respiratoires. Les VE provenant des cellules épithéliales bronchiques humaines — les cellules qui tapissent les conduits respiratoires — sont déjà impliqués dans plusieurs processus pulmonaires : ils peuvent influencer la survenue d’allergies, aider à combattre les infections pulmonaires, modifier la structure des voies respiratoires dans la MPOC et même limiter la formation de cicatrices dans le tissu pulmonaire. Parce qu’ils transportent des fragments de protéines, de lipides et de matériel génétique de leurs cellules d’origine, les VE pourraient agir comme des empreintes de l’état de santé ou de maladie pulmonaire, et pourraient éventuellement être utilisés comme traitements. Le défi réside dans leur taille extrêmement petite, leur grande hétérogénéité et leur faible abondance, ce qui rend leur détection et leur comptage précis difficiles.
Aller au‑delà des tests lents et fragmentés
Traditionnellement, les chercheurs s’appuient sur plusieurs méthodes séparées pour étudier les VE. L’ultracentrifugation ou la chromatographie par exclusion de taille servent à les isoler ; l’analyse par suivi de nanoparticules mesure leur mouvement pour estimer taille et nombre ; et la microscopie électronique fournit des images détaillées. Bien que puissantes, ces approches sont lentes, exigeantes en main d’œuvre et peu adaptées à un usage routinier ou clinique. Surtout, elles sont peu efficaces pour déterminer quelles protéines spécifiques chaque vésicule porte. La cytométrie en flux — technologie largement utilisée pour analyser le sang et les cellules immunitaires — offre une alternative plus rationalisée. Elle fait passer les particules une par une devant des lasers, mesurant leur diffusion lumineuse (liée à la taille) et leur fluorescence (provenant de colorants ou d’anticorps). Les conceptions récentes d’instruments promettent d’étendre la cytométrie en flux à l’échelle des plus petites vésicules, ouvrant la possibilité qu’une seule machine puisse dimensionner, compter et caractériser les VE en un seul passage.
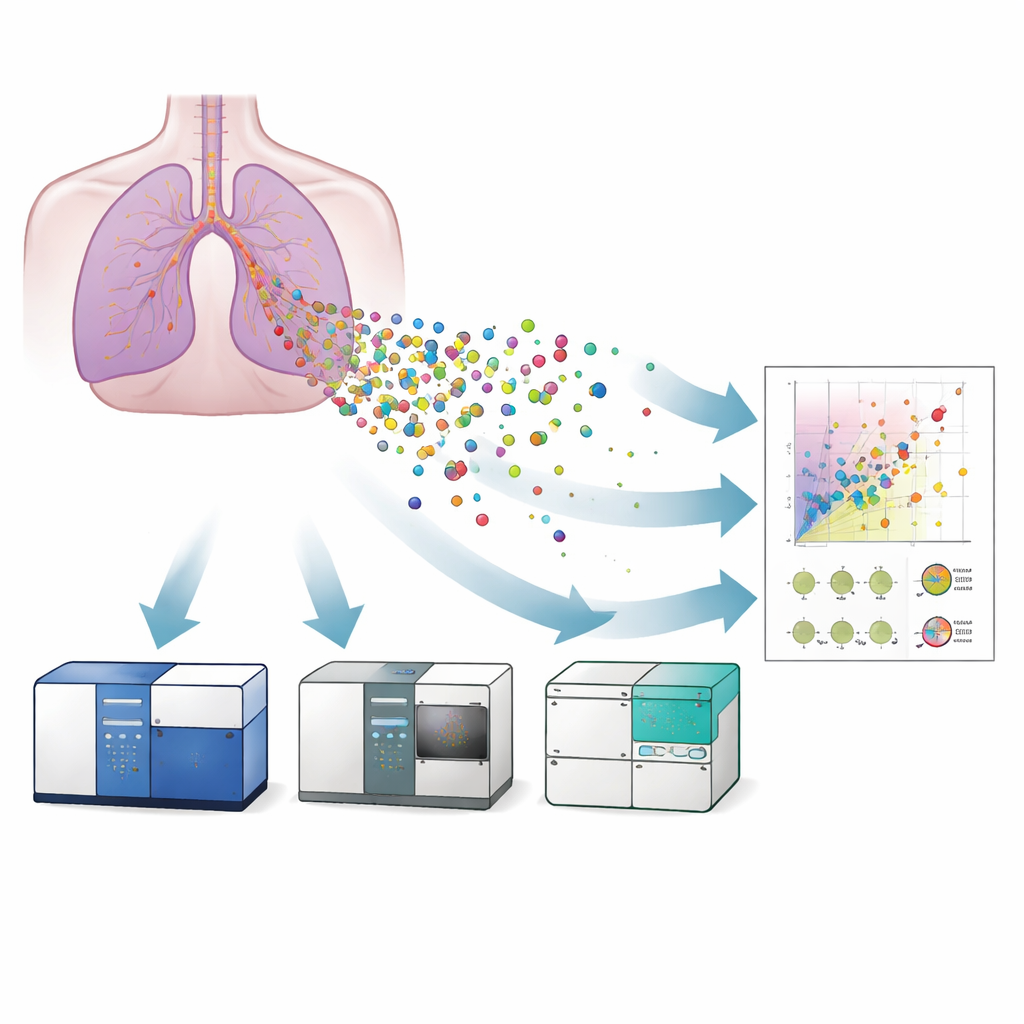
Trois appareils, un objectif
Les chercheurs ont comparé trois variantes de cytométrie en flux pour étudier les VE libérés par un modèle de culture de l’épithélium bronchique humain : un cytomètre en flux conventionnel, un cytomètre en flux d’imagerie et un cytomètre en flux nanoscale. Ils ont d’abord confirmé la présence et l’apparence typique des vésicules par microscopie électronique et microscopie super‑résolutive, qui ont aussi montré que les vésicules portaient des protéines de surface connues sous le nom de tetraspanines (CD9, CD63, CD81) — des marqueurs standards pour identifier les VE. Ils ont ensuite utilisé des billes de référence et des étalons de liposomes soigneusement calibrés pour convertir les signaux lumineux de chaque instrument en tailles approximatives de vésicules. Le cytomètre nanoscale pouvait détecter des vésicules d’environ 40 nanomètres, l’instrument d’imagerie jusqu’à environ 55 nanomètres, tandis que le matériel conventionnel peinait en dessous d’environ 120 nanomètres. En pratique, seuls les systèmes les plus sensibles pouvaient saisir pleinement les plus petites vésicules, potentiellement les plus pertinentes sur le plan médical.
Marquer et compter les vésicules
Pour s’assurer qu’ils mesuraient des vésicules intactes et biologiquement actives plutôt que des débris, l’équipe a utilisé un colorant appelé calcein‑AM. Ce colorant ne s’éclaire qu’une fois qu’il a traversé une membrane intacte et a été traité par des enzymes à l’intérieur de la vésicule. Ils ont ajusté soigneusement la concentration du colorant afin qu’il marque fortement les vésicules tout en minimisant le signal de fond, en choisissant une concentration qui produisait des réponses claires et linéaires sur des dilutions d’échantillons. Le calcein a ensuite été combiné à des anticorps fluorescents qui se lient aux tetraspanines à la surface des vésicules, permettant aux instruments de distinguer les vésicules portant différentes combinaisons de ces marqueurs. Le groupe a aussi évalué la sensibilité de chaque machine à ces étiquettes fluorescentes — c’est‑à‑dire combien de molécules d’anticorps devaient être présentes sur une vésicule avant qu’elle ne soit détectée de manière fiable. La cytométrie en flux d’imagerie offrait généralement des seuils de détection plus faibles que le cytomètre conventionnel, la rendant mieux adaptée aux particules ne portant qu’un petit nombre de protéines marquantes.
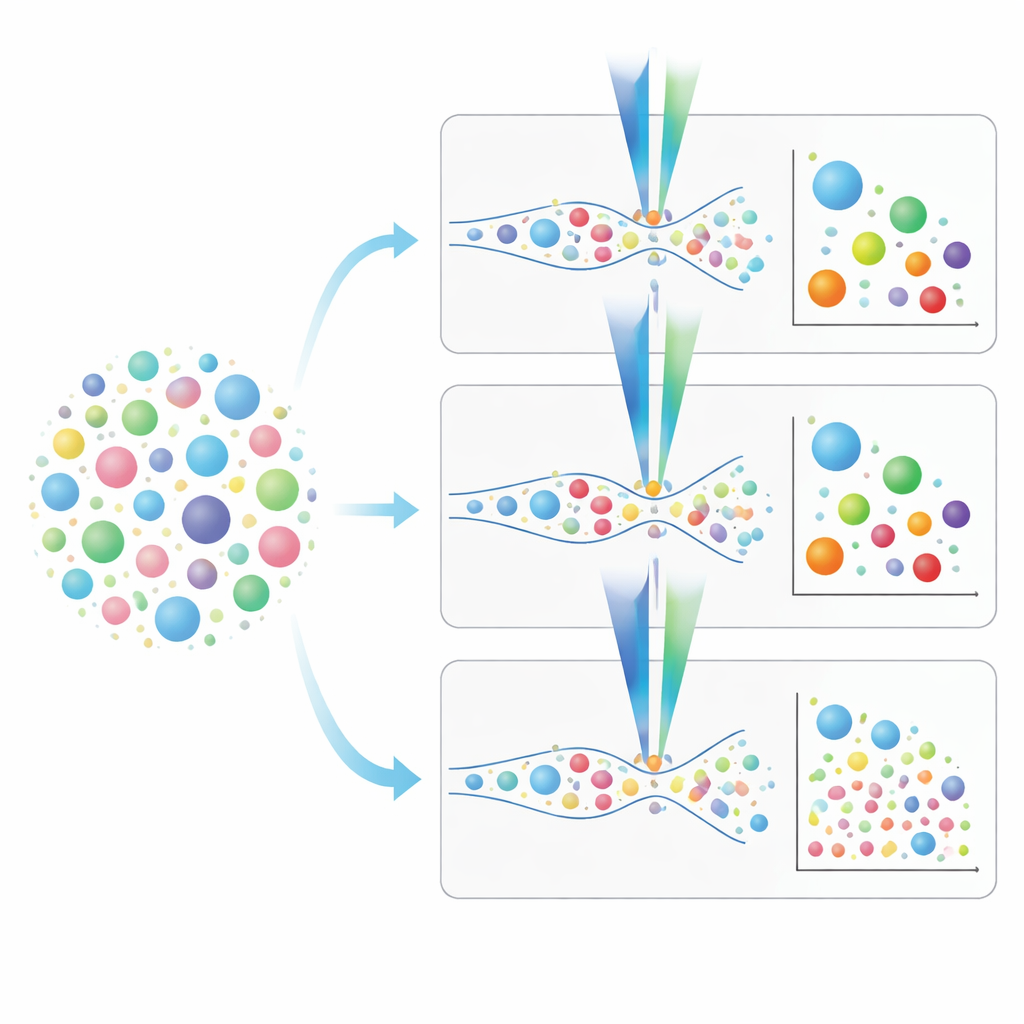
Choisir le bon outil pour les études de vésicules pulmonaires
De cette comparaison directe se dégage un tableau pratique. Les cytomètres en flux conventionnels sont plus rapides et peuvent analyser des échantillons sans isolation préalable, mais ils manquent beaucoup des plus petites vésicules qui peuvent contenir des signaux de maladie cruciaux. Les cytomètres en flux d’imagerie et nanoscale, bien que plus lents et, dans le cas de l’instrument nano, plus dépendants d’un nettoyage préalable des échantillons, peuvent atteindre des tailles beaucoup plus faibles et permettent un « fingerprinting » plus riche des marqueurs de surface. Les auteurs proposent des stratégies pas à pas pour le marquage et l’étalonnage, soulignent l’importance de connaître la limite de détection de chaque étiquette fluorescente et montrent comment éviter des signaux trompeurs venant de colorants qui marquent aussi des fragments ou des particules non‑vésiculaires. En termes simples, ils fournissent une feuille de route pour aider les chercheurs à choisir l’instrument et le protocole adaptés à leurs questions sur les VE pulmonaires, rapprochant le domaine de l’utilisation de ces messagers microscopiques comme outils pratiques pour comprendre, diagnostiquer et, éventuellement, traiter les maladies respiratoires.
Citation: Hopkins, G., Browne, W., Tucis, D. et al. Bronchial epithelial cell-derived extracellular vesicle analysis using conventional, imaging, and nanoscale flow cytometry technologies. Sci Rep 16, 11162 (2026). https://doi.org/10.1038/s41598-026-41848-x
Mots-clés: vésicules extracellulaires, épithélium pulmonaire, cytométrie en flux, maladies respiratoires, analyse de biomarqueurs