Clear Sky Science · fr
Des effets antagonistes des acides aminés soutiennent des nano‑environnements abiotiques dans l’argile
Comment de minuscules poches dans l’argile pourraient nourrir la première chimie de la vie
La vie n’aurait peut‑être pas commencé dans des mers ouvertes, mais à l’intérieur d’espaces inimaginablement petits entre les feuillets de minéraux argileux courants. Cette étude explore comment des molécules simples apparentées aux acides aminés actuels peuvent remodeler l’argile à l’échelle nanométrique, creusant des compartiments douillets qui piègent et organisent la chimie. En montrant comment différents acides aminés renforcent ou perturbent les feuillets d’argile, ce travail suggère un mécanisme naturel par lequel la jeune Terre — ou d’autres mondes rocheux — aurait pu créer de minuscules « laboratoires » favorisant l’assemblage des éléments constitutifs de la vie.
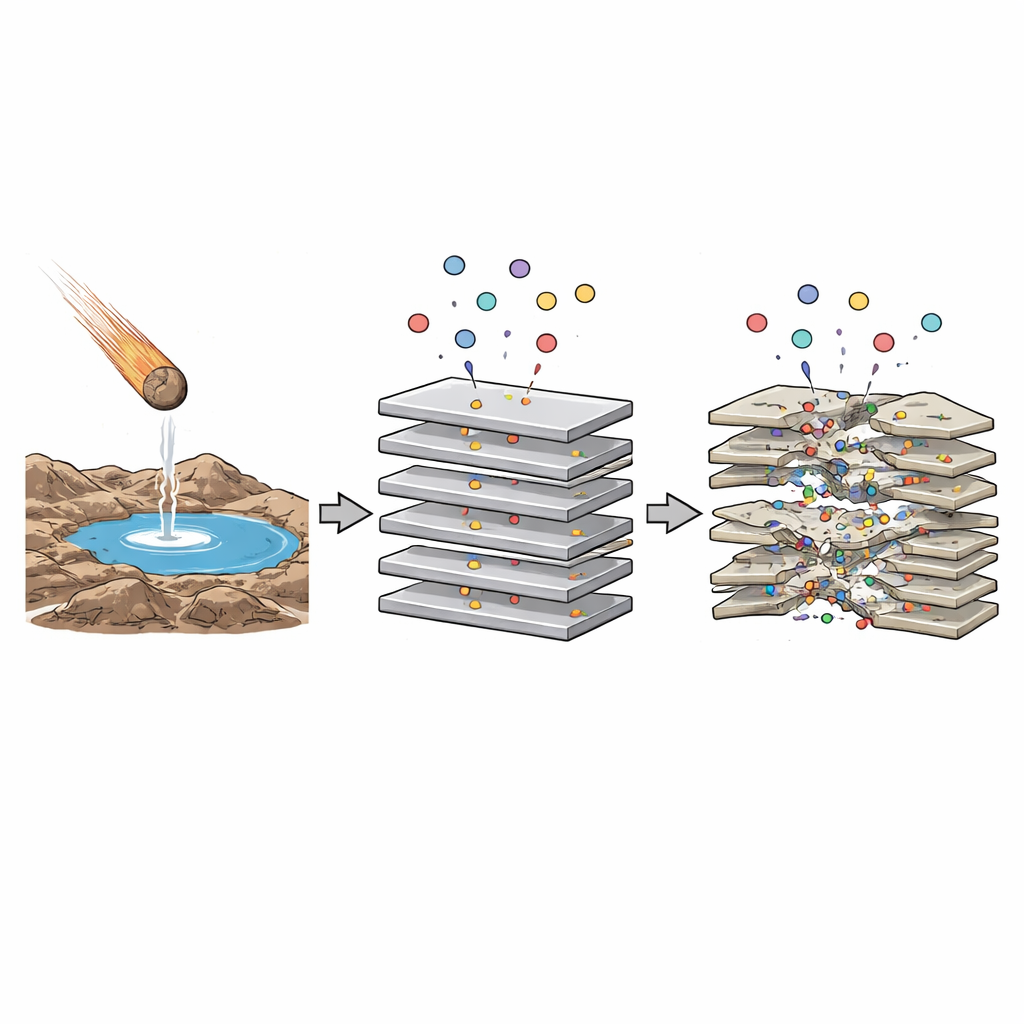
La promesse des espaces cachés
Les scientifiques soupçonnent depuis longtemps que les minéraux faisaient plus que reposer sous les océans et les étangs primordiaux : ils ont peut‑être aidé à assembler les premières chaînes moléculaires. En particulier, des argiles comme la montmorillonite peuvent gonfler et se contracter quand l’eau et de petites molécules s’intercalent entre leurs feuillets empilés. À l’intérieur de ces interstices étroits, l’eau se comporte différemment, les forces électriques sont plus intenses et des réactions difficiles en solution aqueuse ordinaire peuvent devenir plus accessibles. De tels espaces confinés pourraient favoriser la liaison de blocs de construction simples — comme des acides aminés et des nucléotides — en chaînes plus longues, une étape clé vers la vie. Mais les environnements prébiotiques réels étaient des mélanges chimiques complexes contenant de nombreux organiques différents. Cela pose la question : lorsque plusieurs types d’acides aminés interagissent avec l’argile en même temps, s’annulent‑ils mutuellement ou leurs effets concurrents peuvent‑ils en réalité créer des environnements chimiques plus riches ?
Bâtisseurs amicaux et perturbateurs malicieux
Les chercheurs se sont concentrés sur une montmorillonite riche en calcium et sur trois acides aminés. Deux d’entre eux, la lysine et l’arginine, sont des acides aminés standard de construction des protéines bien connus des manuels de biologie. Le troisième, l’acide γ‑aminobutyrique (GABA), n’est pas incorporé dans les protéines modernes mais est fréquent dans les météorites et a donc pu être livré à la jeune Terre. Des travaux antérieurs montraient que la lysine et l’arginine se glissent dans les espaces interfeuillets et se lient fortement, contribuant à maintenir les couches ordonnées et relativement plates. Le GABA, en revanche, adhère à peine — pourtant il a un effet disproportionné : il courbe et partiellement détache les feuillets d’argile, créant des cavités à l’échelle nanométrique. Cette étude s’est intéressée à ce qui se produit lorsqu’une petite quantité d’acide aminé de type protéique est mélangée à un grand excès de GABA de type météoritique, mimant un bassin fortement ensemencé en organiques extraterrestres.
Observer la transformation des feuillets d’argile
Pour suivre ces changements, l’équipe a combiné plusieurs techniques révélant chacune un aspect différent de l’argile. La spectroscopie infrarouge a sondé la vibration des groupes silicium–oxygène du réseau argileux, qui se déplace lorsque les feuillets sont déformés, séparés ou remplis par différentes espèces. La diffraction des rayons X a mesuré l’espacement et l’ordre des feuillets empilés, à la fois sur des échantillons secs et après réhydratation par vapeur d’eau. L’analyse thermogravimétrique a suivi la force de rétention des molécules organiques et de l’eau dans l’argile. Enfin, la microscopie électronique à haute résolution a fourni des images directes des structures en feuillets et des éventuelles cavités entre eux. Ensemble, ces outils ont permis aux auteurs de distinguer les actions stabilisantes de la lysine et de l’arginine de l’influence perturbatrice du GABA, même lorsque tous étaient présents dans un même mélange.
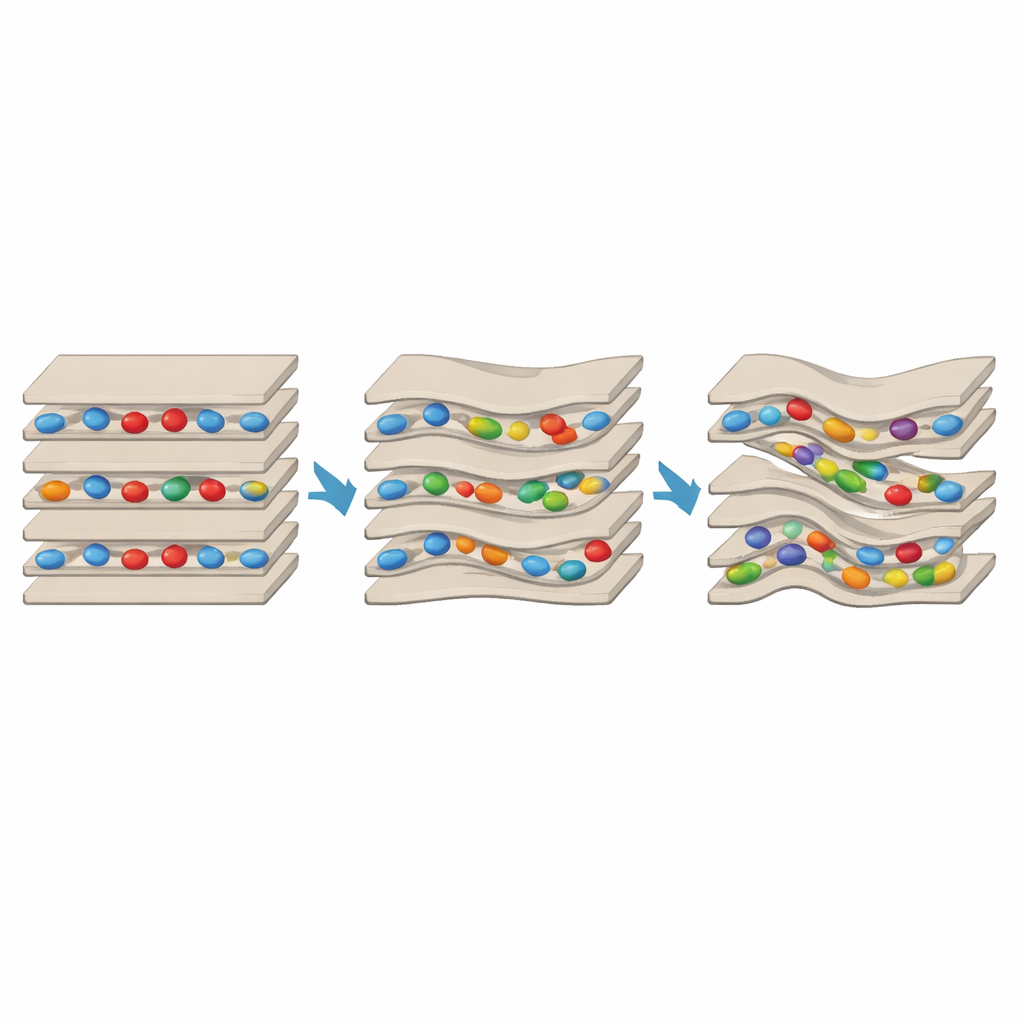
Un yin‑yang nanoscopique dans l’argile
Les résultats révèlent une poussée et une traction saisissantes. Lorsque seule la lysine ou l’arginine était présente, elles s’inséraient dans les espaces interfeuillets, agissant comme des barres transversales qui lient une couche à la suivante. Cela réduisait la capacité de l’argile à gonfler avec l’eau et rendait la structure plus ordonnée et résistante au décollement. Mais lorsque le GABA était ajouté en large excès, il surmontait cet effet stabilisant dans de nombreuses régions. Les signatures spectroscopiques montraient la présence de domaines partiellement exfoliés, et les profils de diffraction X indiquaient plus de désordre et une moindre alignement des couches. La microscopie électronique allait plus loin, révélant des empilements fortement déformés avec des nanocavités nettes intégrées au milieu des feuillets — de petites poches de l’ordre de quelques nanomètres qui n’apparaissaient ni dans le témoin ni dans les échantillons contenant seulement des acides aminés protéiques. Fait important, des régions à feuillets pontés et fermement maintenus coexistaient aux côtés de régions déformées riches en cavités au sein d’un même grain d’argile, démontrant que les deux effets peuvent opérer côte à côte.
Nano‑compartiments naturels pour la chimie primitive
Pour un non‑spécialiste, le message clé est que de simples mélanges d’acides aminés peuvent sculpter l’argile en un patchwork de minuscules compartiments aux propriétés variées. Les acides aminés de construction protéique contribuent à maintenir les feuillets ensemble, tandis que le GABA d’origine météoritique les écarte subtilement et creuse des nanocavités. Ces poches confinées hébergent probablement de l’eau et des molécules dissoutes dans des conditions distinctes de l’environnement alentour, favorisant potentiellement des réactions telles que la formation de polymères, centrales pour l’origine de la vie. Parce que les météorites apportent des acides aminés non protéiques en abondance aux mondes riches en argile, ce « yin‑yang » antagoniste entre molécules stabilisantes et perturbatrices pourrait être un moyen courant pour les planètes rocheuses et les astéroïdes de générer et maintenir des nano‑environnements divers où une biochimie primitive pourrait débuter.
Citation: Bezaly, O.R., King, H.E. & Petrignani, A. Antagonistic effects of amino acids support abiotic nano-environments in clay. Sci Rep 16, 8959 (2026). https://doi.org/10.1038/s41598-026-41502-6
Mots-clés: origines de la vie, chimie prébiotique, minéraux argileux, acides aminés, nanoconfinement