Clear Sky Science · fr
Apprentissage fédéré explicable et sécurisé pour la classification du cancer de la peau respectueuse de la vie privée à l’aide d’un CNN multi‑échelle léger
Pourquoi des contrôles du cancer de la peau plus intelligents comptent
Le cancer de la peau est le cancer le plus fréquent dans le monde, et le dépister tôt peut sauver des vies. Pourtant, un diagnostic précis dépend encore largement d’experts inspectant soigneusement des images de grains de beauté et de taches cutanées. De nombreuses cliniques ne disposent pas de cette expertise, et le partage de vastes collections d’images de patients pour entraîner de meilleurs outils informatiques soulève d’importantes préoccupations en matière de confidentialité. Cette étude présente une nouvelle façon permettant aux hôpitaux de collaborer pour entraîner un système performant de détection du cancer de la peau sans jamais partager les images brutes des patients, tout en fournissant aux médecins des explications visuelles claires de ce que le système perçoit.
Collaborer sans révéler de secrets
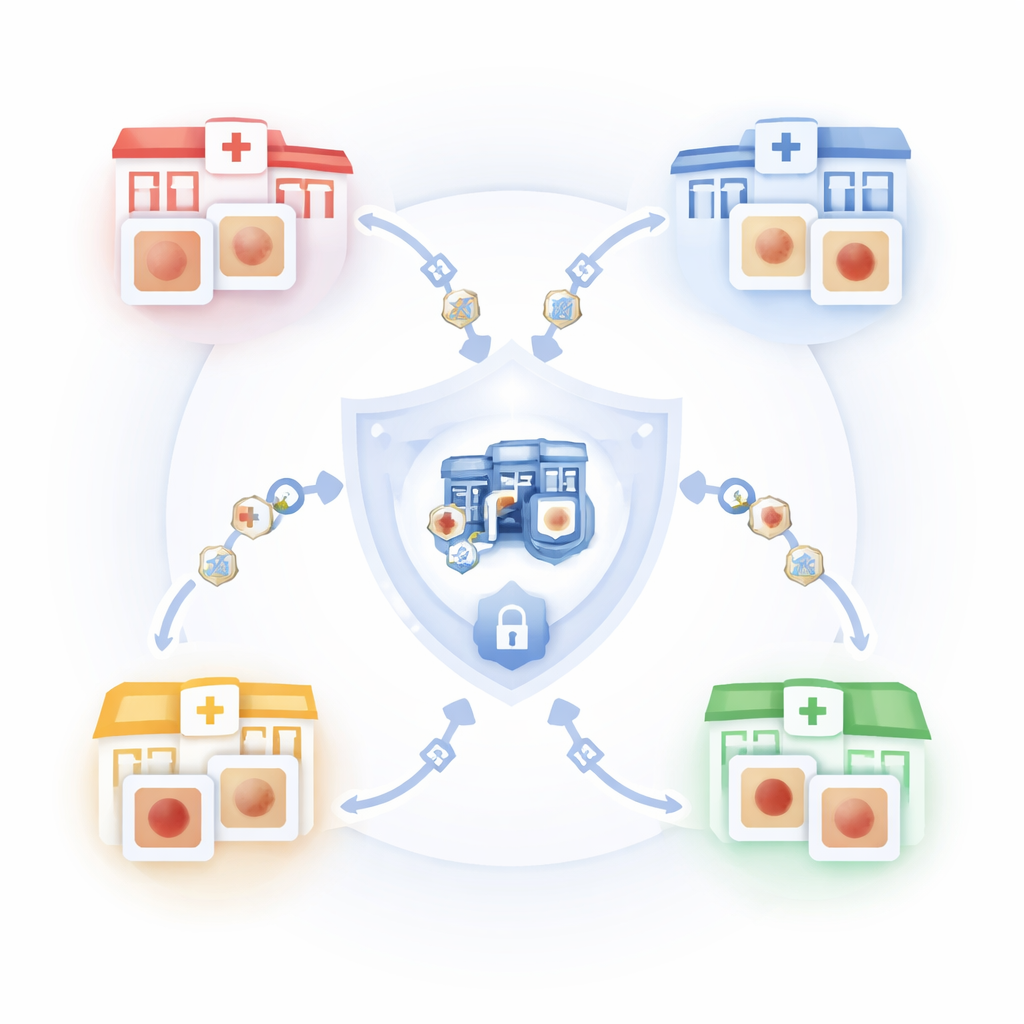
L’idée centrale est une méthode d’entraînement appelée apprentissage fédéré. Plutôt que d’envoyer les images cutanées vers un serveur central, chaque hôpital conserve ses images sur site et entraîne une copie locale du même modèle informatique. Seuls les « savoir‑faire » appris (les mises à jour du modèle) sont envoyés à un serveur central, où ils sont combinés en un meilleur modèle global puis renvoyés à tous les hôpitaux. Dans ce travail, les auteurs simulent plusieurs hôpitaux coopérant de cette manière sur un grand ensemble de données publiques de lésions cutanées, de sorte que le modèle bénéficie de cas divers tout en veillant à ce que les images des patients ne quittent jamais leur institution d’origine.
Un lecteur d’images léger mais perçant
Pour rendre cette collaboration pratique, l’équipe a conçu un nouveau réseau de neurones convolutionnel multi‑échelle léger (LWMS‑CNN). De nombreux modèles d’images populaires sont volumineux et lents à transmettre sur les réseaux hospitaliers ; par contraste, ce modèle utilise moins d’un million de paramètres entraînables, une fraction de ce que requièrent des architectures bien connues. Sa structure traite chaque image cutanée à plusieurs niveaux de détail en parallèle, des bords et textures fins aux motifs plus larges, puis fusionne ces indices. Ce design compact s’est révélé à la fois précis et efficace, surpassant ou égalant des modèles plus lourds comme ResNet et DenseNet sur des mesures standard telles que l’exactitude, la précision et le F1‑score, tout en étant beaucoup plus petit et plus rapide — un atout pour une utilisation sur des serveurs hospitaliers modestes ou même des dispositifs en périphérie.
Renforcer la confidentialité par le chiffrement
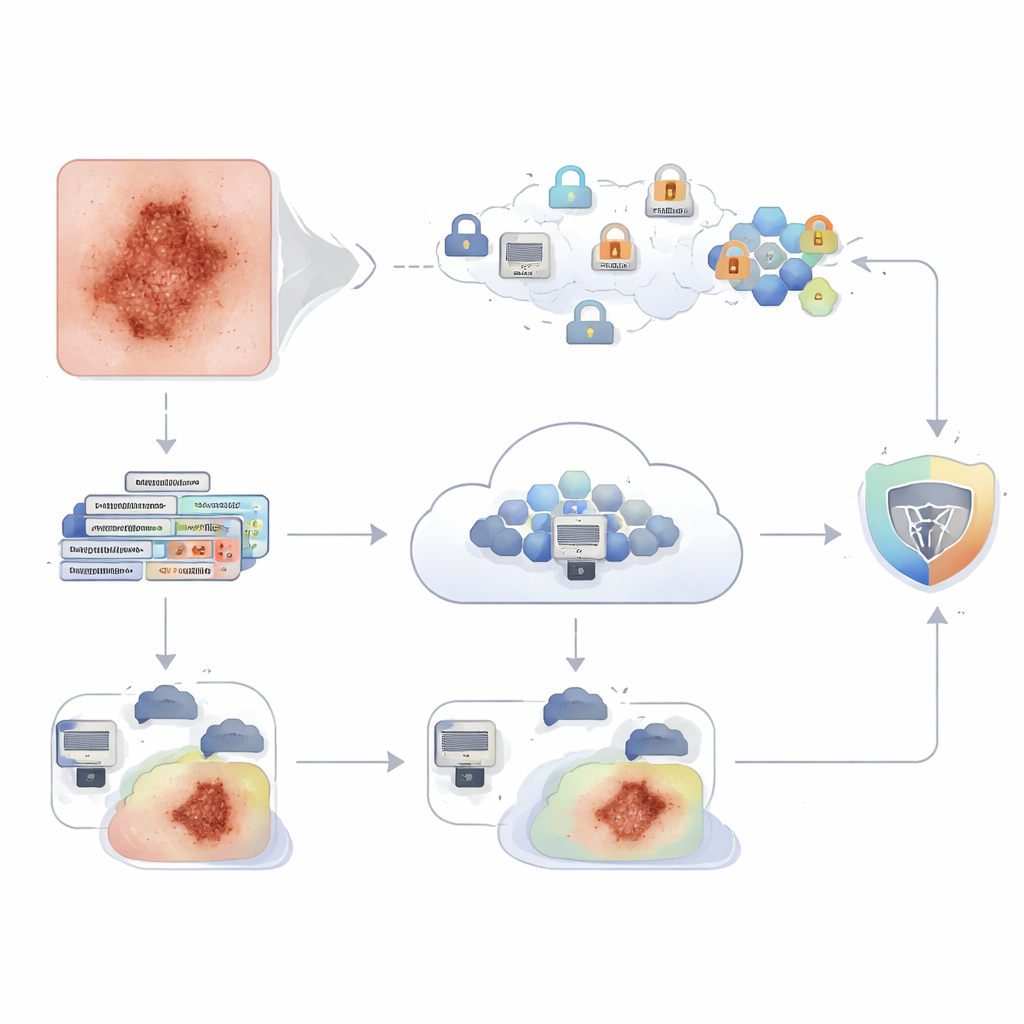
Bien que l’apprentissage fédéré évite l’envoi d’images brutes, les mises à jour de modèle partagées peuvent encore fuir des informations face à des attaques sophistiquées. Pour combler cette lacune, les auteurs enveloppent tout l’échange dans un chiffrement homomorphe, une technique cryptographique qui permet au serveur d’additionner et de moyenniser des mises à jour de modèle alors qu’elles restent chiffrées. Les hôpitaux chiffrent leurs changements de modèle avant de les envoyer ; le serveur ne voit que des nombres brouillés, mais peut tout de même calculer la mise à jour agrégée. Seule une partie de confiance peut déchiffrer le résultat agrégé. Les tests ont montré que l’ajout de cette protection affecte à peine les performances : l’exactitude n’a diminué que d’environ 0,3 point de pourcentage (de 98,62 % à 98,34 %), un faible coût pour une protection de la vie privée et la conformité aux réglementations strictes sur les données médicales.
Ouvrir la boîte noire pour les cliniciens
Une haute exactitude ne suffit pas en médecine ; les cliniciens doivent comprendre pourquoi un algorithme a pris une décision particulière. L’étude ajoute donc des outils d’IA explicable au‑dessus du modèle entraîné. Un outil, SHAP, met en évidence quelles parties d’une image ont le plus influencé une décision, en traitant chaque patch de pixels comme un « joueur » dans un jeu de vote. Un autre, Grad‑CAM, superpose une carte thermique sur la lésion, montrant où le réseau a concentré son attention lorsqu’il a, par exemple, qualifié une tache de maligne ou bénigne. Ensemble, ces vues permettent aux dermatologues de vérifier que le modèle regarde des structures significatives — comme des bords irréguliers ou des variations de couleur — plutôt que des poils, des artefacts d’éclairage ou l’arrière‑plan cutané, et d’examiner les cas incertains ou incorrects.
Des tests en laboratoire aux cliniques du monde réel
Le système fédéré chiffré LWMS‑CNN a été entraîné et évalué sur l’ensemble de données de lésions cutanées HAM10000, puis testé sur deux collections supplémentaires, ISIC 2019 et PAD‑UFES‑20, qui diffèrent par les appareils photo, les types de lésions et les populations de patients. Il a obtenu des précisions élevées sur les trois ensembles, ce qui suggère que l’approche se généralise bien au‑delà d’une seule source de données. Les auteurs ont également exploré des scénarios plus difficiles et réalistes où différents « hôpitaux » voient des mélanges de cas différents, et ont comparé plusieurs manières de combiner les mises à jour de modèle ; la méthode standard FedAvg s’est révélée la plus efficace. Bien que les expériences aient été menées dans une configuration multi‑client simulée plutôt que sur des hôpitaux physiquement séparés, les résultats montrent qu’un modèle compact, un entraînement préservant la vie privée et des explications visuelles claires peuvent être combinés au sein d’un même cadre. Pour les patients, cela ouvre la voie à des contrôles du cancer de la peau plus précis, plus largement accessibles et plus respectueux de la vie privée, tout en maintenant les médecins au cœur du processus.
Citation: Sayeed, A.S.M., Birahim, S.A., Ullah, M.S. et al. Explainable and secure federated learning for privacy-enhancing skin cancer classification using a lightweight multi-scale CNN. Sci Rep 16, 11414 (2026). https://doi.org/10.1038/s41598-026-41360-2
Mots-clés: détection du cancer de la peau, apprentissage fédéré, confidentialité des données médicales, IA explicable, chiffrement homomorphe