Clear Sky Science · fr
Apparition d’un nouveau virus grippal aviaire A(H5N2) hautement pathogène réassortant associé à une pneumonie sévère chez un jeune adulte
Pourquoi ce nouveau cas de grippe aviaire compte
La plupart du temps, la grippe aviaire reste un sujet pour les agriculteurs et les spécialistes de la faune, pas pour le grand public. Cet article décrit la première infection humaine connue par une nouvelle variété de virus de la grippe aviaire appelée H5N2, capable de provoquer des maladies graves chez les oiseaux et, dans ce cas, une pneumonie sévère chez une jeune femme au Mexique. Comprendre comment ce virus est apparu, comment il a affecté la patiente et comment il pourrait se propager aide les cliniciens et les responsables de santé publique à repérer les menaces futures avant qu’elles n’engendrent des épidémies plus larges.
Une maladie rare et grave chez une personne
L’histoire commence à la fin de 2025, lorsqu’une jeune adulte s’est présentée dans un hôpital respiratoire de Mexico après plus d’une semaine de fièvre, maux de gorge, toux, essoufflement et hémoptysie. Elle était obèse mais ne souffrait pas de maladies chroniques majeures et n’avait pas de contact rapproché confirmé avec des volailles, des pigeons ou d’autres animaux. À l’admission, son taux d’oxygène était dangereusement bas, et les scanners pulmonaires montraient des zones trouble et en patchs ainsi que des signes de saignement dans les deux poumons, compatibles avec une pneumonie sévère endommageant les alvéoles responsables des échanges respiratoires.
À la recherche d’un virus inhabituel
Les premiers tests de laboratoire ont montré que la patiente était infectée par un virus influenza A, la grande famille qui inclut la grippe saisonnière et aviaire. Cependant, les tests standards n’ont pas permis de l’identifier comme un sous-type saisonnier connu, ce qui a suscité l’inquiétude qu’il s’agisse d’un variant inhabituel. Des analyses plus spécialisées sur un prélèvement profond des poumons ont confirmé qu’il appartenait à la famille H5 des virus aviaires. La patiente a été placée sous mesures de contrôle des infections et traitée par l’antiviral oseltamivir et oxygénothérapie. Au cours des jours suivants, elle s’est améliorée régulièrement et a finalement été sortie sans complications, tandis que les autorités sanitaires ont commencé à enquêter sur la source de l’infection.
Comment différentes grippes aviaires se sont recombinées en quelque chose de nouveau
Pour comprendre exactement de quoi il s’agissait, les chercheurs ont séquencé le matériel génétique complet du virus prélevé chez la patiente. Les virus grippaux portent leurs gènes en huit segments séparés, qui peuvent être échangés lorsque deux virus différents infectent le même oiseau ou animal. L’analyse a montré que le virus de cette patiente était une mosaïque génétique : certains segments correspondaient à des virus H5N1 hautement pathogènes circulant largement chez les oiseaux sauvages et provoquant de fortes épizooties chez les volailles en Amérique du Nord, tandis que d’autres segments correspondaient à un virus H5N2 de moindre virulence présent depuis des décennies dans les volailles mexicaines. Ce mélange, appelé réassortiment, avait produit une nouvelle version d’H5N2 comportant des caractéristiques des deux virus parentaux.
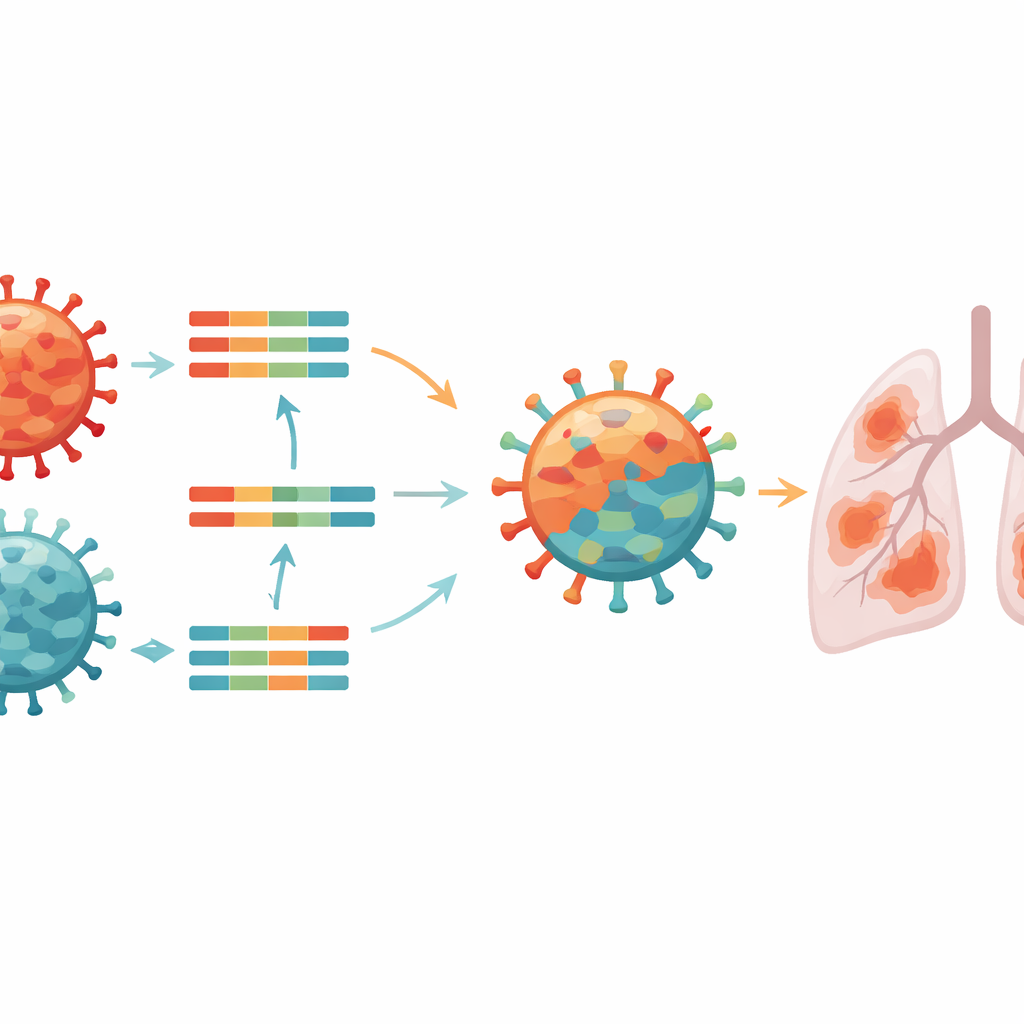
Indices génétiques sur le risque pour les humains et les animaux
En comparant les gènes du virus à des milliers d’autres prélèvements de grippe aviaire d’Amérique du Nord et du Mexique, l’équipe a pu le situer dans des arbres phylogénétiques détaillés et l’affecter à un profil génétique jusque-là non observé, qu’ils ont provisoirement nommé B3.14. Ils ont également recherché des changements spécifiques susceptibles d’améliorer l’infection des mammifères ou la résistance aux médicaments. Le virus conservait une signature moléculaire typique des souches aviaires hautement létales et n’exhibait pas de mutations connues pour neutraliser les antiviraux courants. Toutefois, il portait plusieurs altérations associées, dans d’autres études, à une meilleure réplication dans des cellules de mammifères et à des modifications de la fixation aux récepteurs des voies respiratoires, ce qui laisse craindre qu’il soit quelque peu mieux adapté à infecter l’homme ou d’autres mammifères que des souches antérieures.
Ce que ce cas isolé nous apprend sur les menaces futures
Malgré la gravité de la maladie chez la femme, le suivi de plus de 40 contacts humains proches n’a révélé aucune infection supplémentaire et aucun signe de transmission interhumaine. Des prélèvements effectués sur une poule, deux pigeons et un chien au domicile de la patiente ont mis en évidence des virus H5 apparentés, soulignant que la source probable était la circulation continue de souches mixtes de grippe aviaire chez les animaux locaux plutôt que la transmission entre personnes. Les auteurs concluent qu’il s’agit de la première infection humaine documentée par un virus H5N2 hautement pathogène de cette nouvelle composition génétique et d’un signal d’alerte sur la rapidité avec laquelle les virus aviaires et animaux peuvent mélanger leurs gènes et franchir les barrières d’espèce. Ils soutiennent que la surveillance génétique continue chez les oiseaux sauvages, les volailles et les mammifères — ainsi qu’un diagnostic et un traitement rapides chez l’humain — est essentielle pour repérer tôt ces nouveaux agents dangereux et orienter le développement de vaccins et de stratégies antivirales avant qu’ils n’aient l’occasion de se propager plus largement.
Citation: Vázquez-Pérez, J.A., Becerril-Vargas, E., Ramírez‐González, J.E. et al. Emergence of a novel reassorted high pathogenicity avian influenza A(H5N2) virus associated with severe pneumonia in a young adult. Sci Rep 16, 8841 (2026). https://doi.org/10.1038/s41598-026-41122-0
Mots-clés: grippe aviaire, H5N2, virus réassortant, pneumonie, infection zoonotique