Clear Sky Science · fr
Normalisation des colorations en histopathologie : évaluation des méthodes sur un jeu de données multicentrique
Des images tissulaires plus nettes pour les médecins et les ordinateurs
Lorsque les pathologistes examinent des prélèvements au microscope, ils s’appuient sur des nuances subtiles de rose et de violet pour déterminer si les cellules sont saines ou cancéreuses. Aujourd’hui, ces couleurs peuvent beaucoup varier d’un laboratoire à l’autre, ce qui complique non seulement le diagnostic humain mais perturbe aussi les outils d’intelligence artificielle entraînés sur ces images. Cette étude visait à quantifier l’ampleur de ce problème de couleur et à tester quelles techniques informatiques rendent les images de lames plus homogènes sans perdre d’informations importantes.
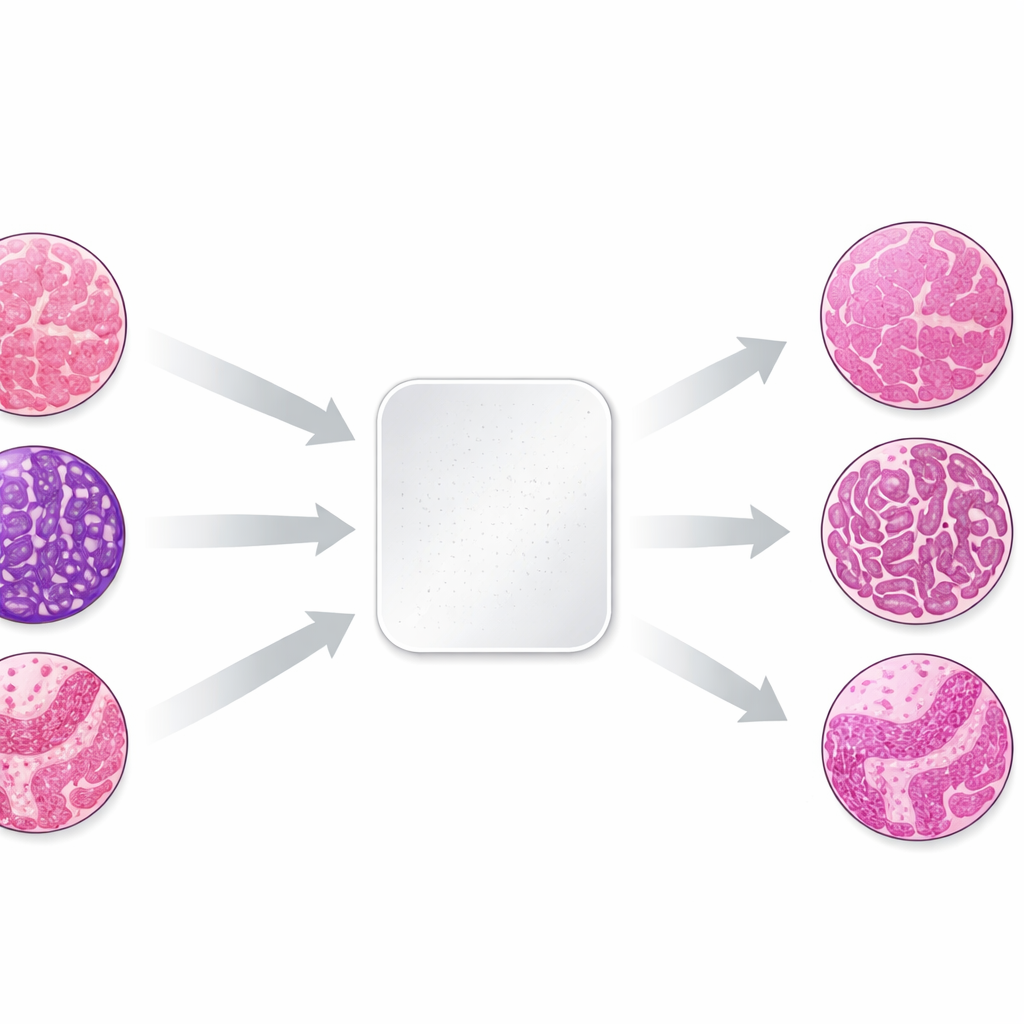
Pourquoi la couleur varie selon les laboratoires
Le travail porte sur la paire de colorants la plus courante en pathologie, l’hématoxyline et l’éosine, qui colorent les noyaux cellulaires en bleu‑violet et les tissus environnants en rose. De petites différences dans la fixation, le traitement et la coloration des tissus, ainsi que dans la numérisation des lames, peuvent modifier ces teintes de façon importante. Pour étudier cet effet de manière contrôlée, les auteurs ont prélevé trois petits échantillons de tissu — peau, rein et côlon — issus des mêmes blocs donneurs et ont envoyé des coupes non colorées identiques à 66 laboratoires dans 11 pays. Chaque laboratoire a appliqué sa procédure de coloration habituelle, puis les lames terminées ont été numérisées. Comme le matériel biologique était presque identique, toute différence d’apparence reflétait principalement la façon dont chaque laboratoire avait coloré et numérisé le tissu.
Construire un banc d’essai unique pour la correction des couleurs
La collection d’images obtenue montrait une variation frappante : des lames provenant du même bloc pouvaient aller du très pâle à presque noir, ou glisser d’une teinte froide à une teinte très chaude. L’équipe a d’abord quantifié ces différences en mesurant les niveaux moyens de rouge et de bleu de chaque lame. Ils ont ensuite choisi pour chaque type de tissu une lame de référence bien équilibrée et ont appliqué huit méthodes différentes de normalisation des colorations à toutes les autres. Quatre méthodes étaient des approches traditionnelles, basées sur des opérations mathématiques ajustant des statistiques colorimétriques globales ou séparant et redimensionnant les composantes de coloration. Quatre autres reposaient sur des approches « génératives » modernes, qui apprennent à transformer des images d’un style colorimétrique à un autre via des réseaux neuronaux.
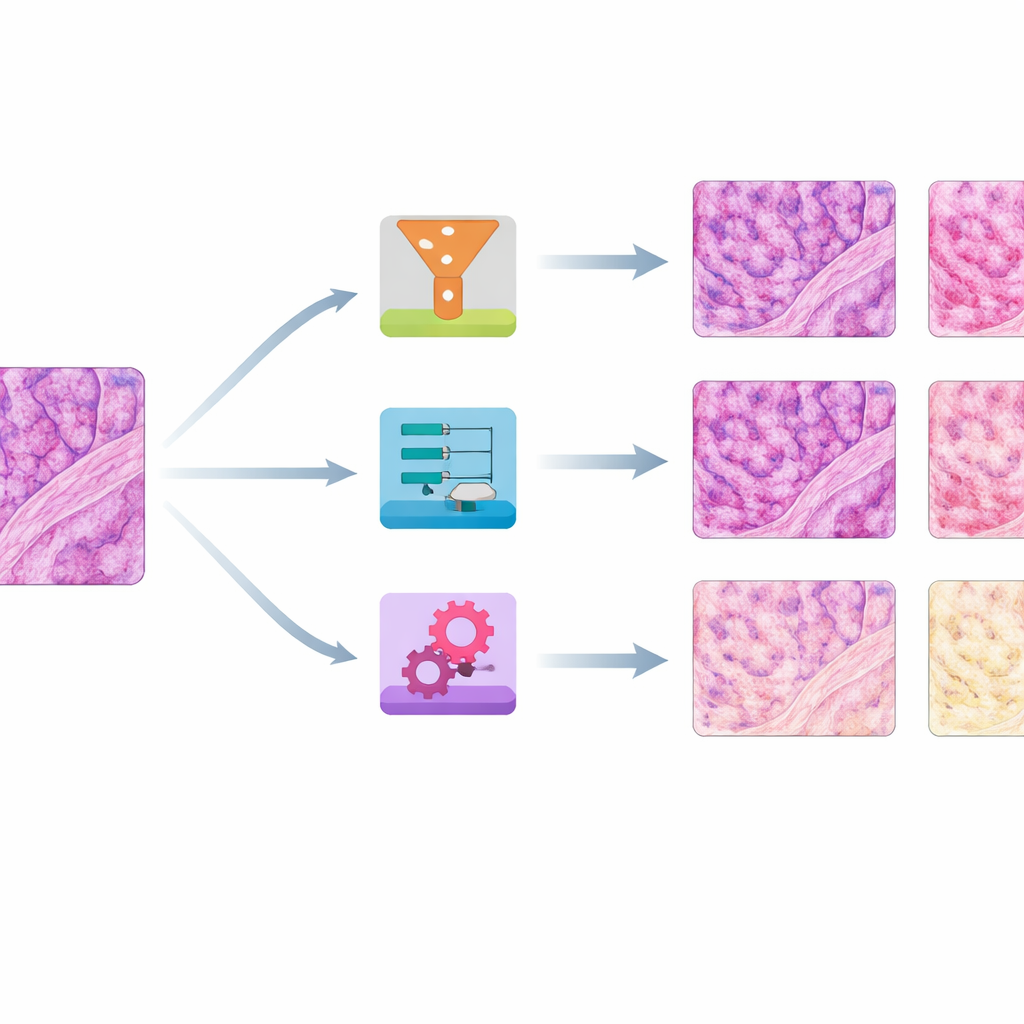
Quelles méthodes ont le mieux préservé la couleur et la structure
Pour évaluer les performances, les auteurs se sont posé deux questions principales : dans quelle mesure les images corrigées approchaient‑elles les couleurs de la référence, et dans quelle mesure conservaient‑elles la structure tissulaire fine ? Ils ont utilisé plusieurs scores numériques comparant les distributions de couleur, une mesure de similarité d’image de haut niveau empruntée à la vision par ordinateur, et un indice structurel sensible au floutage ou aux distorsions. Sur peau, rein et côlon, une méthode simple appelée « histogram matching » — consistant essentiellement à remodeler la distribution de couleurs de chaque lame pour imiter la référence — a produit de façon constante la correspondance colorimétrique la plus proche tout en préservant globalement les structures. Une autre approche classique, la normalisation de Reinhard, a souvent obtenu des résultats presque équivalents. Une troisième méthode, Vahadane, a excellé pour préserver la structure mais avait tendance à tirer tout vers des tons rosés et à atténuer la coloration bleue des noyaux.
Comment les images étaient perçues par des experts humains et des outils d’IA
Des pathologistes expérimentés ont examiné des lames de côlon normalisées pour évaluer l’impact des méthodes sur l’interprétabilité en pratique. Ils ont vérifié si les couches et types cellulaires importants restaient faciles à distinguer, si les lames originellement trop ou insuffisamment colorées étaient améliorées, et si des artefacts numériques étranges apparaissaient. Aucune méthode n’a résolu tous les problèmes, mais l’histogram matching a généralement donné des couleurs homogènes proches de la référence sans artefacts évidents, notamment sur des échantillons fortement surcolorés. Certaines méthodes basées sur l’IA, en particulier des versions de CycleGAN et Pix2pix, ont produit des résultats visuellement réalistes mais ont parfois introduit de subtiles structures artificielles ou des anomalies de couleur dans des cellules sanguines et des zones de fond. L’équipe a aussi montré que la normalisation modifiait le comptage de noyaux par un algorithme de détection de cellules de pointe et la représentation des lames par un grand modèle « fondation », soulignant que la correction des couleurs peut influencer fortement le comportement des systèmes d’IA en aval.
Ce que cela implique pour le diagnostic numérique futur
Dans l’ensemble, l’étude révèle que les différences de couleur entre laboratoires sont suffisamment importantes pour affecter tant les lecteurs humains que les systèmes automatisés, et que rendre les images plus uniformes est une étape importante vers une pathologie numérique fiable et partageable. De façon surprenante, sur ce jeu de données soigneusement contrôlé et au contenu tissulaire très similaire, des méthodes globales simples comme l’histogram matching ont souvent surpassé des techniques d’apprentissage profond plus complexes, lesquelles nécessitent bien plus de données d’entraînement qu’une seule lame par laboratoire. Les auteurs publient ouvertement leur jeu de données à 66 centres afin que d’autres puissent évaluer de nouvelles méthodes et mieux concevoir des données d’entraînement reflétant la variation réelle. Pour les patients, les progrès dans ce domaine pourraient se traduire par des systèmes d’IA mieux transférables d’un hôpital à l’autre, offrant des diagnostics plus cohérents, quel que soit le lieu de traitement d’une biopsie.
Citation: Khan, U., Härkönen, J., Friman, M. et al. Staining normalization in histopathology: Method benchmarking using multicenter dataset. Sci Rep 16, 11097 (2026). https://doi.org/10.1038/s41598-026-40943-3
Mots-clés: pathologie numérique, normalisation des colorations, imagerie histologique, IA médicale, variation de couleur