Clear Sky Science · fr
Classification pan‑cancer des lames congelées par un vision transformer à mélange souple d'experts sous supervision faible
Pourquoi cela compte au bloc opératoire
Quand les chirurgiens enlèvent une tumeur suspecte, ils n'ont souvent que quelques minutes pour savoir si tout le cancer a été retiré. Les pathologistes s’efforcent d’examiner une tranche de tissu rapidement congelée et de donner une réponse pendant que le patient est encore sur la table. Ce processus sous haute pression peut être perturbé par des lames floues, des tumeurs subtiles et des contraintes de temps. L'étude décrite ici explore comment un système d'intelligence artificielle (IA) peut aider les pathologistes à distinguer rapidement et de façon fiable le tissu inoffensif du tissu dangereux dans de nombreux organes différents, en utilisant des équipements réalistes pour les hôpitaux de tous les jours.
Un test rapide avec des défis intégrés
L'analyse en coupe congelée est un pilier de la chirurgie moderne : un mince morceau de tissu est congelé, coupé, coloré et observé au microscope pour juger s'il est bénin ou malin et si la marge chirurgicale est nette. Contrairement aux lames permanentes de laboratoire, les coupes congelées présentent souvent des fissures, des plis et des colorations inégales. Différents pathologistes peuvent diverger sur des cas limites, et le temps presse. Ces problèmes sont particulièrement aigus dans les hôpitaux de plus petite taille ou très occupés, où seuls quelques spécialistes doivent couvrir de nombreux types de cancer. Les auteurs soutiennent qu'un assistant informatisé robuste pourrait rendre les décisions sur les coupes congelées plus cohérentes, plus rapides et plus largement disponibles.
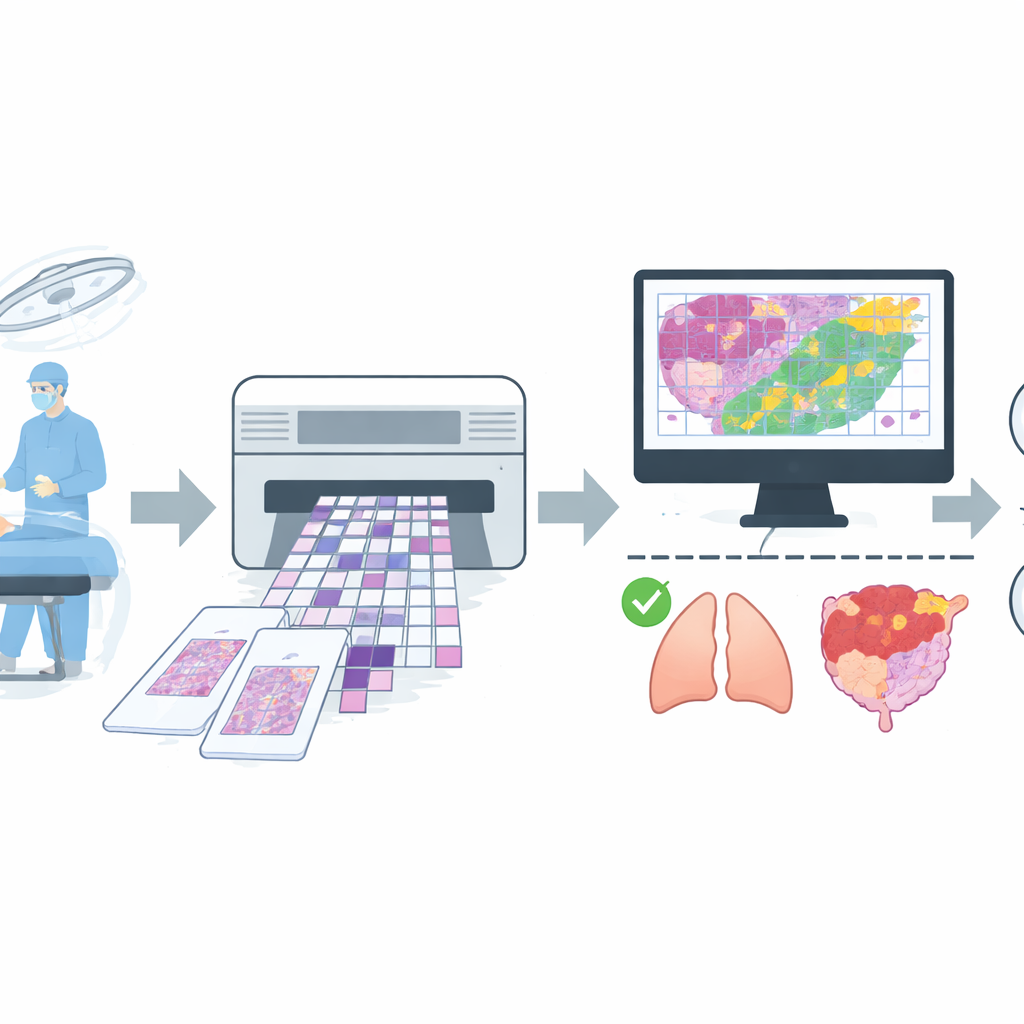
Constituer un jeu d'images large et représentatif du monde réel
Pour entraîner un tel assistant, l'équipe a rassemblé une grande collection d'images numériques issues d'interventions de routine dans un grand hôpital. Ils ont réunis 4 754 lames numériques de tissus congelés provenant de plus de 2 600 patients, puis appliqué des règles de qualité strictes pour éliminer les lames avec des artefacts sévères ou des diagnostics incertains. Le jeu de données final contenait 4 667 lames, chacune étiquetée simplement comme bénigne ou maligne sur la base de l'accord entre la lecture rapide sur lame congelée et le rapport ultérieur plus soigné de la coupe permanente. Les lames couvraient des sites fréquents tels que le poumon, le sein, la thyroïde, les ganglions lymphatiques et les organes reproducteurs féminins, plus un groupe mixte d'emplacements moins fréquents comme l'estomac, le foie et la peau. Les données ont été séparées en groupes distincts pour l'entraînement, l'affinage et les tests finaux, en veillant à ce que les images d'un même patient n'apparaissent jamais dans plus d'un groupe.
Comment l'IA apprend à partir d'indices faibles
Les chercheurs ont construit leur modèle sur une classe de réseaux neuronaux appelée Vision Transformer, qui excelle à repérer des motifs sur de grandes images. Chaque image tissulaire gigantesque a été automatiquement découpée en de nombreux petits carreaux et patchs afin de pouvoir être traitée sur du matériel graphique standard. Une innovation clé a été de remplacer une partie du réseau par un « mélange souple d'experts », un ensemble de nombreuses branches spécialisées de petite taille, chacune focalisée sur différents motifs visuels. Plutôt que d'activer ou désactiver des experts, le système mélange en douceur leurs contributions, ce qui stabilise l'entraînement et optimise l'utilisation de données limitées. Comme les pathologistes n'avaient pas dessiné le contour des tumeurs, le modèle devait apprendre avec une supervision faible : il ne savait que si une lame entière était bénigne ou maligne. Une stratégie d'apprentissage par instances multiples a mis en avant les patchs les plus suspects au sein d'une lame maligne pour servir d'exemples positifs, permettant au réseau de se concentrer progressivement sur les régions les plus informatives.
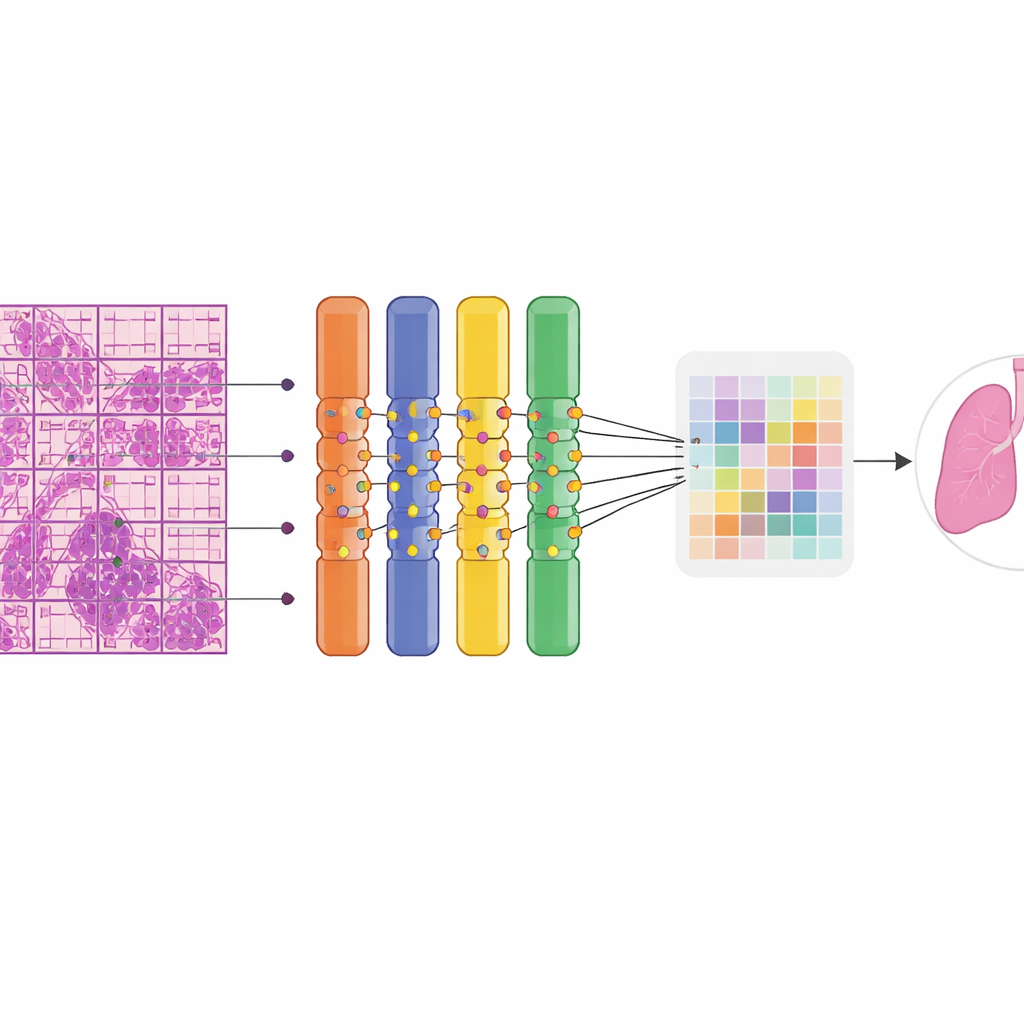
Quelle est l'efficacité du système en pratique
Testé sur 669 lames inédites, l'IA a distingué le tissu bénin du tissu malin avec une grande précision. Elle a correctement classé environ 90 % des cas au total et a montré une excellente capacité à séparer les deux groupes selon les seuils de probabilité. La sensibilité, la probabilité de signaler une lame réellement maligne, était d'environ quatre cas sur cinq, tandis que la spécificité, la probabilité d'identifier à bon escient une lame bénigne comme telle, était encore plus élevée. Fait important, les performances sont restées solides selon les organes : le système a détecté parfaitement tous les cas malins du poumon et du sein présents dans l'ensemble de test et a bien performé sur des groupes plus rares comme les tumeurs annexielles féminines et les organes « autres » mixtes. Des cartes de chaleur colorées superposées aux lames ont révélé que l'attention du modèle se concentrait sur des régions que les pathologistes experts reconnaissaient comme tumorales, y compris des foyers métastatiques dans les ganglions lymphatiques, tout en ignorant largement les structures normales. Le système fonctionnait efficacement, nécessitant moins de 5 Go de mémoire, ce qui le rend adapté à l'utilisation sur des cartes graphiques couramment disponibles plutôt que sur des grappes coûteuses.
Limites, erreurs et pistes d'amélioration
Les auteurs ont aussi étudié les situations où l'IA échouait. Les faux négatifs impliquaient souvent des cellules cancéreuses extrêmement rares, des zones de numérisation floues ou une forte inflammation masquant des foyers malins. Les faux positifs survenaient plutôt dans des conditions bénignes mimant le cancer au microscope, comme des proliférations réactionnelles ou des tissus congelés déformés. Parce que les flux de travail chirurgicaux de routine n'incluent pas de contours détaillés des régions tumorales, l'équipe n'a pas pu quantifier exactement dans quelle mesure les cartes de chaleur correspondaient aux annotations d'experts, se fiant plutôt à une revue qualitative. Certains types d'organes, comme la langue ou certaines tumeurs des tissus mous, restaient sous‑représentés, ce qui suggère que des collections plus larges et multicentriques seront nécessaires pour étendre la portée du système.
Ce que cela pourrait signifier pour les patients et les hôpitaux
Dans l'ensemble, l'étude montre qu'un système d'IA soigneusement conçu peut assister de manière précise et interprétable une tâche centrale de la pathologie chirurgicale : décider, en temps réel, si un tissu est bénin ou malin sur de nombreux types d'organes. En opérant uniquement avec des étiquettes au niveau de la lame, en tournant sur du matériel largement disponible et en mettant en évidence les zones suspectes pour révision humaine, le modèle offre une voie pratique vers des décisions sur coupes congelées plus cohérentes. Pour les patients, cela pourrait se traduire par des interventions mieux informées en une seule opération ; pour les hôpitaux, en particulier ceux qui disposent de peu d'experts, cela ouvre la voie à un futur où des outils numériques avancés contribuent à fournir des soins oncologiques de haute qualité de manière plus équitable.
Citation: Wu, J., Yang, M., Li, J. et al. Pan-cancer frozen section classification using a soft mixture of experts vision transformer under weak supervision. Sci Rep 16, 10297 (2026). https://doi.org/10.1038/s41598-026-40924-6
Mots-clés: lame congelée, pathologie numérique, diagnostic du cancer, vision transformer, apprentissage faiblement supervisé