Clear Sky Science · fr
Mise en œuvre d’un test de biopsie liquide couvrant 1 021 gènes pour le profilage génomique tumoral en pratique oncologique réelle
Pourquoi un test sanguin pour le cancer est important
La plupart des gens savent que les médecins doivent souvent prélever un morceau de tumeur pour comprendre le cancer d’un patient. Mais cette biopsie traditionnelle est invasive, peut être douloureuse et peut ne pas refléter l’ensemble d’une maladie qui s’est déjà propagée. Cette étude explore une autre approche : utiliser un simple prélèvement sanguin pour rechercher des altérations génétiques sur plus d’un millier de gènes liés au cancer. En montrant l’efficacité de ce large test sanguin dans des consultations oncologiques courantes, les auteurs mettent en avant un avenir où les choix thérapeutiques, le suivi et même l’évaluation du risque héréditaire pourraient être guidés par un tube de sang plutôt que par un scalpel.
De l’aiguille dans la tumeur à l’aiguille dans la veine
Le cancer libère de minuscules fragments de son ADN dans le sang lorsque les cellules tumorales meurent et se désagrègent. Ces fragments, appelés ADN tumoral circulant, sont mélangés à l’ADN normal des cellules saines. L’équipe a étudié 1 110 personnes atteintes de cancers métastatiques (avancés) de différents types, notamment du poumon, du sein, colorectal, du pancréas, de la prostate, de l’ovaire et d’autres. Ils ont utilisé un test étendu lisant 1 021 gènes à partir d’un échantillon sanguin et, lorsque disponible, ont comparé ces résultats sanguins à l’ADN provenant du tissu tumoral du patient. Ils ont également séquencé les globules blancs prélevés lors du même prélèvement sanguin pour distinguer les véritables signaux tumoraux des modifications liées à l’âge dans les cellules hématopoïétiques. 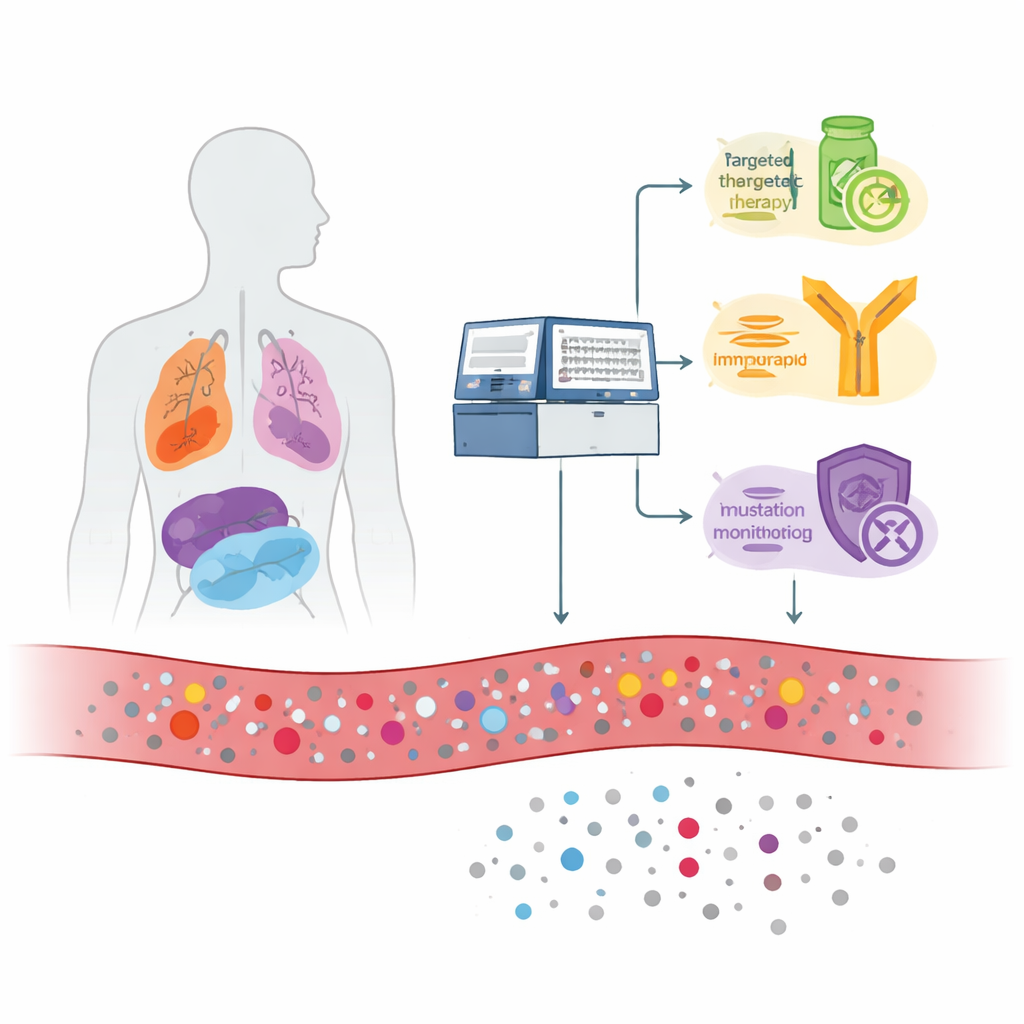
Ce que le sang a révélé sur les tumeurs
Le test sanguin a détecté des altérations d’ADN liées au cancer chez environ les deux tiers des patients. Beaucoup de ces altérations pointaient directement vers des opportunités thérapeutiques. Chez environ 16 % des patients, le test a identifié des cibles « on‑label » — des mutations associées à des médicaments déjà approuvés pour ce type de cancer spécifique, comme certaines altérations d’EGFR dans le cancer du poumon ou PIK3CA et ESR1 dans le cancer du sein. Lorsque les auteurs ont également compté les cibles « off‑label » (mutations avec des médicaments approuvés pour d’autres cancers), les altérations étudiées dans des essais cliniques et les mutations connues pour entraîner une résistance aux médicaments, plus de la moitié des patients présentaient au moins une découverte potentiellement utile. Le test a également calculé deux caractéristiques d’ADN plus larges — la charge mutationnelle tumorale et l’instabilité des microsatellites — qui peuvent signaler des patients susceptibles de répondre aux inhibiteurs des points de contrôle immunitaire ; près de 9 % des patients semblaient être des candidats à une telle immunothérapie sur la base du seul prélèvement sanguin.
Différents cancers, différentes intensités de signal
Toutes les tumeurs ne libèrent pas d’ADN dans le sang de la même manière. Des cancers tels que colorectal, prostate et sein libèrent souvent suffisamment d’ADN pour que le test détecte aisément plusieurs altérations, tandis que les tumeurs cérébrales et de nombreux sarcomes en libèrent très peu, en partie à cause de barrières physiques comme la barrière hémato‑encéphalique ou parce que leurs altérations sont de types plus difficiles à détecter. Les chercheurs ont estimé, pour chaque patient, la fraction d’ADN libre circulant provenant de la tumeur. Cette « fraction tumorale » était généralement faible — environ 2 % en moyenne — probablement parce que de nombreux patients recevaient déjà un traitement, ce qui réduit la charge tumorale et la quantité d’ADN tumoral en circulation. Néanmoins, le large panel de gènes a aidé à confirmer la présence réelle d’ADN tumoral, rendant un résultat « négatif » plus fiable dans les cancers qui en libèrent à des niveaux modérés.
Suivre le cancer dans le temps et découvrir le risque héréditaire
Un sous‑groupe de patients a eu leur sang testé à plusieurs reprises. Pour certains initialement négatifs, des tests ultérieurs sont devenus positifs à mesure que les niveaux d’ADN tumoral augmentaient, suggérant une progression de la maladie plutôt qu’une apparition soudaine d’une résistance. Chez d’autres, de nouvelles mutations apparues lors de tests ultérieurs sont connues pour provoquer une résistance aux thérapies ciblées ou hormonales, illustrant comment des prélèvements sanguins sériés peuvent détecter plus tôt les voies d’échappement tumorales que les seuls scanners. Parallèlement, le séquençage des globules blancs a permis à l’équipe d’identifier des mutations héréditaires (germinales) dans des gènes de risque de cancer tels que BRCA1 et BRCA2. Environ 11 % des patients portaient de telles altérations héréditaires, ce qui peut influencer à la fois leur propre traitement — par exemple l’éligibilité aux inhibiteurs de PARP — et les recommandations de dépistage pour leurs familles. 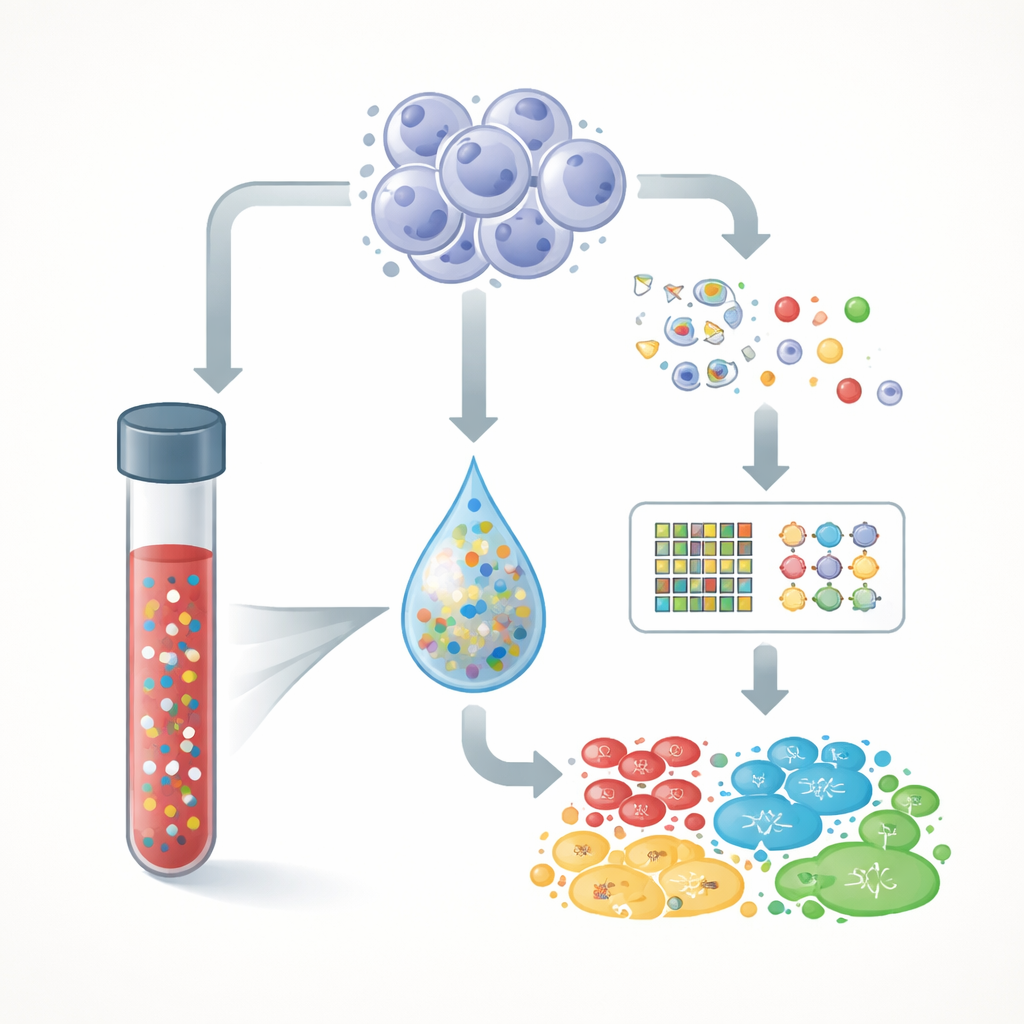
Comment le sang et le tissu fonctionnent ensemble
Pour 145 patients, les chercheurs ont pu comparer directement les résultats sanguins au tissu tumoral. Pour les mutations liées aux médicaments les plus importantes, la concordance entre sang et tissu était forte : environ 90 % du temps, ils s’accordaient sur la présence ou l’absence d’une cible clé. Dans certains cas, le test sanguin a détecté des modifications de résistance que l’échantillon tissulaire antérieur n’avait pas mises en évidence, probablement parce que la tumeur avait évolué sous l’effet du traitement. Dans d’autres cas, le tissu a révélé des altérations non détectables dans le sang, souvent dans des cancers qui libèrent peu d’ADN. Ce schéma suggère que sang et tissu ne sont pas opposés mais complémentaires : le tissu reste indispensable lorsque peu d’ADN tumoral circule, tandis que la biopsie liquide offre rapidité, moindre invasivité et possibilité de répétition des tests au fil de l’évolution de la maladie.
Ce que cela signifie pour les patients
Pour un non‑spécialiste, le message de cette étude est qu’un simple prélèvement sanguin peut désormais fournir un portrait génétique étonnamment complet de nombreux cancers avancés. En explorant un large spectre de plus d’un millier de gènes et en séparant soigneusement les signaux tumoraux du bruit de fond et des altérations héréditaires, le test a mis en évidence des options thérapeutiques et des indices de résistance chez la majorité des patients, et a signalé près d’un patient sur dix comme candidat possible à l’immunothérapie. Lorsqu’il est combiné à l’analyse tissulaire traditionnelle, cette approche augmente les chances de trouver une cible exploitable, aide les oncologues à choisir et à ajuster les traitements plus rapidement et peut mettre au jour des risques héréditaires importants pour des familles entières. Bien qu’elle ne remplace pas toutes les biopsies — en particulier pour les cancers qui libèrent peu d’ADN dans le sang — elle montre comment la biopsie liquide devient un complément puissant et pragmatique aux soins standards en oncologie en pratique réelle.
Citation: Florou-Chatzigiannidou, C., Papadopoulou, E., Metaxa-Mariatou, V. et al. Implementation of a 1021-gene liquid biopsy assay for real-world tumor genomic profiling in oncology practice. Sci Rep 16, 10064 (2026). https://doi.org/10.1038/s41598-026-40923-7
Mots-clés: biopsie liquide, ADN tumoral circulant, génomique du cancer, thérapie ciblée, inhibiteurs des points de contrôle immunitaire