Clear Sky Science · fr
IA explicable pour la surveillance des lésions gastro-intestinales et la délivrance de médicaments ciblés de précision
Des examens plus intelligents, des traitements plus sûrs
Beaucoup de personnes redoutent les traitements anticancéreux à cause de leurs effets secondaires sévères. Cette recherche explore un avenir dans lequel de minuscules caméras avalables, des algorithmes intelligents et des transporteurs de médicaments microscopiques coopèrent pour que des médicaments puissants soient délivrés uniquement là où ils sont réellement nécessaires. En fermant la boucle entre la détection d’un problème dans l’intestin et son traitement in situ, les auteurs visent à rendre les soins gastro-intestinaux plus précis, moins invasifs et beaucoup plus sûrs.
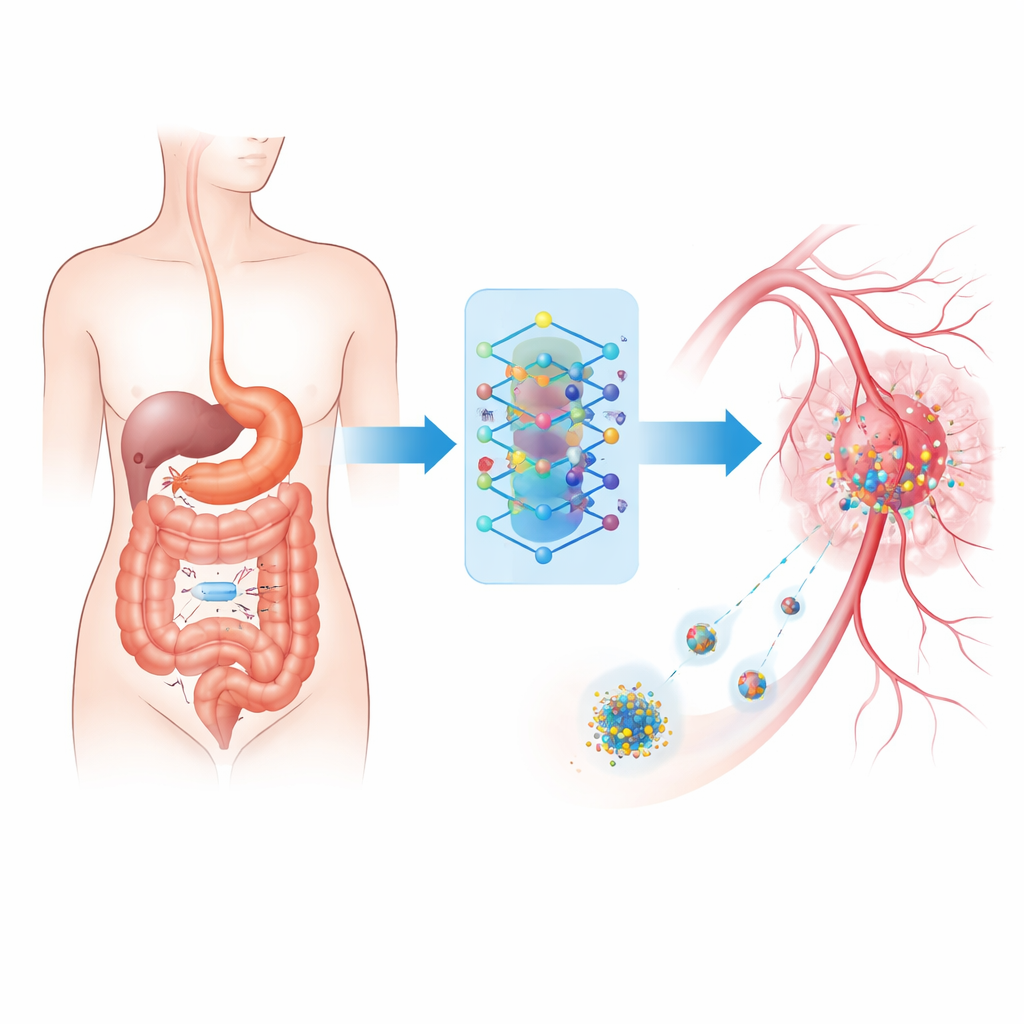
Une minuscule caméra en voyage
Au cœur du système se trouve un dispositif d’imagerie ingestible sans fil — une capsule de la taille d’un comprimé qui traverse naturellement le tube digestif en prenant des dizaines de milliers de photos. Plutôt que de compter uniquement sur un médecin pour passer en revue ce flot d’images, la capsule les envoie à une unité portable à l’extérieur du corps. Là, un ordinateur compact utilise un logiciel avancé de reconnaissance de motifs pour distinguer le tissu normal des lésions suspectes pouvant être cancéreuses ou fortement enflammées. Cette configuration reprend l’endoscopie par capsule déjà utilisée en milieu hospitalier, mais est améliorée pour fonctionner en temps réel et se connecter directement aux outils de traitement.
L’intelligence artificielle comme décideur
L’unité portable exécute un modèle d’analyse d’images soigneusement entraîné, basé sur des techniques modernes de vision par ordinateur. Il a appris à reconnaître 25 affections gastro-intestinales différentes — des polypes et ulcères à l’inflammation sévère — en s’appuyant sur une grande collection publique d’images d’endoscopie et de tissus. Pour tenir compte du fait que certaines maladies sont beaucoup plus rares que d’autres, les auteurs ont entraîné le système en deux étapes : d’abord pour apprendre les empreintes visuelles générales de chaque condition, puis pour l’affiner afin que les découvertes dangereuses mais peu fréquentes ne soient pas ignorées. Lors des tests, cette approche a correctement classé les images plus de neuf fois sur dix et a particulièrement bien réussi sur les catégories liées au cancer.
Voir à l’intérieur de la « boîte noire »
Parce que le personnel médical doit pouvoir faire confiance à tout diagnostic automatisé susceptible d’influer sur une posologie, les auteurs ont utilisé des techniques d’IA explicable pour montrer quelles parties de chaque image motivent la décision du modèle. Des superpositions de type carte de chaleur mettent en évidence les régions exactes considérées comme importantes par le système. Ces cartes explicatives n’ont pas été seulement inspectées visuellement ; elles ont été évaluées par des tests quantitatifs mesurant dans quelle mesure la confiance du modèle changeait lorsque les régions mises en évidence étaient retirées ou ajoutées, la stabilité des explications au cours de répétitions d’entraînement, et leur recouvrement avec des contours de lésions dessinés par des experts. Parmi plusieurs méthodes testées, une appelée LayerCAM a produit les explications les plus fidèles et cohérentes, aidant les médecins à vérifier que le système « regarde » au bon endroit.
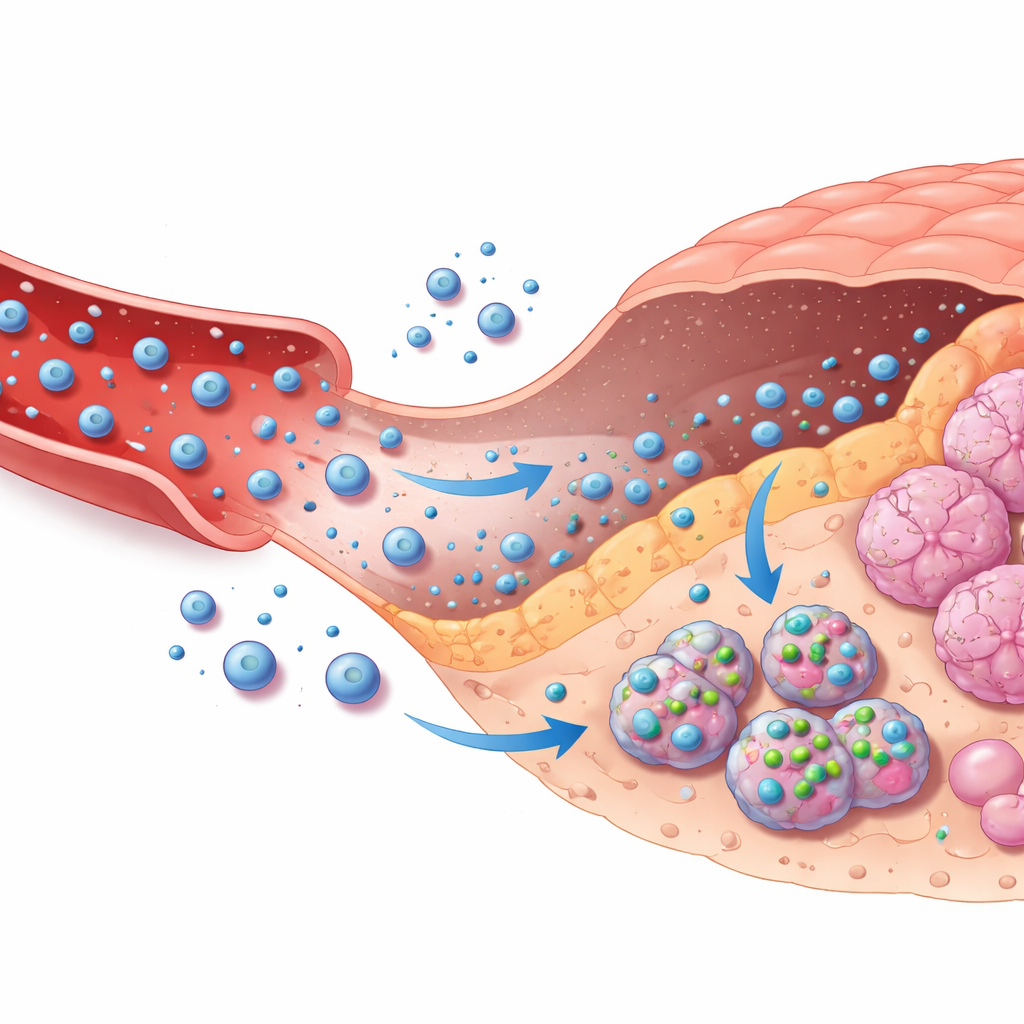
Guider les transporteurs de médicaments dans le corps
La seconde partie du cadre relie ces décisions basées sur l’image à la délivrance ciblée de chimiothérapie. Les auteurs modélisent comment un médicament anticancéreux courant, la doxorubicine, circule depuis une pompe externe dans le sang, s’échappe vers le tissu tumoral, pénètre dans les cellules tumorales, puis est finalement éliminé. Cela est capturé dans un modèle mathématique multi-compartiments qui suit les niveaux de médicament dans le sang, le tissu environnant et à l’intérieur des cellules. En fonction de la confiance de l’IA qu’une lésion est maligne et de la sévérité apparente, un système de règles simple choisit entre absence de traitement, traitement modéré ou traitement intensif, en ajustant la vitesse à laquelle les nanoparticules chargées libèrent leur charge et la durée de l’infusion. Une couche de sécurité vérifie en permanence les niveaux de médicament prédits à l’intérieur des cellules et réduit automatiquement les doses si un plafond de sécurité est approché, même si l’IA est trop confiante.
Protéger la vie privée et prévenir les usages abusifs
Comme le même canal qui transporte les images peut aussi porter des commandes de traitement, la sécurité est cruciale. Les auteurs présentent un schéma de confidentialité léger qui brouille les signaux biomédicaux à l’aide d’une carte mathématique chaotique avant qu’ils ne circulent dans le nano-réseau du corps, rendant les données interceptées très difficiles à interpréter. Par-dessus cela, la passerelle portable authentifie les dispositifs et vérifie que les signaux de commande correspondent à des schémas physiques attendus, aidant à bloquer les commandes falsifiées. Les simulations montrent comment différents réglages de confidentialité échangent une petite perte d’exactitude de détection contre une protection renforcée, et identifient des points d’exploitation qui maintiennent de bonnes performances cliniques tout en limitant fortement les fuites de données. Avec des limites strictes de dose, des règles d’arrêt d’urgence et des journaux de sécurité, ces mesures visent à rendre le système résilient face aux accidents comme aux attaques.
Ce que cela pourrait signifier pour les patients
En termes simples, ce travail esquisse le fonctionnement possible d’une boucle « voir-et-traiter » à l’intérieur du corps : une caméra avalable repère des zones suspectes, un assistant intelligent interprète ce qu’il voit avec un raisonnement transparent, et un système de délivrance contrôlée de médicaments répond avec des doses soigneusement limitées ciblées sur le tissu malade. L’étude reste théorique et basée sur des simulations, mais elle montre qu’un tel dispositif en boucle fermée peut atteindre les cibles thérapeutiques tout en respectant des limites de sécurité strictes, même lorsque l’IA commet des erreurs ou que les conditions varient d’un individu à l’autre. Si ce concept se concrétise, ce type de système pourrait aider à transformer la chimiothérapie brute en un outil bien plus précis et personnalisé pour les maladies gastro-intestinales.
Citation: Kamal, I.R., El-Zoghdy, S.F. & Soliman, R.F. Explainable AI for gastrointestinal lesion surveillance and precision targeted drug delivery. Sci Rep 16, 9807 (2026). https://doi.org/10.1038/s41598-026-40882-z
Mots-clés: imagerie gastro-intestinale, IA explicable, livraison ciblée de médicaments, nanomédecine, endoscopie par capsule