Clear Sky Science · fr
Un microARN issu de l’exon 4 d’amelogénine régule la formation de l’émail en contrôlant l’épissage de l’exon 4 et l’expression de l’amelogénine
Pourquoi un tout petit ARN compte pour des dents solides
L’émail dentaire est la substance la plus dure du corps humain, mais sa formation peut être étonnamment fragile quand elle déraille. Cette étude révèle comment un tout petit fragment d’information génétique, un microARN nommé miR‑exon4, aide les cellules qui forment les dents à produire un émail correctement durci. En montrant que ce microARN ajuste finement à la fois la protéine principale de l’émail et la chronologie du dépôt minéral, le travail relie des processus subtils de maturation de l’ARN à l’intérieur des cellules à des défauts d’émail visibles, similaires à ceux observés dans une maladie héréditaire appelée amélogenèse imparfaite.
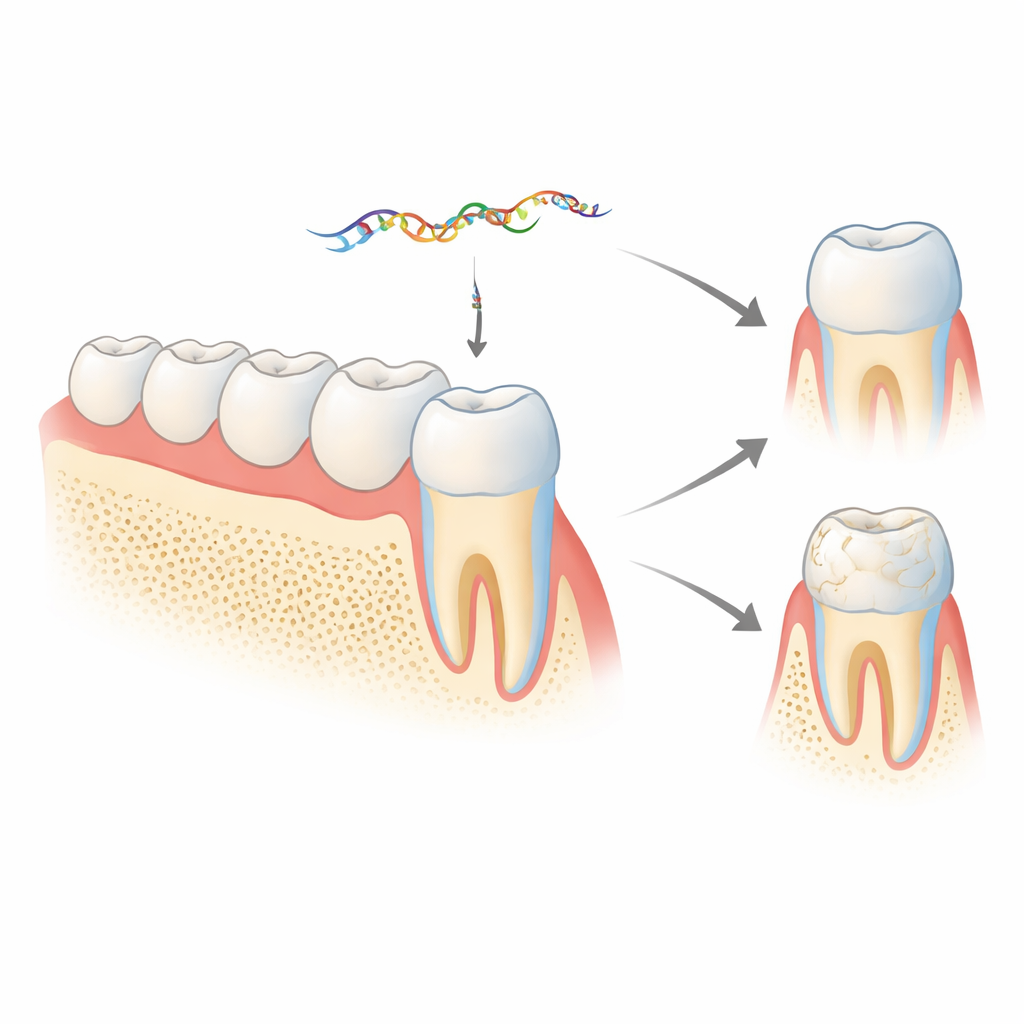
Un message caché à l’intérieur d’un gène de l’émail
L’émail est en grande partie construit à partir d’une protéine appelée amelogénine, produite par des cellules nommées améloblastes. Le gène de l’amelogénine (Amelx chez la souris) peut être découpé et recollé de différentes manières, créant plusieurs versions protéiques nécessaires à différents stades du développement dentaire. Un petit segment, appelé exon 4, est en général retiré du message final codant pour la protéine. Des travaux antérieurs de ce groupe ont montré que l’exon 4 écarté n’est pas du gaspillage : il est transformé en un microARN, miR‑exon4, qui peut réguler d’autres gènes importants pour l’os et l’émail. La nouvelle étude s’interroge sur ce qui se passe chez des animaux vivants lorsque ce microARN est réduit ou bloqué, et si ce dernier exerce aussi une rétroaction sur la façon dont l’amelogénine elle‑même est assemblée.
Une chaîne régulatrice à l’intérieur des cellules formatrices dentaire
Les chercheurs ont d’abord confirmé dans des dents de souris que miR‑exon4 participe à une chaîne régulatrice qu’ils avaient précédemment cartographiée dans des cellules en culture. Dans des organes émaillaires normaux, miR‑exon4 maintient deux gènes en amont, Nfia et Prkch, sous contrôle. Quand ces gènes sont bas, les niveaux d’un facteur de transcription clé, RUNX2, augmentent. En utilisant des souris soit dépourvues du gène de l’amelogénine, soit recevant un excès de miR‑exon4, ou traitées par un bloqueur de miR‑exon4, l’équipe a montré que la diminution de miR‑exon4 augmente Nfia et Prkch et réduit RUNX2, tandis que l’ajout de miR‑exon4 produit l’effet inverse. Ceci confirme que la voie miR‑exon4–Nfia/Prkch–RUNX2 fonctionne in vivo au sein des dents en développement.
De signaux perturbés à un émail affaibli
Pour voir comment ces variations moléculaires affectent l’émail réel, les scientifiques ont inhibé miR‑exon4 chez des souriceaux pendant une semaine durant la phase active de formation dentaire. L’imagerie 3D par rayons X a révélé que les animaux traités présentaient une diminution nette de l’émail fortement minéralisé, tant dans les incisives que dans les molaires. Des cartes thermiques et des coupes colorées ont montré que le démarrage de l’accumulation minérale le long de la couche d’émail était retardé et que la phase initiale de minéralisation était raccourcie, entraînant des surfaces plus rugueuses et des frontières moins nettes entre l’émail et les tissus sous‑jacents. En parallèle, les niveaux de la protéine RUNX2 dans les améloblastes ont diminué, tandis que la protéine amelogénine — y compris les isoformes contenant l’exon 4 — a augmenté. Ce profil reflète des modèles antérieurs où la surproduction d’une forme longue d’amelogénine contenant l’exon 4 provoque des défauts d’émail, suggérant que l’excès de cette isoforme, déclenché par la perte de miR‑exon4, peut perturber directement la minéralisation normale.
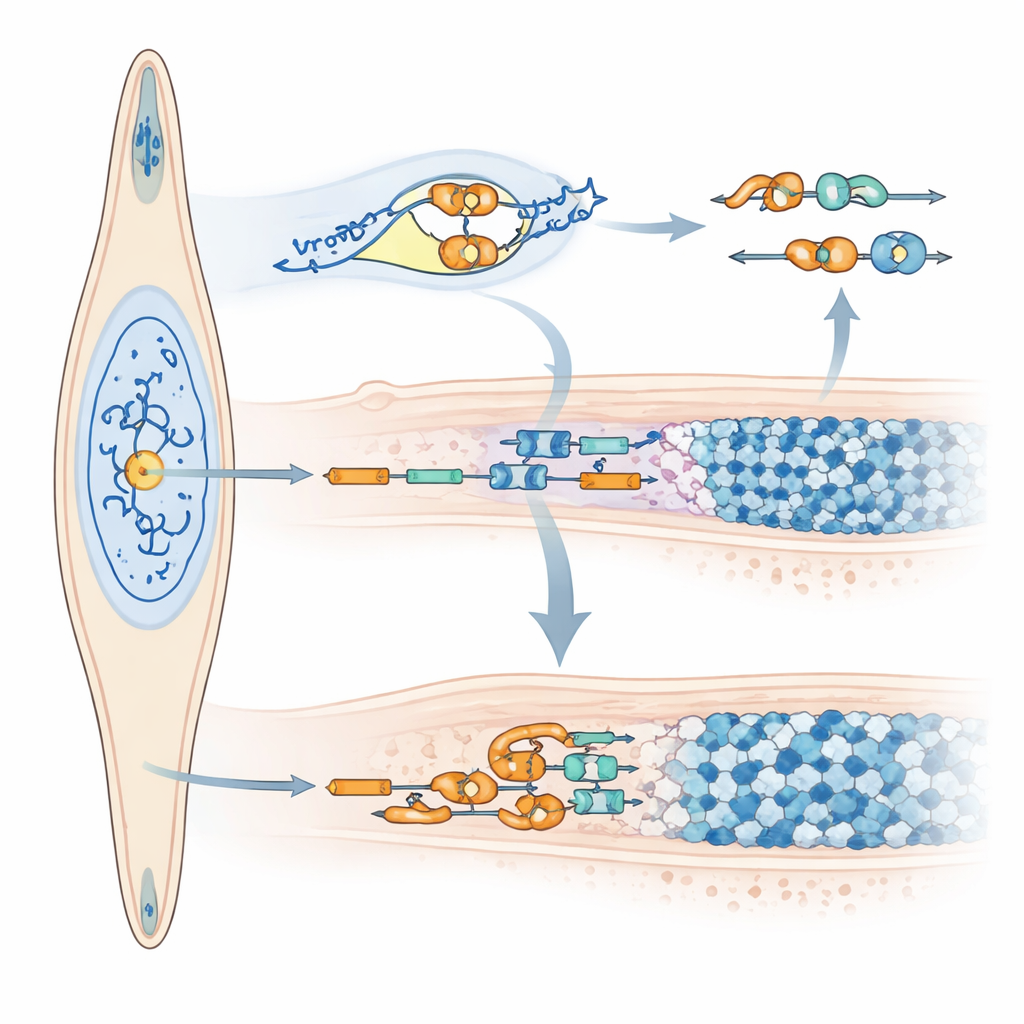
Comment le microARN reconfigure le message de l’amelogénine
Au‑delà de modifier la quantité d’amelogénine produite, miR‑exon4 altère aussi la façon dont le message d’amelogénine est découpé et épissé. Un blocage à court terme de miR‑exon4 a réduit les molécules d’ARN contenant encore l’exon 4 sans changer les niveaux totaux d’amelogénine, indiquant que l’exon 4 était plus souvent omis. L’équipe a relié ce changement à des variations dans plusieurs gènes régulateurs de l’épissage (SRSF), certains augmentant et d’autres diminuant lorsque miR‑exon4 était réduit. Dans des modèles cellulaires portant une version spécialement conçue du gène d’amelogénine produisant moins de miR‑exon4, l’exon 4 était également plus fréquemment évité. Fait crucial, le microARN lui‑même a été détecté à l’intérieur du noyau cellulaire, là où a lieu l’épissage, et des tests biochimiques ont montré qu’il s’associe à l’ARN précurseur de l’amelogénine en un point de contrôle précis dans l’intron voisin. Ces résultats soutiennent un double rôle pour miR‑exon4 : façonner indirectement le choix d’exon en modulant les facteurs d’épissage, et se lier directement près de l’exon 4 pour influencer s’il est conservé ou retiré.
Ce que cela signifie pour la santé de l’émail
Pris ensemble, les résultats présentent miR‑exon4 comme un petit mais central coordinateur de la formation de l’émail. Lorsqu’il est présent à un niveau approprié, il soutient l’activité normale de RUNX2, maintient l’équilibre de la production d’amelogénine et aide à garantir que l’exon 4 est inclus ou exclu aux bons stades. Quand miR‑exon4 fait défaut ou est réduit, cet équilibre bascule : les voies de signalisation sont perturbées, l’exon 4 est mal traité, les isoformes d’amelogénine deviennent déséquilibrées et la minéralisation précoce de l’émail est affaiblie. Ces enseignements contribuent à expliquer comment certaines mutations du gène de l’amelogénine peuvent provoquer des troubles d’émail héréditaires et mettent en lumière les microARN nucléaires comme des acteurs importants dans la formation du tissu le plus dur du corps.
Citation: Shemirani, R., Duong, T., Kim, R. et al. A splicing-derived microRNA from amelogenin exon4 regulates enamel formation via control of exon4 splicing and amelogenin expression. Sci Rep 16, 11044 (2026). https://doi.org/10.1038/s41598-026-40706-0
Mots-clés: émail dentaire, amelogénine, microARN, épissage de l’ARN, amélogenèse imparfaite