Clear Sky Science · fr
ABE9 fusionné à SpRY Cas9 nickase permet la génération précise de modèles murins sans « bystanders »
Des outils plus précis pour construire de meilleurs modèles de maladie
De nombreuses maladies graves sont causées par des fautes d’une seule lettre dans notre ADN. Pour comprendre ces affections et éventuellement les traiter, les chercheurs créent souvent des souris porteuses des mêmes mutations que les patients humains. Mais réécrire l’ADN avec une telle précision est étonnamment difficile : les méthodes anciennes peuvent laisser des cicatrices dans le génome, introduire des mutations supplémentaires et brouiller les résultats expérimentaux. Cette étude présente un outil d’édition génique raffiné, appelé ABE9-SpRY, conçu pour changer une seule lettre d’ADN tout en laissant les lettres voisines — et le reste du génome — largement intactes.
Des coupures brutales aux ajustements délicats de l’ADN
L’édition CRISPR‑Cas9 traditionnelle fonctionne comme une paire de ciseaux moléculaires, coupant les deux brins d’ADN. Les cellules réparent ces cassures de façon imparfaite, laissant souvent de petites insertions ou délétions qui perturbent les gènes de manière imprévisible. C’est utile pour inactiver des gènes, mais pas pour reproduire une mutation causale précise. Les éditeurs de bases, en revanche, ne coupent pas l’ADN. Ils poussent chimiquement une lettre d’ADN à se transformer en une autre — ici, convertir un A en G — tout en conservant l’intégrité de la double hélice. Cette approche réduit considérablement les grandes délétions et réarrangements, mais les premiers éditeurs d’adénine souffraient encore de trois limites principales : ils modifiaient parfois des lettres voisines « bystanders », ne pouvaient atteindre des sites d’ADN qu’à côté de courts motifs spécifiques, et provoquaient parfois des modifications à des endroits inattendus du génome.
Concevoir un crayon moléculaire plus sélectif
Les chercheurs ont cherché à résoudre ces trois limites simultanément. Ils ont commencé par ABE9, une variante d’éditeur de base plus récente qui concentre son activité sur une plage d’ADN très étroite, réduisant tellement la « fenêtre d’édition » que beaucoup moins de lettres voisines sont modifiées par erreur. Ils ont ensuite fusionné ABE9 à une Cas9 nickase modifiée appelée SpRY. Contrairement à la Cas9 standard, qui exige un motif strict « NGG » à côté du site cible, SpRY peut reconnaître un ensemble beaucoup plus large de séquences d’ADN. Cela permet d’atteindre des positions associées aux maladies qui étaient auparavant inaccessibles. L’outil fusionné résultant, ABE9‑SpRY, vise à être à la fois très précis et beaucoup plus flexible quant à ses sites d’action.
Test de performance dans des cellules et des embryons
Pour vérifier si ABE9‑SpRY tenait ses promesses, l’équipe l’a comparé à un éditeur plus agressif et largement utilisé, ABE8e‑SpRY. Ils ont ciblé quatre positions d’intérêt liées à des maladies dans des gènes codant pour des canaux ioniques (TPC1, TPC2 et TRPM4), importants pour le cœur et le foie. Dans des cellules nerveuses murines cultivées, ABE8e‑SpRY modifiait la lettre cible plus efficacement mais altérait aussi de nombreuses bases voisines. ABE9‑SpRY, en revanche, produisait moins d’éditions au total mais une fraction beaucoup plus élevée de résultats « propres » : des lectures où seule la lettre voulue avait été changée, sans mutations supplémentaires dans la région locale. Le même schéma a été observé dans des embryons de souris. Lorsqu’ils injectaient les composants d’édition dans des œufs fécondés, ABE8e‑SpRY convertissait souvent presque toutes les copies du gène cible, mais avec beaucoup de changements bystanders. ABE9‑SpRY éditait moins de copies au total, mais lorsqu’il agissait, la séquence d’ADN était généralement corrigée exactement comme prévu.
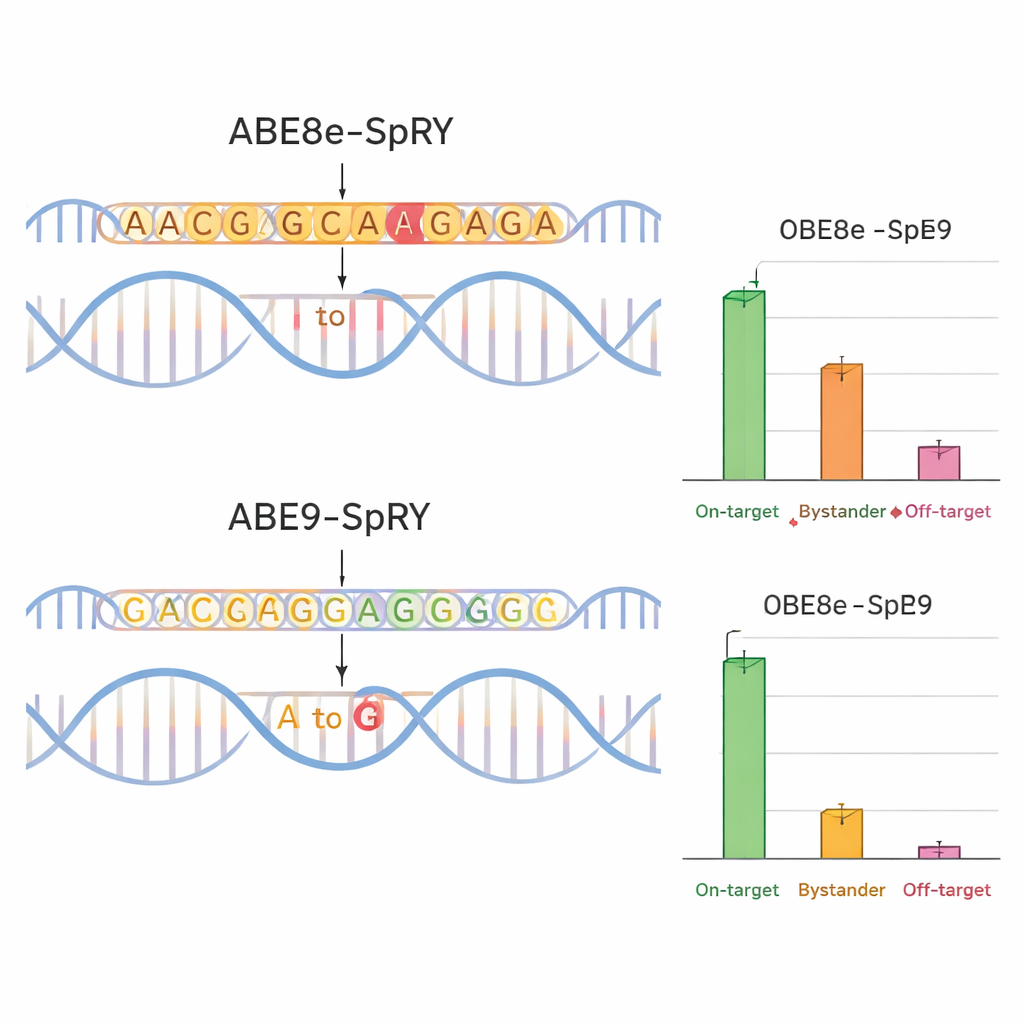
Éditions plus nettes, moins d’effets secondaires
La précision ne concerne pas seulement le voisinage immédiat de l’ADN. L’équipe a aussi examiné si leur éditeur modifiait des régions éloignées du génome. En combinant des prédictions informatiques et un séquençage ciblé, ils ont mesuré les modifications hors cible potentielles dans des sites ressemblant au site cible chez des embryons murins. ABE8e‑SpRY introduisait fréquemment des changements A→G non désirés à ces emplacements, parfois à des niveaux étonnamment élevés. ABE9‑SpRY montrait beaucoup moins d’événements de ce type, avec seulement de rares éditions hors cible et aucune activité détectable dans un test spécialisé pour les dommages à l’ADN indépendants de Cas9. Fait important, quand ABE9‑SpRY a été utilisé seul — et non dans des tests groupés — pour introduire deux mutations spécifiques chez la souris, il a généré de nombreux animaux fondateurs chez lesquels l’édition souhaitée était présente à un niveau élevé et transmise de façon fiable à la descendance, là encore avec des changements bystanders minimes et peu d’insertions ou délétions de petite taille.
Étendre l’édition précise aux cellules souches humaines
Comme les cellules souches patient‑spécifiques sont de plus en plus utilisées pour étudier les maladies et tester des médicaments, les chercheurs ont aussi testé ABE9‑SpRY dans des cellules souches pluripotentes induites humaines. Ils ont ciblé la version humaine du gène TPC1 à une position équivalente à l’un des sites murins. En utilisant un rapporteur fluorescent pour enrichir les cellules éditées, ils ont constaté qu’ABE8e‑SpRY produisait des taux bruts d’édition plus élevés mais modifiait encore plusieurs bases voisines. ABE9‑SpRY éditait moins d’allèles au total, mais la proportion de séquences parfaitement éditées — une seule modification voulue et rien d’autre — était nettement plus élevée, avec moins d’insertions ou délétions perturbatrices. Dans le travail sur cellules souches, où des clones individuels sont développés pour des études détaillées, ce type d’édition « propre » vaut généralement plus que l’efficacité brute.
Pourquoi cela compte pour la recherche future sur les maladies
Pour les chercheurs qui cherchent à comprendre comment un changement d’une seule lettre d’ADN provoque une maladie, des mutations accessoires non voulues peuvent être profondément trompeuses. Cette étude montre qu’ABE9‑SpRY, bien que quelque peu moins puissant en termes de vitesse brute d’édition, peut inscrire des changements d’une lettre dans les génomes de souris et de cellules souches humaines avec une précision remarquable et une large flexibilité de ciblage. Cela en fait un outil prometteur pour construire des modèles animaux et cellulaires fidèles des troubles génétiques humains, en particulier lorsque la présence d’une mutation accessoire pourrait confondre la biologie ou compromettre une thérapie potentielle.
Citation: Ong, J.K., Bhunia, S., Hilbert, B. et al. ABE9 fused to SpRY Cas9 nickase enables precise generation of bystander free mouse models. Sci Rep 16, 7463 (2026). https://doi.org/10.1038/s41598-026-40642-z
Mots-clés: édition de bases adénine, modèles de maladies CRISPR, génétique murine, effets hors cible, édition génique hiPSC