Clear Sky Science · fr
La variante de la chymotrypsine C (CTRC) p.R240Q associée à la pancréatite compromet sélectivement la dégradation du trypsinogène en perturbant des interactions électrostatiques à longue portée
Pourquoi cela compte pour la santé pancréatique
La pancréatite chronique est une inflammation douloureuse et durable du pancréas qui peut conduire au diabète, à des troubles digestifs et à une forte diminution de la qualité de vie. Cette étude examine pourquoi certaines personnes sont plus vulnérables en raison de petites variations héréditaires dans leurs enzymes digestives. En se concentrant sur une seule variante génétique d’une enzyme protectrice, les chercheurs montrent comment un changement moléculaire subtil peut faire basculer l’équilibre de la protection vers l’auto-digestion du pancréas.
Un système de sécurité intégré dans la digestion
Notre pancréas produit des enzymes protéolytiques puissantes qui sont normalement libérées dans l’intestin sous une forme inactive. L’un de ces précurseurs, le trypsinogène, peut parfois s’activer trop tôt, à l’intérieur du pancréas. Lorsqu’il en est ainsi, il peut commencer à digérer l’organe de l’intérieur et déclencher une inflammation. Pour éviter cela, l’organisme utilise des dispositifs de protection, notamment une protéine inhibitrice (SPINK1) et une autre enzyme digestive, la chymotrypsine C (CTRC). La CTRC a un double rôle : elle aide à activer les enzymes digestives quand et où elles sont nécessaires, mais elle coupe aussi l’excès de trypsinogène avant qu’il ne se transforme en trypsine active et ne cause des dégâts. Les personnes qui héritent de formes affaiblies de la CTRC présentent un risque accru de pancréatite chronique.
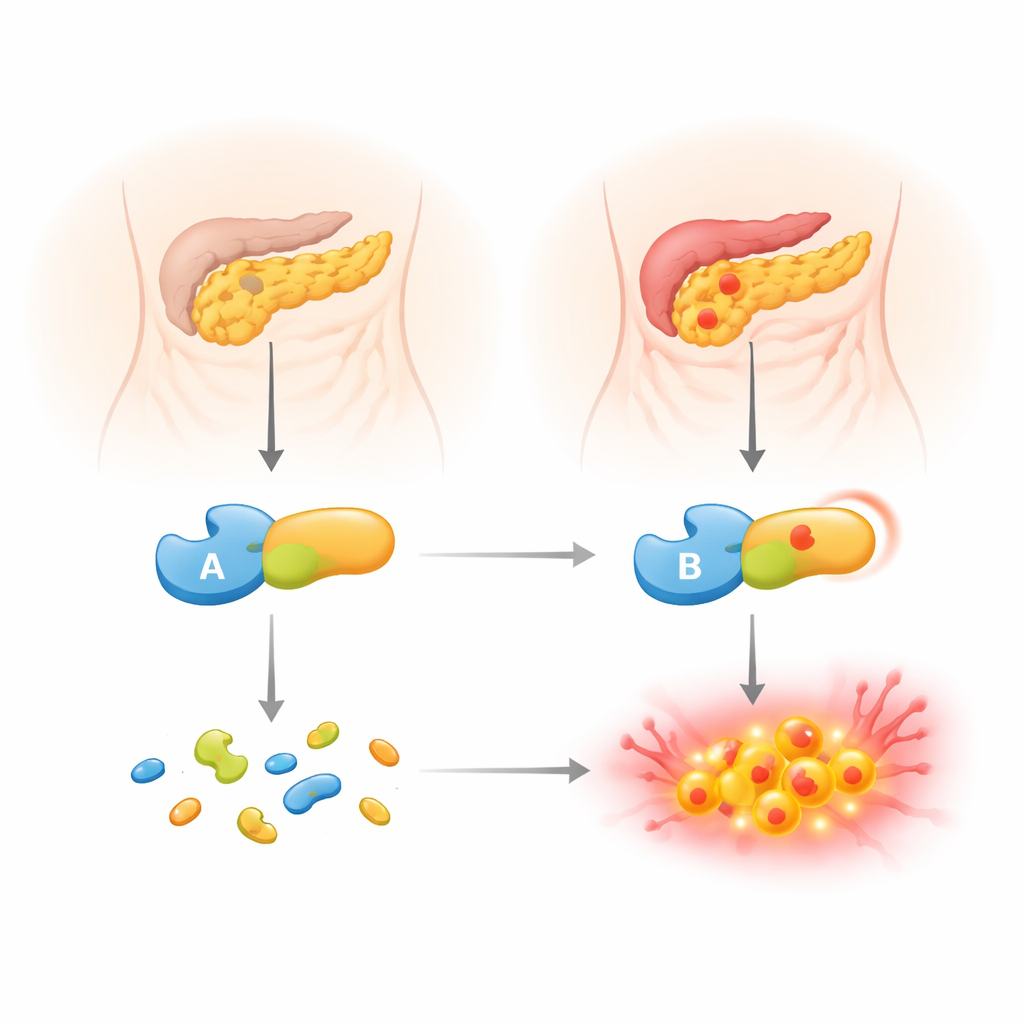
Un rare changement génétique passé au crible
L’équipe s’est concentrée sur une variante rare de la CTRC appelée p.R240Q, trouvée chez un garçon slovaque atteint d’une pancréatite chronique débutant dans l’enfance et chez son père affecté. Cette variante modifie un seul résidu à la surface de l’enzyme, remplaçant une unité chargée positivement par une unité neutre. De grandes bases de données génétiques la classent comme probablement bénigne, pourtant elle est apparue chez plusieurs jeunes patients atteints de la maladie. Pour déterminer son véritable effet, les auteurs ont combiné les informations génétiques de la famille avec des expériences de laboratoire détaillées. Ils ont comparé l’enzyme variante directement à la CTRC normale, en évaluant sa production et sa sécrétion cellulaires, son activité sur des substrats tests et son interaction avec le trypsinogène, la cible clé qu’elle doit contrôler.
Force normale, mais orientation compromise
Les chercheurs ont d’abord montré que les cellules synthétisent et sécrètent la CTRC p.R240Q aussi bien que la version normale : la variante n’entraîne donc pas de mauvais repliement ni de défaut de production. Dans des tests in vitro avec un petit peptide synthétique et une protéine du lait (bêta-caséine), la variante fonctionnait aussi bien, voire légèrement mieux, que la CTRC normale. Cela signifie que son pouvoir de coupure est intact. La surprise est venue en examinant la réaction qui importe le plus pour la pancréatite : la dégradation du trypsinogène cationique humain. Là, l’enzyme porteuse de la variante était beaucoup moins efficace — environ quatre à cinq fois plus lente pour fragmenter le trypsinogène et bien moins performante pour empêcher l’auto-activation du trypsinogène en trypsine. Dans des expériences d’auto-activation, il fallait beaucoup plus de CTRC variant pour maintenir les niveaux de trypsine sous contrôle comparé à l’enzyme normale.
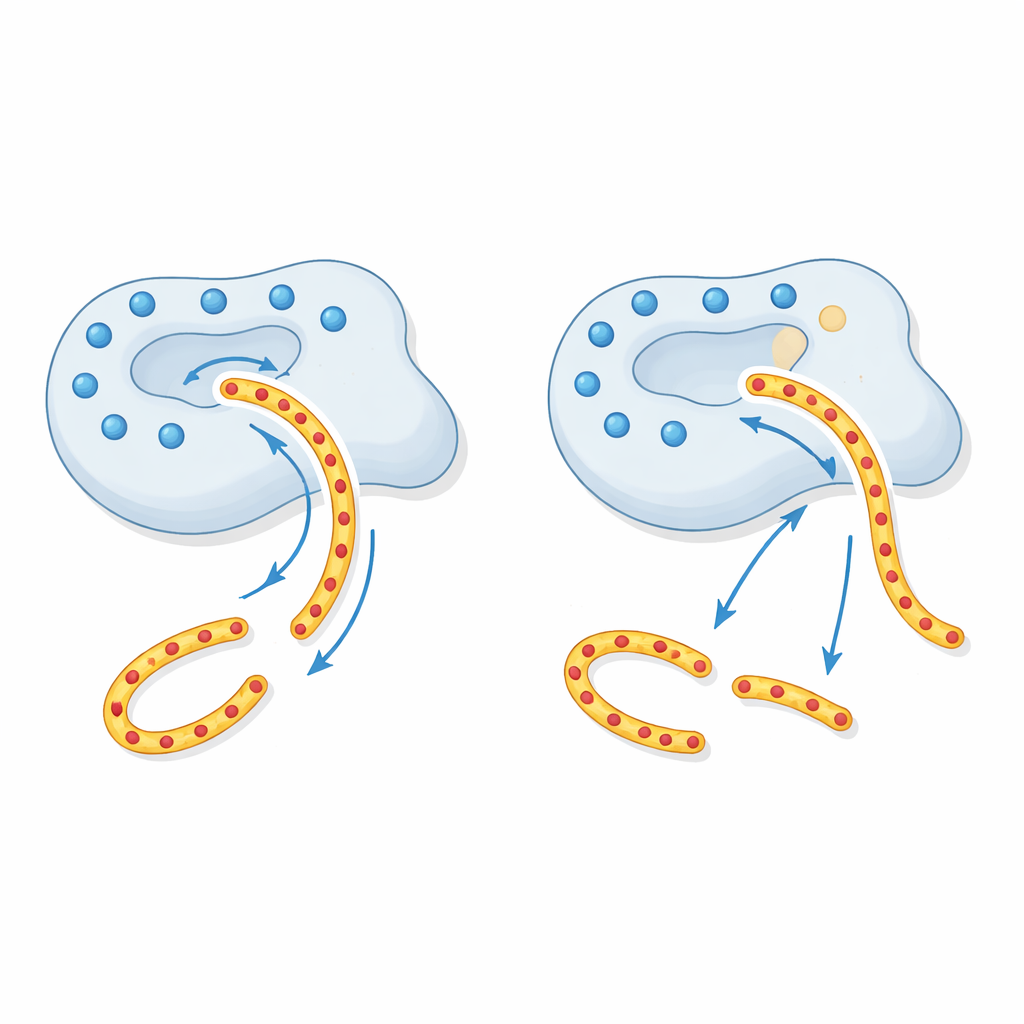
Un « faisceau tracteur » électrostatique perturbé
Pour comprendre pourquoi cela se produit, les auteurs se sont appuyés sur des modèles structuraux de la CTRC. Autour de la gouttière où la CTRC saisit ses substrats se trouve un anneau de charge électrique positive formé par plusieurs acides aminés chargés, dont le site modifié par p.R240Q. Les régions du trypsinogène que la CTRC doit couper sont fortement négatives, si bien que cet anneau positivement chargé agit comme un « faisceau tracteur » à longue portée, guidant le trypsinogène dans la bonne position. En neutralisant l’un de ces points positifs, la variante p.R240Q affaiblit cette attraction à distance. L’enzyme reste tranchante, mais le système de guidage étant endommagé, le trypsinogène ne se lie pas aussi efficacement, de sorte qu’une moindre quantité est dégradée en toute sécurité. D’autres substrats qui ne dépendent pas autant de ce motif de charge sont traités normalement, expliquant le défaut très sélectif observé dans les expériences.
Conséquences pour les patients et le diagnostic
Cliniquement, le garçon affecté et son père portaient aussi une seconde variante délétère de la CTRC, et le père présentait des facteurs de risque liés au mode de vie, comme une consommation excessive d’alcool. Cela correspond à l’idée que la pancréatite chronique résulte souvent de plusieurs atteintes génétiques et environnementales qui s’additionnent. Les travaux montrent qu’une variante considérée comme inoffensive par les outils prédictifs courants peut néanmoins être dangereuse d’une manière très spécifique. Pour le dépistage génétique, le message est clair : pour évaluer si une variante de CTRC augmente le risque de pancréatite, les scientifiques doivent la tester sur la cible réelle, le trypsinogène, et pas seulement sur des substrats génériques de laboratoire. En termes simples, cette étude révèle comment un minuscule changement à la « surface de guidage » de l’enzyme peut saper discrètement l’un des verrous de sécurité clés du pancréas, poussant des individus susceptibles vers une inflammation chronique.
Citation: Nagy, Z.A., Sándor, M., Hegyi, E. et al. Pancreatitis-associated chymotrypsin C (CTRC) variant p.R240Q selectively impairs trypsinogen degradation through disruption of long-range electrostatic interactions. Sci Rep 16, 8937 (2026). https://doi.org/10.1038/s41598-026-40633-0
Mots-clés: pancréatite chronique, chymotrypsine C, trypsinogène, variante génétique, enzymes digestives