Clear Sky Science · fr
La liaison à faible affinité de l’anticorps anti‑B7‑H3 clone MJ18 à B7‑H3 murin ne parvient pas à induire la régression tumorale
Pourquoi cela importe pour la recherche sur le cancer
L’immunothérapie du cancer repose souvent sur des anticorps — des protéines fabriquées en laboratoire conçues pour se fixer aux cellules tumorales et aider le système immunitaire à les détruire. Une cible prometteuse est une molécule appelée B7‑H3, abondante sur de nombreux cancers humains mais rare sur les tissus sains. Cet article examine de près un anticorps de recherche largement utilisé, MJ18, censé bloquer B7‑H3 dans les études murines. Les auteurs montrent que MJ18 adhère à peine à sa cible prévue et n’inhibe pas la croissance tumorale, ce qui soulève des doutes sur l’interprétation des expériences animales antérieures ayant utilisé cet outil.
La promesse d’un marqueur tumoral
B7‑H3 suscite un vif intérêt parce qu’il agit comme un bouclier moléculaire : les tumeurs riches en cette protéine contiennent en général moins de cellules immunitaires agressives et sont associées à de moins bons pronostics. Dans plusieurs modèles murins, la suppression du gène B7‑H3 dans les cellules tumorales libère une réponse immunitaire plus forte et peut entraîner la régression ou la disparition des tumeurs. Ces observations ont stimulé le développement de médicaments, de cellules immunitaires génétiquement modifiées et de conjugués anticorps‑médicament ciblant B7‑H3 sur les cancers humains. Cependant, la manière exacte dont B7‑H3 atténue l’immunité — et même quel récepteur il engage sur les cellules immunitaires — reste incertaine, d’autant plus que les versions murine et humaine de B7‑H3 diffèrent structurellement.
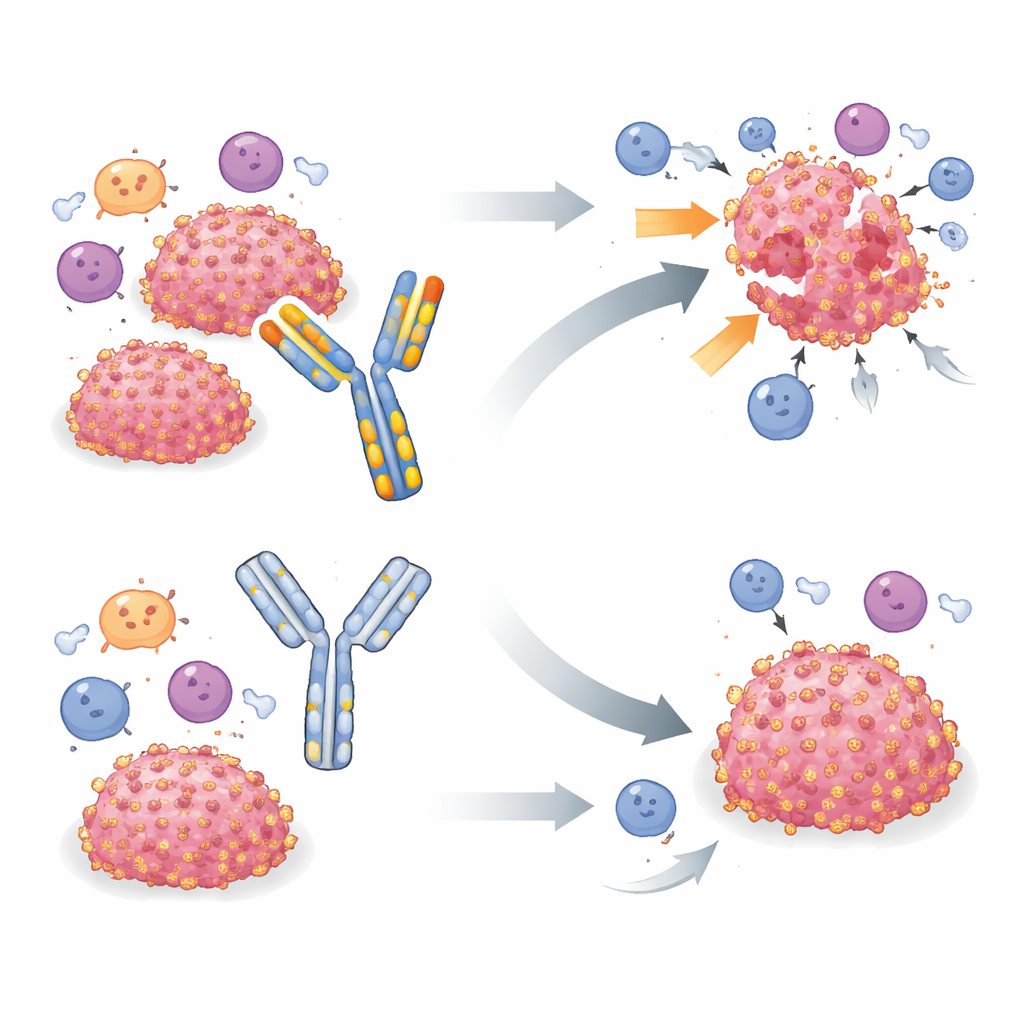
Un outil couramment utilisé passé au crible
Pour étudier B7‑H3 chez la souris vivante, de nombreux groupes se sont appuyés sur un seul anticorps dérivé du rat, MJ18, rapporté comme reconnaissant B7‑H3 murin et bloquant son activité immunosuppressive. Des études antérieures utilisant MJ18 dans divers modèles de maladies, y compris des cancers, ont souvent décrit un ralentissement de la croissance tumorale et une meilleure survie. L’équipe actuelle a d’abord testé MJ18 dans un modèle murin de rhabdomyosarcome, un cancer pédiatrique des tissus mous où B7‑H3 avait déjà été identifié comme un mécanisme d’échappement important. Lorsque MJ18 n’a pas amélioré le contrôle tumoral, les chercheurs ont élargi leurs essais à deux autres tumeurs positives pour B7‑H3 — des cancers pancréatiques et mammaires — qui sont clairement sensibles à la suppression du gène B7‑H3. Dans ces trois modèles, l’ablation de B7‑H3 dans les cellules tumorales retardait ou éliminait nettement les tumeurs, mais le traitement des souris avec MJ18, à des doses et sur des schémas similaires à ceux rapportés dans la littérature, n’a eu aucun impact détectable sur la croissance tumorale ni sur la survie.
Vérifier si MJ18 atteint vraiment sa cible
Les auteurs se sont alors posé une question fondamentale qui, étonnamment, n’avait jamais été traitée rigoureusement : MJ18 se lie‑t‑il vraiment à B7‑H3 murin, et avec quelle force ? Par cytométrie en flux, ils ont comparé MJ18 à un autre anticorps, EPNCIR122, connu pour détecter B7‑H3. Sur plusieurs lignées cellulaires tumorales murines, EPNCIR122 a donné un signal net qui disparaissait lorsque le gène B7‑H3 était supprimé, confirmant sa spécificité. MJ18, en revanche, n’a montré aucune liaison convaincante même à forte concentration. Lorsqu’ils ont examiné des cellules immunitaires de la rate, MJ18 a lié ces cellules, mais le profil n’était pas compatible avec B7‑H3, et EPNCIR122 n’a détecté aucune expression de B7‑H3 sur ces cellules, suggérant que MJ18 se fixait à autre chose.
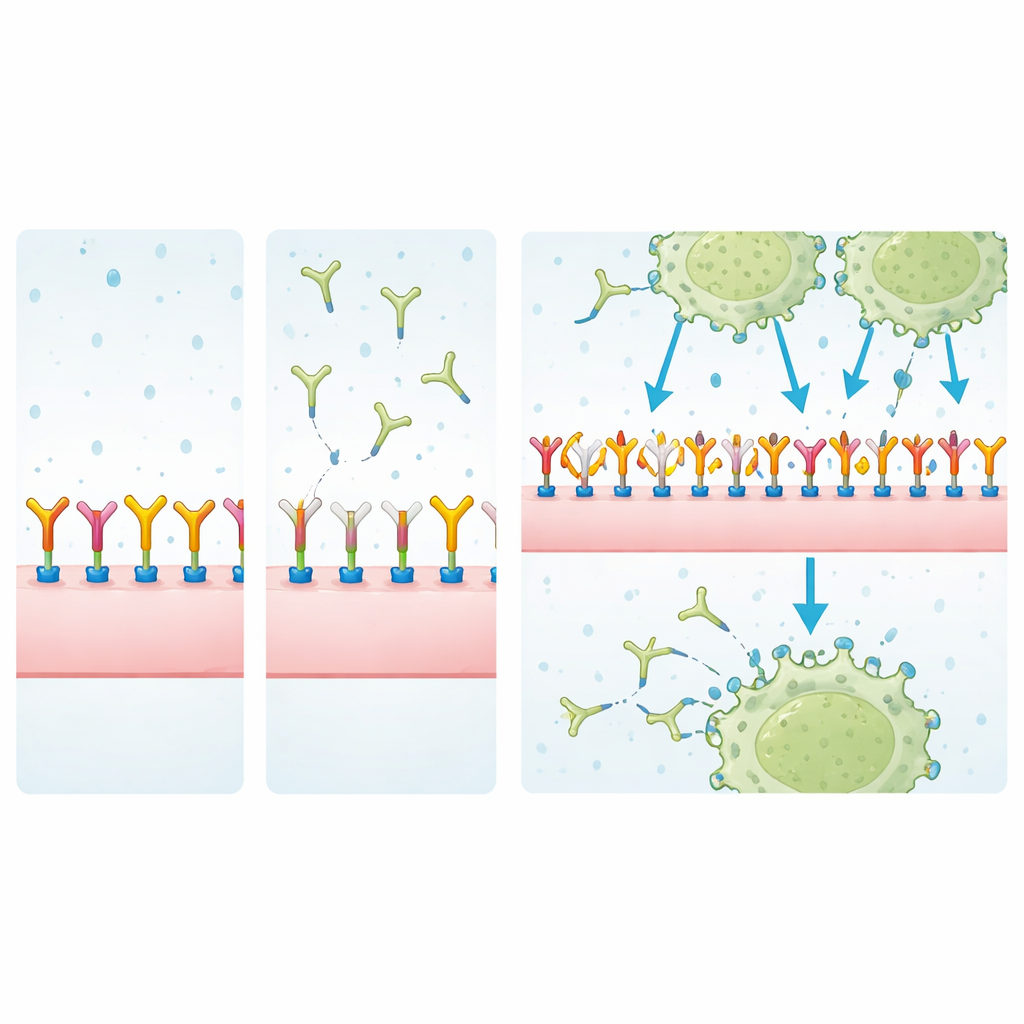
Creuser pour identifier les partenaires de liaison
Pour déterminer ce que MJ18 pourrait réellement reconnaître, les chercheurs ont capturé les protéines de surface cellulaire à l’aide de MJ18 ou d’EPNCIR122 et les ont analysées par spectrométrie de masse, en filtrant les contaminants de fond courants. Dans les cellules tumorales, EPNCIR122 a fortement enrichi B7‑H3 par rapport aux autres protéines, confirmant qu’il s’agit d’un réactif très spécifique. MJ18, en revanche, a extrait un mélange de protéines dans lequel B7‑H3 n’apparaissait que faiblement et à des niveaux comparables à des liaisons non spécifiques. Des mesures par résonance plasmonique de surface, une technique sensible pour quantifier les interactions moléculaires, ont confirmé le constat : l’affinité de MJ18 pour B7‑H3 murin était environ 7 000 fois plus faible que celle d’EPNCIR122 — bien en deçà de ce qui est habituel pour des anticorps thérapeutiques.
Quand des anticorps sont captés par de mauvaises cellules
L’histoire ne s’est pas arrêtée à la faible affinité. Dans les cellules de la rate, des tests supplémentaires ont montré que MJ18 et des anticorps de rat similaires étaient reconnus par des récepteurs Fc murins — des molécules sur les cellules immunitaires qui lient naturellement l’extrémité Fc des anticorps. Le blocage de ces récepteurs a fortement réduit le signal de MJ18, impliquant que la majeure partie de sa liaison apparente provenait des cellules immunitaires attrapant l’anticorps lui‑même, plutôt que d’un ciblage spécifique d’une protéine de surface. Les tentatives pour identifier un partenaire protéique unique de MJ18 sur les cellules immunitaires n’ont révélé que des candidats à des niveaux indiscernables du bruit de fond. Dans l’ensemble, les données suggèrent que MJ18 se comporte majoritairement comme un anticorps à faible affinité et non spécifique, dont les interactions sont dominées par l’engagement des récepteurs Fc plutôt que par la reconnaissance précise de B7‑H3.
Conséquences pour l’avenir
Pour les non‑spécialistes, la conclusion est simple : bien que B7‑H3 reste une cible intéressante sur de nombreux cancers, l’anticorps MJ18 n’est pas un outil fiable. Il se lie à B7‑H3 chez la souris très faiblement et ne reproduit pas le contrôle tumoral puissant observé lors de la suppression du gène B7‑H3. Les études murines antérieures qui ont rapporté des bénéfices marqués avec MJ18 pourraient donc refléter d’autres effets — par exemple l’engagement de la queue d’anticorps avec les récepteurs des cellules immunitaires — plutôt qu’un véritable blocage de B7‑H3. Les auteurs soutiennent que le domaine a un besoin urgent d’anticorps murins bien validés et à haute affinité contre B7‑H3, et que les chercheurs devraient systématiquement confirmer la spécificité et la force de tels outils. Ce n’est qu’avec des réactifs fiables que les résultats issus des modèles animaux pourront guider en toute confiance le développement de thérapies ciblant B7‑H3 chez les patients.
Citation: Gulyás, D., Nammor, T., Frizzell, J. et al. Low-affinity binding of anti-B7-H3 clone MJ18 to murine B7-H3 fails to induce tumor regression. Sci Rep 16, 9519 (2026). https://doi.org/10.1038/s41598-026-40628-x
Mots-clés: B7-H3, immunothérapie du cancer, validation d’anticorps, checkpoints immunitaires, modèles tumoraux