Clear Sky Science · fr
Analyse théorique de la suppression optogénétique à faible puissance des potentiels d’action dans des cardiomyocytes ventriculaires humains exprimant des channelrhodopsines sélectives pour le potassium
Une façon plus douce, à base de lumière, d’apaiser un cœur affolé
Les rythmes cardiaques rapides et chaotiques peuvent provoquer des évanouissements, des AVC ou une mort subite. Les traitements actuels — médicaments puissants, défibrillateurs implantés ou chocs à haute énergie — peuvent sauver des vies mais sont aussi douloureux et imprécis. Cette étude explore une idée très différente : utiliser de faibles éclairs de lumière et des protéines spécialement conçues pour ramener discrètement les cellules cardiaques à un rythme sûr et régulier, en consommant beaucoup moins d’énergie que les approches actuelles.
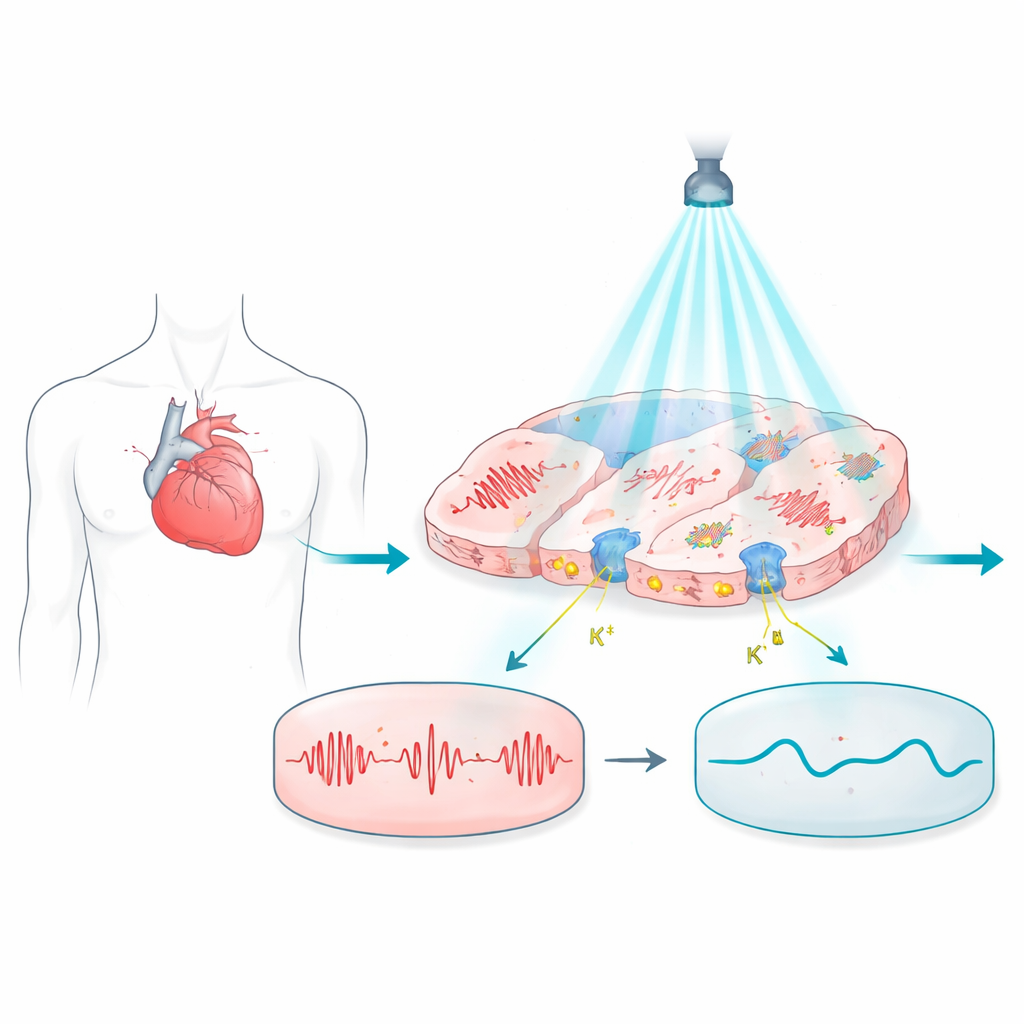
Éclairer les battements cardiaques problématiques
Les travaux reposent sur l’optogénétique, une technique consistant à équiper les cellules de protéines sensibles à la lumière pour contrôler leur activité électrique par des éclairs lumineux. Dans le cœur, ces protéines peuvent en principe remplacer les électrodes métalliques, offrant un contrôle sans contact et indolore. Mais la plupart des protéines activées par la lumière utilisées jusqu’à présent tendent à pousser le potentiel de membrane vers le haut, vers un état excité, ce qui rend difficile de maintenir les cellules au repos ou d’ajuster finement la durée de chaque battement. Cela limite leur utilité pour éteindre en toute sécurité des rythmes dangereux ou corriger des troubles électriques dépendant de subtils timings.
Nouveaux interrupteurs lumineux accordés sur le « repos » du cœur
Des protéines récemment découvertes, appelées channelrhodopsines sélectives pour le potassium, notamment WiChR et HcKCR1, semblent résoudre ce décalage. Contrairement aux protéines plus anciennes qui laissent passer un mélange d’ions, ces canaux préfèrent fortement le potassium et ramènent naturellement le potentiel de membrane vers le même niveau négatif qu’au repos. Les auteurs ont construit des modèles informatiques détaillés de cardiomyocytes ventriculaires humains exprimant ces nouveaux canaux et les ont comparés à deux opsines plus excitatrices bien connues, ChR2(H134R) et ChRmine. En simulant la réponse de ces cellules à différentes longueurs d’onde et intensités lumineuses, ils ont pu explorer en toute sécurité des conditions difficiles ou longues à tester sur des cœurs réels.
Lumière douce, contrôle puissant
Les simulations montrent que les canaux sélectifs pour le potassium offrent un contrôle bien plus économique et stable. En particulier, WiChR pourrait complètement bloquer les potentiels d’action — ces brèves impulsions électriques qui déclenchent chaque battement — en utilisant des intensités lumineuses des centaines à des milliers de fois plus faibles que celles requises pour de nombreux outils antérieurs. Sous lumière continue, WiChR et HcKCR1 maintenaient le potentiel de membrane près de son niveau de repos normal, maintenant la cellule dans un état calme et sûr. En revanche, ChR2 et ChRmine avaient tendance à pousser le potentiel vers des valeurs plus positives, bloquant parfois l’activité mais seulement après avoir forcé la cellule dans un état stressé et hyperexité. WiChR fonctionnait aussi bien avec de brèves impulsions lumineuses, empêchant de façon fiable les pics électriques cellule par cellule, ce qui suggère qu’elle pourrait suivre des rythmes cardiaques rapides sans surchauffer les tissus ni gaspiller d’énergie.
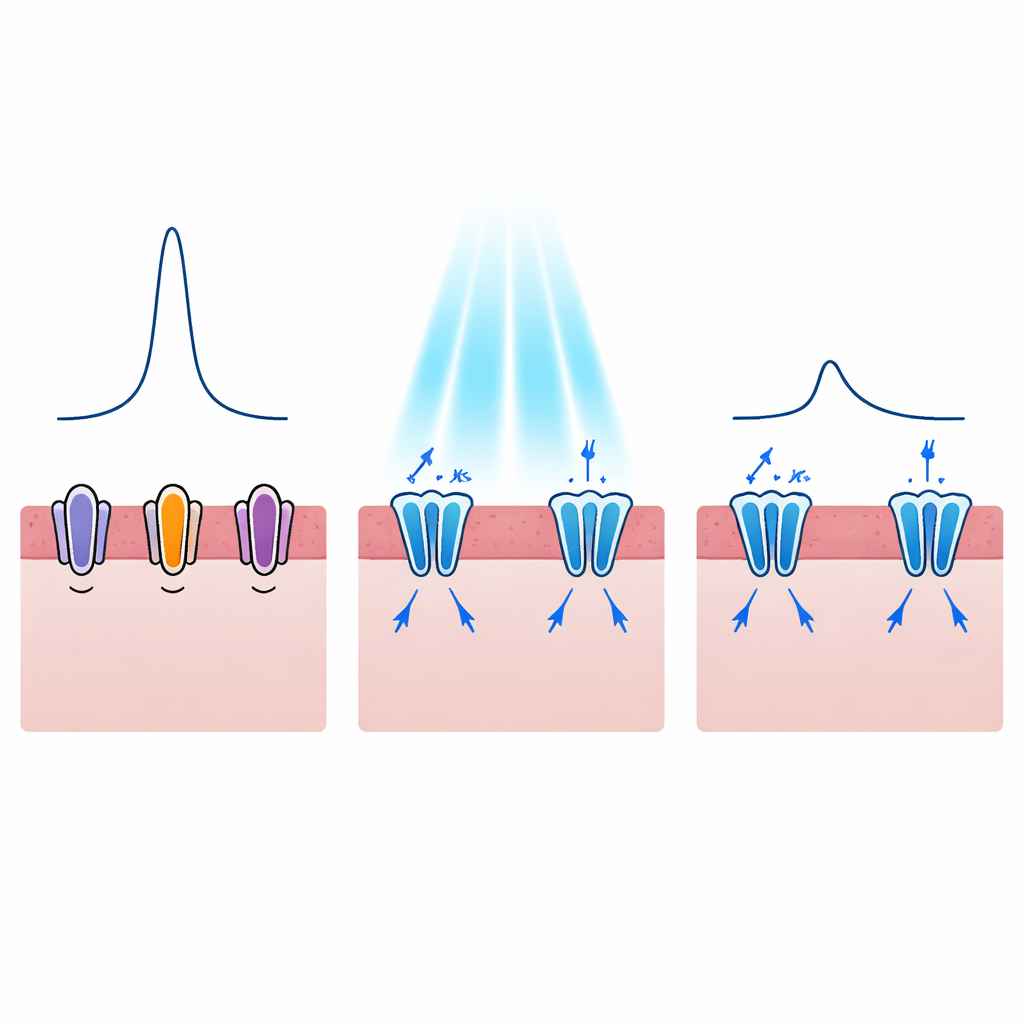
Façonner chaque battement, pas seulement l’arrêter
Les arythmies dangereuses sont souvent liées non seulement au fait qu’une cellule cardiaque déclenche ou non un battement, mais aussi à la durée de son état excité. Dans des troubles comme le syndrome du QT long, l’impulsion électrique de chaque battement est prolongée, augmentant le risque de basculement vers des rythmes potentiellement mortels. Les auteurs se sont donc demandé si des canaux potassiques activés par la lumière pouvaient raccourcir cette impulsion de manière contrôlée. Leurs modèles ont montré que l’activation de WiChR ou HcKCR1 pendant la phase de plateau du potentiel d’action générait de forts courants potassiques sortants qui ramenaient le potentiel à la baisse plus tôt. À mesure que l’intensité lumineuse augmentait, la durée de l’impulsion électrique passait d’environ 300 millisecondes à environ la moitié de cette valeur, et cet effet pouvait être obtenu même avec des éclairs lumineux très courts. WiChR avait tendance à produire des périodes de silence plus durables, tandis que HcKCR1 offrait un rétablissement plus rapide une fois la lumière éteinte, suggérant des usages cliniques potentiels différents.
Des modèles informatiques aux thérapies futures
Globalement, l’étude conclut que les canaux lumineux sélectifs pour le potassium, en particulier WiChR, sont des outils prometteurs pour un contrôle cardiaque doux et à faible consommation d’énergie. Ils peuvent à la fois faire taire une activité électrique incontrôlée et raccourcir des battements excessivement longs, tout en maintenant le potentiel de membrane proche de son état de repos naturel. Bien que les résultats proviennent de simulations détaillées de cellules isolées plutôt que d’expériences sur un cœur entier, ils fournissent des indications quantitatives sur la quantité de lumière nécessaire, le moment opportun pour l’appliquer et les variantes protéiques les mieux adaptées selon les objectifs. À long terme, cette voie de recherche ouvre la perspective où des cardiologues utiliseraient des faisceaux de lumière finement réglés, plutôt que des chocs douloureux, pour prévenir ou arrêter des arythmies potentiellement mortelles.
Citation: Dixit, N., Pyari, G. & Roy, S. Theoretical analysis of low-power optogenetic suppression of action potentials in human ventricular cardiomyocytes expressed with potassium-selective channelrhodopsins. Sci Rep 16, 9765 (2026). https://doi.org/10.1038/s41598-026-40578-4
Mots-clés: optogénétique cardiaque, suppression des arythmies, channelrhodopsines potassiques, durée du potentiel d’action, syndrome du QT long