Clear Sky Science · fr
Sexage in ovo et génotypage par techniques PCR : une contribution aux principes des 3R dans l’élevage de poulets
Pourquoi ce qui se passe à l’intérieur d’un œuf compte
Chaque année, des millions de poussins mâles sont tués peu après l’éclosion parce qu’ils ne sont pas utiles à la production d’œufs. Parallèlement, des laboratoires de recherche dans le monde éclosent plus d’animaux qu’il n’en faut simplement parce qu’ils ne peuvent pas déterminer suffisamment tôt le sexe ou le patrimoine génétique d’un embryon. Cette étude présente une méthode pratique pour « lire » le sexe et les gènes d’un poussin alors qu’il se développe encore à l’intérieur de l’œuf, en utilisant des tests ADN standard. En procédant tôt et en douceur, la méthode vise à éviter l’éclosion d’animaux excédentaires et à réduire la souffrance, sans exiger d’équipements industriels coûteux.
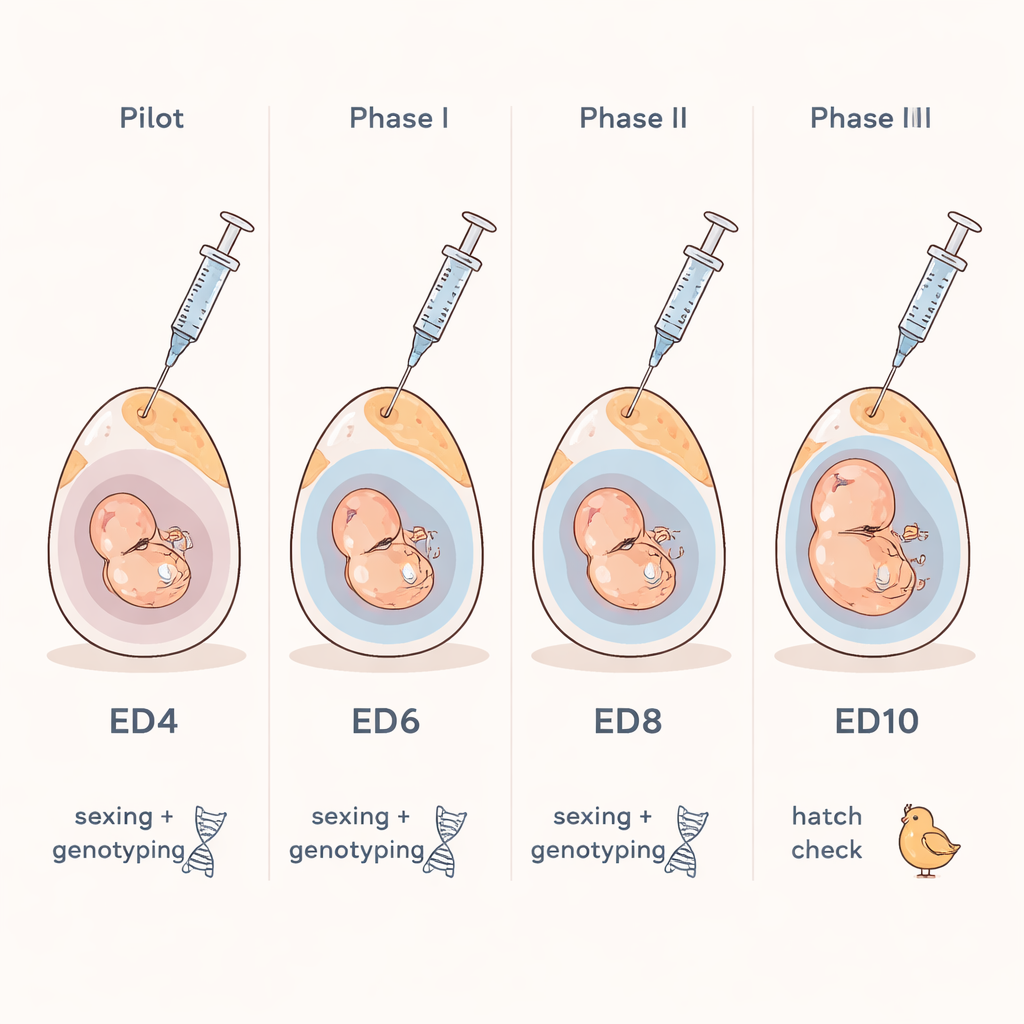
Regarder à l’intérieur de l’œuf sans l’ouvrir
Les chercheurs se sont concentrés sur une question simple : peut‑on prélever en toute sécurité un minuscule échantillon de fluide d’un œuf de poule fécondé et l’utiliser pour identifier le sexe de l’embryon et des traits génétiques clés ? Ils se sont appuyés sur un concept familier de la médecine humaine, où l’on analyse des liquides autour du fœtus pour rechercher des anomalies génétiques. Chez la poule, une fine poche remplie de liquide appelée allantoïde se forme autour de l’embryon au fur et à mesure de son développement. Au septième jour d’incubation, cette poche contient suffisamment de fluide pour qu’une aiguille fine puisse l’atteindre sans toucher l’embryon lui‑même. L’équipe a utilisé une lampe puissante pour localiser la chambre à air à l’extrémité arrondie de l’œuf, a percé une ouverture de la taille d’une épingle dans la coquille et a aspiré quelques gouttes de fluide avec une toute petite seringue.
De quelques gouttes à une empreinte génétique
Le fluide prélevé sur des œufs tôt dans le développement contient des quantités infimes d’ADN. Pour contourner ce problème, les scientifiques ont d’abord amplifié l’ensemble du matériel génétique présent dans chaque échantillon, créant de nombreuses copies sans en modifier le contenu. Ils ont ensuite appliqué deux tests de laboratoire courants : une réaction en chaîne par polymérase (PCR) standard et une variante appelée Kompetitive Allele Specific PCR (KASP). Ces deux tests peuvent distinguer les chromosomes sexuels des poussins mâles et femelles et détecter des marqueurs génétiques spécifiques, comme la mutation responsable d’une coquille d’œuf bleue ou la présence d’un gène inséré en laboratoire dans des lignées de recherche spécialisées. Sur plus de 800 œufs issus de plusieurs races — y compris des pondeuses commerciales brunes et blanches, des croisements Araucana colorés et une lignée de recherche génétiquement modifiée — ces méthodes ont fourni des identifications correctes dans environ 92 à 100 % des cas.
Déterminer le moment le plus sûr pour prélever
Un prélèvement trop précoce risque d’endommager des structures fragiles, vitales pour l’embryon, tandis qu’un prélèvement trop tard laisse peu de temps pour agir sur les résultats. Pour définir la fenêtre idéale, l’équipe a d’abord cultivé des embryons hors coquille afin d’observer comment les membranes et les espaces fluides se développent dans le temps. Ils ont ensuite réalisé une série d’essais à différents stades sur des œufs intacts. Du quatrième jour, il était possible de recueillir du fluide, mais les taux de réussite des tests ADN étaient plus faibles à ces stades précoces et la procédure était techniquement plus difficile. En comparant les taux d’éclosion entre œufs perforés et œufs témoins intacts, ils ont constaté que le septième jour offrait le meilleur compromis : il y avait suffisamment d’allantoïde claire, les tests ADN fonctionnaient de façon fiable et la plupart des embryons survivaient jusqu’à l’éclosion. À ce stade, il reste encore plusieurs jours avant l’apparition probable de la perception de la douleur chez l’embryon de poussin, ce qui offre une marge éthique pour la prise de décision.
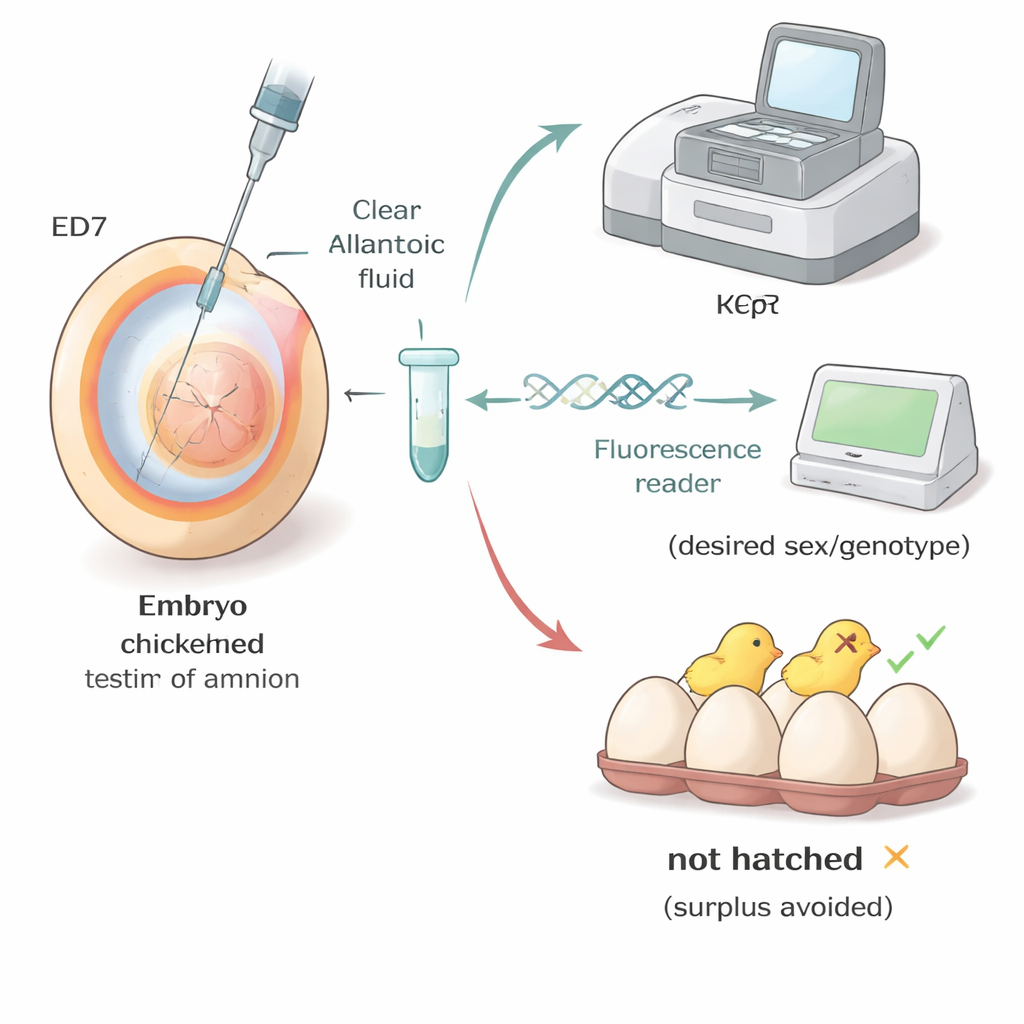
Mettre la méthode en œuvre dans des troupeaux réels
Les chercheurs ont testé leur protocole dans des conditions proches de celles des installations d’élevage et des laboratoires universitaires. Dans des lignées de pondeuses commerciales brunes et blanches, les œufs prélevés entre les jours quatre et sept ont montré que la capacité d’éclosion s’améliorait généralement lorsque le prélèvement était réalisé plus tard, avec de meilleurs résultats au jour sept. Dans une lignée « hôte de substitution » spécialisée utilisée pour la génétique avancée, l’équipe est allée plus loin : ils ont sexé et génotypé les embryons au jour sept, puis n’ont laissé poursuivre l’éclosion que pour ceux présentant la combinaison de sexe et de gènes souhaitée. Presque tous les embryons sélectionnés ont éclos en poussins sains qui ont évolué normalement, démontrant que la sélection précoce peut réduire fortement le nombre d’animaux indésirables sans compromettre la qualité des poussins.
Ce que cela signifie pour le bien‑être animal et la recherche
Pour un non‑spécialiste, le message principal est simple : d’un petit trou d’épingle et avec des outils de laboratoire courants, il est désormais possible de savoir, pendant que le poussin est encore en sécurité à l’intérieur de l’œuf, s’il est mâle ou femelle et s’il porte des traits génétiques particuliers. L’étude montre que réaliser cela autour du septième jour d’incubation est à la fois techniquement fiable et suffisamment doux pour que la plupart des embryons survivent. En permettant d’éliminer les embryons indésirables avant qu’ils ne soient probablement capables de ressentir la douleur, l’approche soutient les principes largement acceptés des 3R : remplacer, réduire et améliorer l’utilisation des animaux en science. Pour les couvoirs comme pour les laboratoires de recherche, cette technique offre une voie réaliste vers moins d’animaux en surplus, une meilleure utilisation des ressources et des standards de bien‑être plus élevés — sans besoin de machines industrielles complexes.
Citation: Dierks, C., Förster, A., Meunier, D. et al. In ovo sexing and genotyping using PCR techniques: a contribution to the 3R principles in chicken breeding. Sci Rep 16, 7464 (2026). https://doi.org/10.1038/s41598-026-40562-y
Mots-clés: embryon de poulet, sexage in ovo, génotypage PCR, bien‑être animal, principes des 3R