Clear Sky Science · fr
L’axe MEOX1-PAX1 régule de concert la malignité des cellules tumorales et la différenciation des Treg dans le glioblastome
Pourquoi cette étude sur le cancer du cerveau est importante
Le glioblastome est l’un des cancers du cerveau les plus mortels, en partie parce que la tumeur peut à la fois croître rapidement et se dissimuler aux défenses de l’organisme. Cette étude révèle une « chaîne de commandement » moléculaire à l’intérieur des cellules tumorales qui non seulement alimente leur comportement agressif mais apprend aussi aux cellules immunitaires voisines à se tenir en retrait. En décodant cette chaîne, les chercheurs suggèrent une façon d’attaquer à la fois la tumeur et son bouclier immunitaire.
Une tumeur mortelle qui désarme les défenses
Le glioblastome est réputé pour récidiver après chirurgie, radiothérapie et chimiothérapie. Une des raisons en est son voisinage hostile, appelé microenvironnement tumoral. Plutôt que d’être rempli de cellules qui combattent le cancer, cet environnement contient souvent des cellules immunitaires qui protègent en réalité la tumeur. Parmi les plus importantes se trouvent les cellules T régulatrices, ou Tregs, un type de globules blancs qui empêche normalement une inflammation excessive. Dans le glioblastome, cependant, les Tregs s’accumulent autour de la tumeur et l’aident à échapper à l’attaque immunitaire.
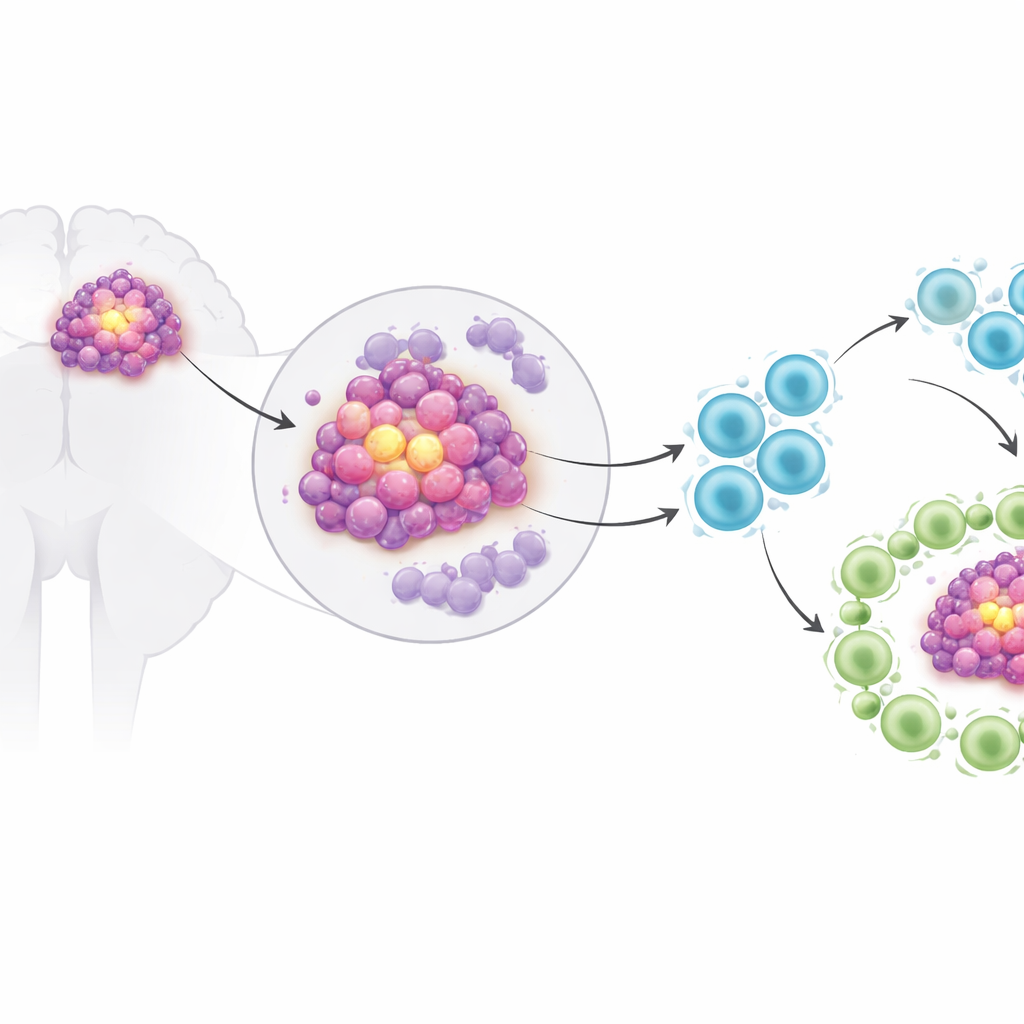
Deux interrupteurs clés à l’intérieur des cellules tumorales
Les chercheurs se sont focalisés sur deux protéines qui agissent comme des interrupteurs génétiques dans les cellules : MEOX1 et PAX1. Des travaux antérieurs avaient lié MEOX1 à la croissance tumorale et suggéré qu’il pouvait influencer les cellules immunitaires, tandis que PAX1 est mieux connu comme suppresseur de tumeur qui freine la prolifération cellulaire. Dans des cellules de glioblastome cultivées en laboratoire, l’équipe a montré qu’une augmentation de MEOX1 rendait les cellules tumorales plus prolifératives, plus mobiles et capables d’envahir des barrières, tout en réduisant leur propension à mourir. Abaisser MEOX1 produisait l’effet inverse, ralentissant la croissance et favorisant la mort cellulaire. Ils ont ensuite démontré que MEOX1 exerce ces effets en réprimant PAX1 ; lorsque les niveaux de PAX1 étaient restaurés, les actions néfastes de MEOX1 disparaissaient en grande partie.
Des interrupteurs tumoraux au remodelage immunitaire
L’étude a dépassé la seule croissance tumorale pour explorer comment ce tableau de commandes interne affecte les cellules immunitaires. Les scientifiques ont cultivé des cellules humaines de glioblastome en présence de lymphocytes CD4 purifiés, un groupe de cellules immunitaires qui peuvent devenir soit des cellules auxiliaires orientées vers l’attaque, soit des Tregs apaisants. Ils ont constaté que lorsque PAX1 dans les cellules tumorales était réduit, davantage de lymphocytes environnants se différenciaient en Tregs. Lorsque PAX1 était augmenté, moins de lymphocytes prenaient cette identité suppressive. Des échantillons tissulaires d’un patient atteint de glioblastome montraient un nombre plus élevé de Tregs dans les zones tumorales que dans le tissu cérébral non tumoral adjacent, ce qui concorde avec les observations en laboratoire. Ces résultats indiquent que le niveau de PAX1 dans les cellules tumorales est un facteur critique qui oriente les cellules immunitaires locales vers un rôle protecteur pour la tumeur.
Un seul axe, un double avantage pour la tumeur
Pris ensemble, les données soutiennent un modèle dans lequel un niveau élevé de MEOX1 dans les cellules de glioblastome abaisse PAX1, conférant à la tumeur un double avantage. À l’intérieur des cellules cancéreuses, ce basculement stimule la croissance, la mobilité et la résistance à la mort cellulaire. À l’extérieur, il favorise la conversion de lymphocytes ordinaires en Tregs qui s’installent dans l’environnement tumoral et atténuent les attaques immunitaires. De cette manière, l’axe MEOX1–PAX1 relie le moteur interne de l’agressivité tumorale à la couche externe d’immunosuppression, créant un système étroitement lié qui favorise la survie de la tumeur.
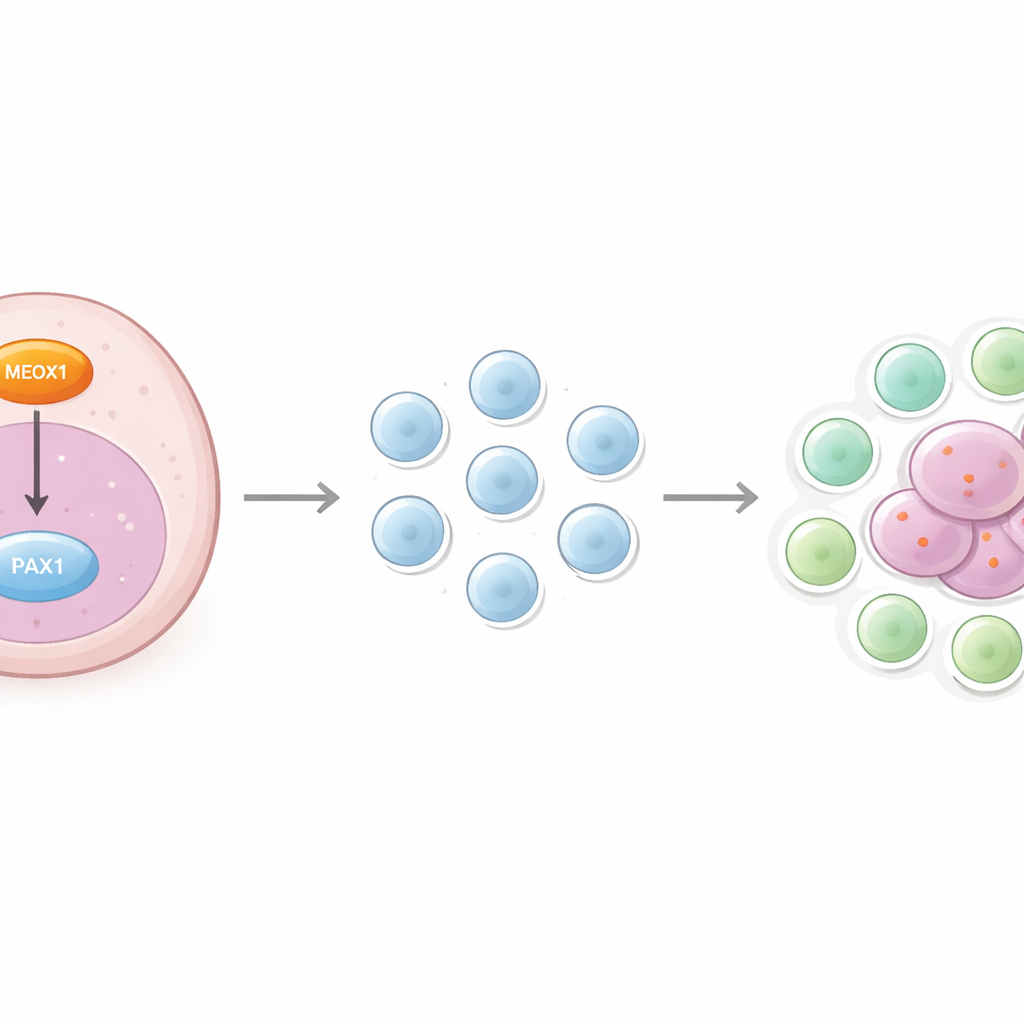
Ce que cela pourrait signifier pour les traitements futurs
Pour les personnes confrontées au glioblastome, ces résultats mettent en évidence une idée thérapeutique prometteuse : cibler l’axe MEOX1–PAX1 afin d’atteindre à la fois la tumeur et son bouclier immunitaire. Des médicaments bloquant MEOX1 ou restaurant l’activité de PAX1 pourraient ralentir la croissance tumorale tout en réduisant le nombre de Tregs dans le microenvironnement tumoral, rendant potentiellement les traitements existants, y compris les immunothérapies, plus efficaces. Bien que ces résultats proviennent d’expériences sur cellules et tissus et doivent encore être testés chez des organismes vivants, ils offrent une carte plus claire de la manière dont le glioblastome déjoue le système immunitaire — et indiquent de nouvelles voies pour rééquilibrer la situation en faveur du patient.
Citation: Pan, P., Wang, R., Lv, P. et al. The MEOX1-PAX1 axis coordinately regulates tumor cell malignancy and Treg differentiation in glioblastoma. Sci Rep 16, 9136 (2026). https://doi.org/10.1038/s41598-026-40453-2
Mots-clés: glioblastome, microenvironnement tumoral, cellules T régulatrices, immunosuppression tumorale, voies de signalisation du cancer