Clear Sky Science · fr
Porteurs nanométriques en ferrite recouverts de chitosane sensibles aux stimuli pour la délivrance ciblée de capsaïcine et une bioactivité sélective dépendant du cœur sur les cellules HepG2
Une épice au pouvoir caché
Les piments apportent plus que de la chaleur à nos plats : leur brûlure provient de la capsaïcine, un composé naturel qui peut aussi tuer des cellules cancéreuses. Pourtant, l’utilisation de la capsaïcine comme médicament reste difficile car elle se dissout mal dans l’eau, disparaît rapidement de l’organisme et irrite les tissus sains à fortes doses. Cette étude explore une façon de dompter cette molécule brûlante en l’enfermant dans de minuscules particules intelligentes capables de transporter la capsaïcine en toute sécurité dans la circulation et de la libérer principalement à l’intérieur des tumeurs hépatiques.
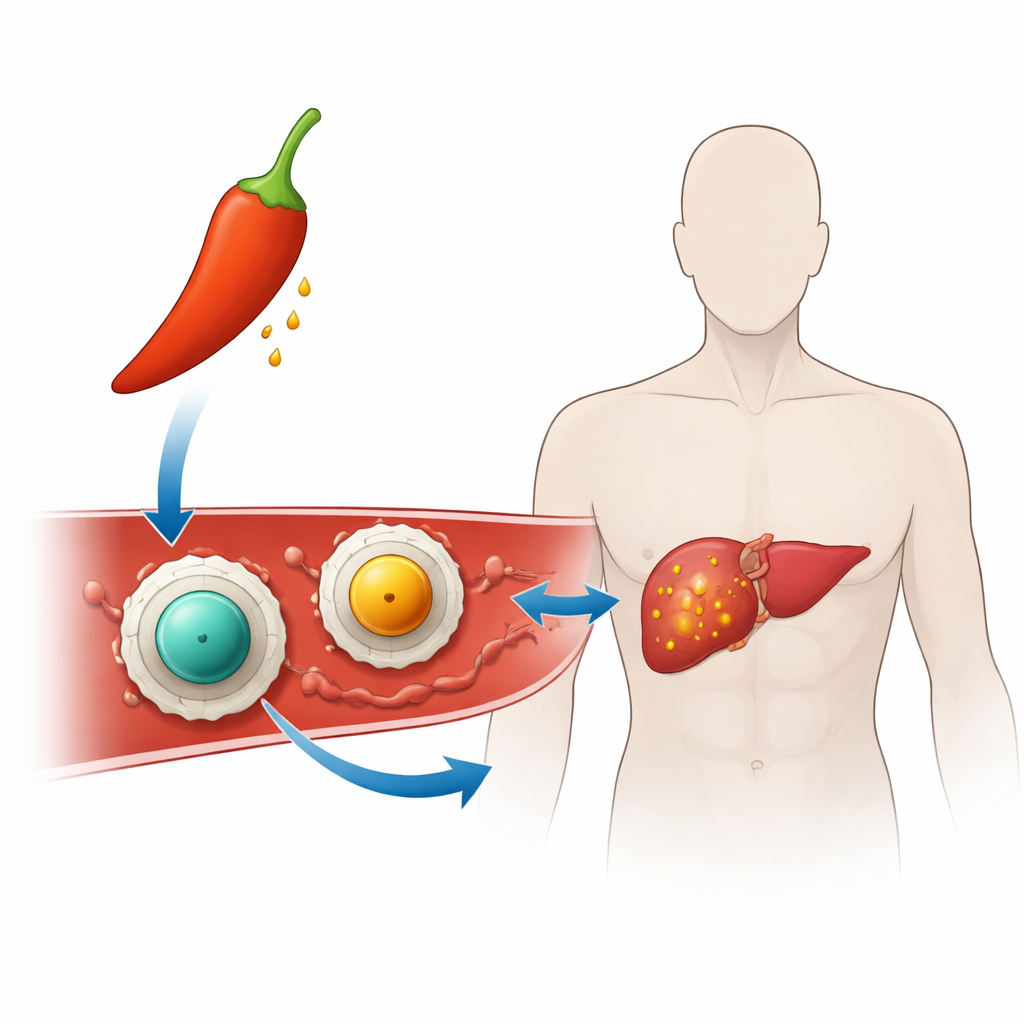
Transformer le piment en thérapie ciblée
Les chercheurs ont construit des « nanovecteurs » – des particules des milliers de fois plus petites qu’un grain de sable – pour acheminer la capsaïcine vers les cellules cancéreuses. Chaque nanovecteur possède un cœur solide composé d’un minéral magnétique appelé ferrite (soit ferrite de zinc soit ferrite de manganèse) enveloppé d’une fine couche de chitosane, une substance sucre-like dérivée de crustacés déjà utilisée en médecine et dans l’alimentation. Ce revêtement facilite la suspension des particules dans l’eau et favorise leur adhérence aux surfaces cellulaires et à l’ADN, ce qui est important pour l’activité anticancéreuse. En chargeant la capsaïcine dans cette enveloppe de chitosane, l’équipe espérait stabiliser le médicament et le garder dissimulé jusqu’à ce qu’il atteigne l’environnement agressif à l’intérieur d’une tumeur.
Libération intelligente dans les conditions tumorales
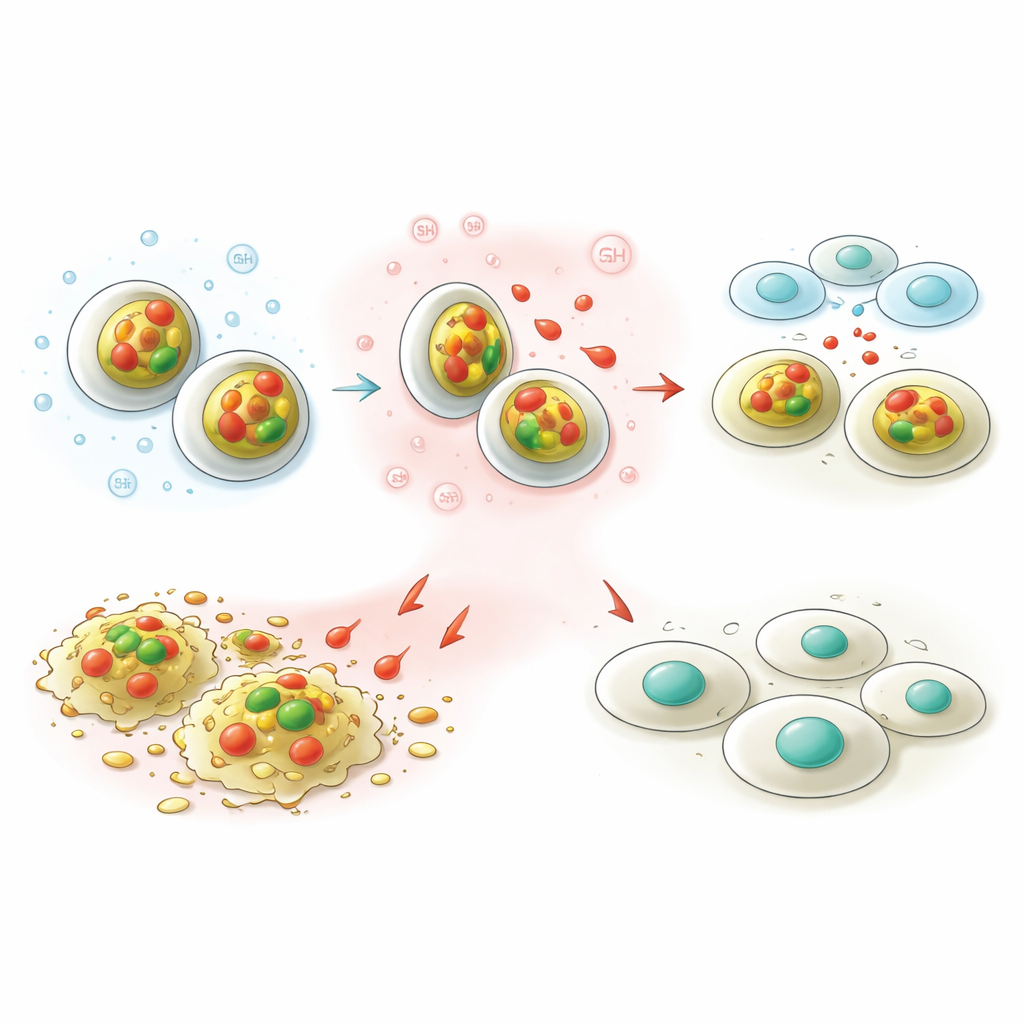
Une caractéristique clé des tumeurs est qu’elles sont souvent plus acides et riches en certains antioxydants, comme le glutathion, que les tissus sains. L’équipe a conçu ses nanovecteurs pour détecter ces conditions. Dans des tests en laboratoire à un pH sanguin normal, moins de 10 % de la capsaïcine stockée s’est échappée en deux jours, ce qui suggère que les particules transporteraient leur cargaison en toute sécurité pendant la circulation. Dans des conditions imitant la tumeur – plus acides et avec un glutathion abondant – les particules ont libéré environ un tiers de leur capsaïcine. Ce comportement « marche–arrêt » signifie que le médicament a plus de chances d’être déchargé à l’intérieur des cellules cancéreuses plutôt qu’en chemin, ce qui peut augmenter l’efficacité tout en réduisant les effets secondaires.
Comment la composition des particules influence sécurité et performance
Bien que les deux nanovecteurs paraissent similaires de loin, leurs cœurs internes faisaient une vraie différence. Les particules à base de zinc avaient tendance à être plus petites et à retenir la capsaïcine plus fermement, tandis que celles à base de manganèse étaient plus poreuses et laissaient le médicament s’échapper plus facilement. Les deux types présentaient une forte charge de surface positive, ce qui favorise leurs interactions avec les surfaces négativement chargées des cellules et de l’ADN. Des essais sur le sang humain ont montré de faibles dommages aux globules rouges, et les particules vides étaient peu agressives pour des cellules pulmonaires normales, soutenant leur sécurité de base. Lorsqu’ils étaient chargés en capsaïcine, les deux systèmes devenaient plus puissants contre les cellules cancéreuses du foie, mais la version à base de manganèse trouvait le meilleur compromis : elle nuisait davantage aux cellules cancéreuses tout en restant relativement douce pour les cellules normales.
Au-delà du cancer : effets protecteurs supplémentaires
Les nanovecteurs ont fait plus que délivrer la capsaïcine. Ils ont aussi ralenti la croissance de plusieurs bactéries pathogènes aussi efficacement qu’un antibiotique standard dans certains tests, et ils ont aidé à neutraliser les radicaux libres nocifs, liés à l’inflammation et aux dommages tissulaires. Des mesures optiques précises ont montré qu’une fois la capsaïcine encapsulée dans les particules ferrite–chitosane, elle se liait à l’ADN de façon plus forte et plus stable. Des expériences cinétiques rapides ont révélé une danse en deux étapes : l’ADN s’accroche d’abord à la surface positivement chargée de la particule, puis le complexe se réarrange en une association plus serrée et durable. Ces interactions renforcées expliquent probablement pourquoi les particules chargées présentent des effets anticancéreux, antibactériens et antioxydants plus marqués que la capsaïcine ou les particules de ferrite seules.
Ce que cela pourrait signifier pour les patients
Pour l’instant, ces résultats proviennent de boîtes de laboratoire, pas de patients. Néanmoins, ils suggèrent que des nanovecteurs soigneusement conçus peuvent transformer un ingrédient alimentaire épicé en une arme anticancéreuse plus précise. En choisissant le bon matériau de cœur et de revêtement, les chercheurs ont créé de minuscules paquets qui maintiennent la capsaïcine stable, la transportent en toute sécurité dans le sang et la déchargent de préférence dans des conditions similaires à celles des tumeurs, en particulier dans les cellules du cancer du foie. Parmi les architectures testées, les particules à base de manganèse offraient le mélange le plus prometteur d’action anticancéreuse ciblée, de faible toxicité pour les cellules normales et d’avantages antibactériens et antioxydants supplémentaires. Avec des études animales et des évaluations de sécurité complémentaires, de telles particules « intelligentes » inspirées du piment pourraient un jour contribuer à des thérapies plus douces et plus ciblées contre le cancer du foie et potentiellement d’autres maladies.
Citation: Bakr, E., Elshami, F.I., Okba, E.A. et al. Stimuli-responsive chitosan-coated ferrite nanocarriers for targeted capsaicin delivery and core-dependent HepG2-selective bioactivity. Sci Rep 16, 8957 (2026). https://doi.org/10.1038/s41598-026-40433-6
Mots-clés: capsaïcine, cancer du foie, nanoparticules, administration ciblée de médicaments, vecteurs sensibles aux stimuli