Clear Sky Science · fr
L’effet d’un surcroît de charge pondérale sur le poids corporel dépend en partie de Piezo1 dans les cellules de la lignée ostéoblastique et du signal TrkA
Pourquoi un poids supplémentaire pourrait aider à combattre l’obésité
La plupart d’entre nous considèrent un surpoids comme quelque chose à éviter, mais que se passerait-il si ajouter soigneusement du poids pouvait en fait aider l’organisme à perdre de la graisse ? Cette étude explore un système intégré de détection du poids dans les os qui semble informer le cerveau lorsque le corps est trop lourd, l’incitant à brûler de la graisse. En révélant comment ce système fonctionne au niveau cellulaire, les chercheurs ouvrent des pistes pour des traitements qui réduiraient la masse grasse tout en préservant la masse musculaire précieuse.
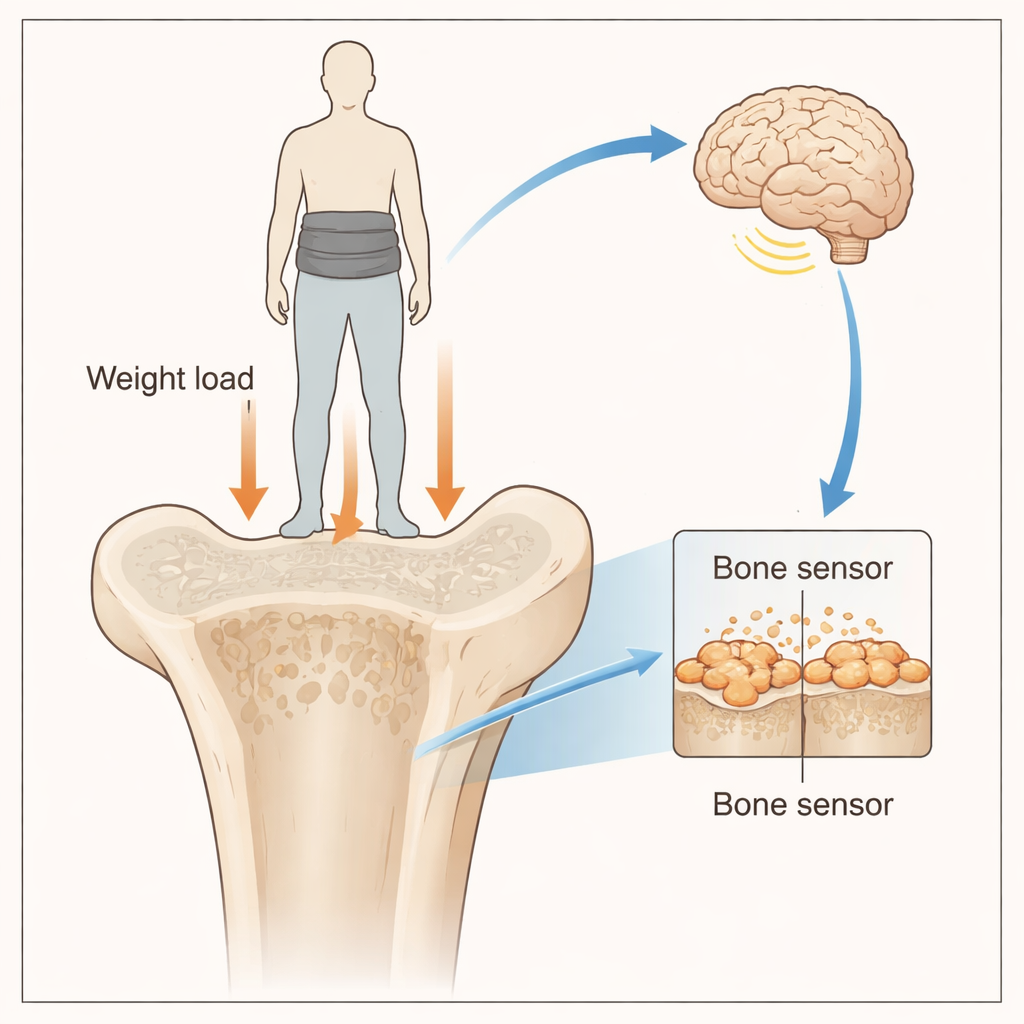
Une balance cachée dans vos os
L’obésité est associée au diabète, aux maladies cardiovasculaires et à plusieurs cancers, et même les médicaments amaigrissants les plus récents entraînent souvent une perte à la fois de graisse et de muscle. C’est un problème sérieux pour les personnes atteintes d’« obésité sarcopénique », qui ont déjà des muscles fragiles. Des essais antérieurs chez l’humain ont montré que le simple port d’un gilet lesté pendant plusieurs semaines peut diminuer la graisse corporelle sans réduire la masse musculaire. Des travaux antérieurs sur des animaux ont conduit les auteurs à proposer que les os des pattes contiennent une sorte de « balance gravitationnelle » interne qui détecte le poids du corps et contribue à maintenir la masse grasse sous contrôle. Mais les molécules responsables de cette détection restaient inconnues.
Tester le capteur de poids osseux chez des souris obèses
Pour enquêter, les chercheurs ont utilisé des souris rendues obèses par un régime riche en graisses, puis ont implanté chirurgicalement de petites capsules dans leur abdomen. Dans un groupe, la capsule était remplie d’un matériau lourd, ajoutant environ 15 % au poids corporel ; chez les souris témoins, la capsule était presque sans poids. Après l’intervention, les scientifiques ont soustrait le poids de la capsule à chaque mesure afin de suivre l’évolution réelle du poids corporel. Ils ont aussi prélevé un dépôt graisseux spécifique — le tissu adipeux blanc rétro-péritonéal — dans l’abdomen à la fin de l’expérience pour mesurer la perte de graisse.
Un canal sensible à la pression dans les cellules osseuses
L’équipe s’est d’abord concentrée sur Piezo1, un canal protéique de la membrane cellulaire qui s’ouvre lorsque les cellules sont étirées ou comprimées mécaniquement. Grâce à l’ingénierie génétique, ils ont supprimé Piezo1 uniquement dans les cellules précoce de formation osseuse (cellules de la lignée ostéoblastique) qui expriment un marqueur appelé Runx2, principalement présentes dans les os longs des pattes. Des analyses microscopiques détaillées ont confirmé que Piezo1 était fortement réduit dans ces cellules osseuses mais restait présent dans le muscle voisin, montrant que la suppression était spécifique. Chez les souris obèses ayant un Piezo1 normal, l’ajout de poids entraînait une baisse marquée du poids corporel global et une forte réduction de la graisse abdominale. En revanche, les souris dépourvues de Piezo1 dans les cellules de la lignée osseuse affichaient une réponse beaucoup plus faible : leur poids et leur graisse abdominale diminuaient à peine sous la charge supplémentaire. Cela indique que Piezo1 dans les cellules osseuses est une composante clé du système de détection du poids.
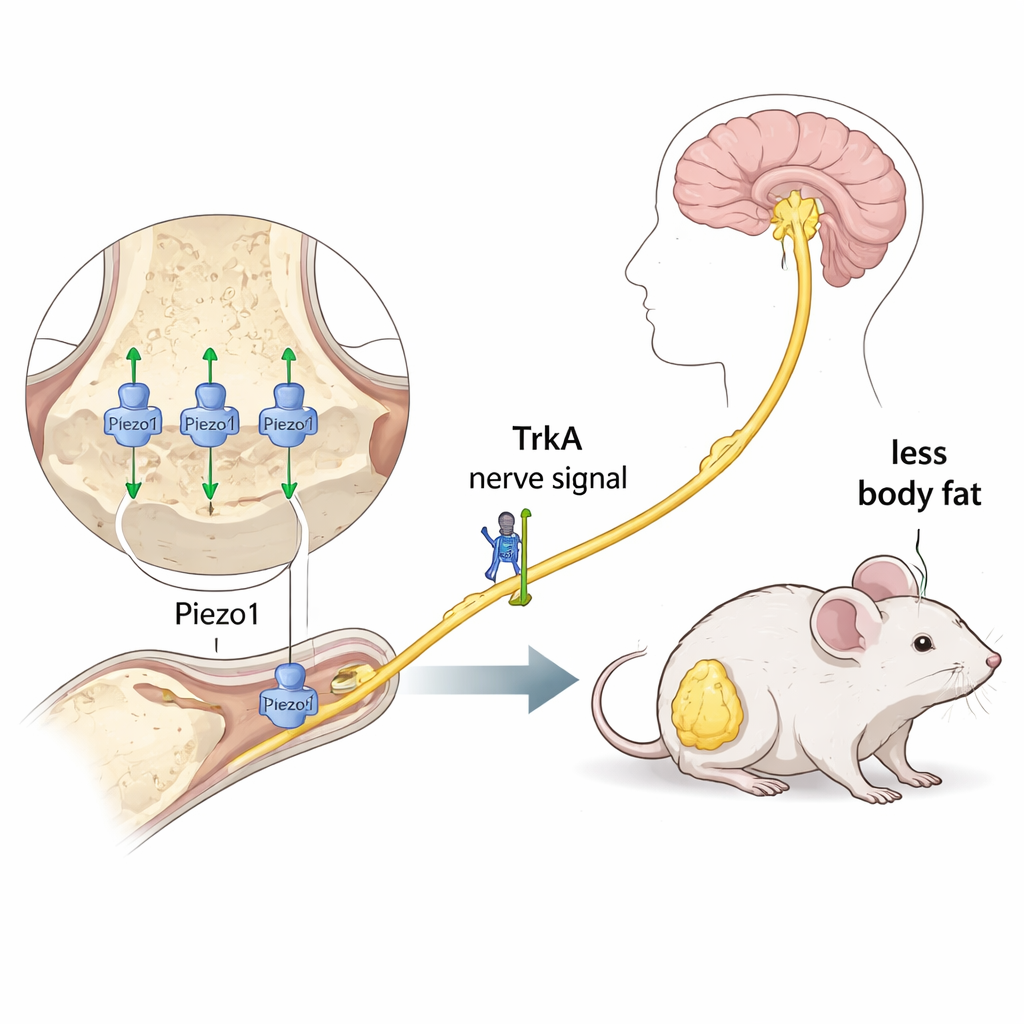
Des signaux nerveux qui transmettent le message au cerveau
Ensuite, les scientifiques ont examiné un second acteur : TrkA, un récepteur principalement présent sur certaines fibres nerveuses qui répondent au facteur de croissance nerveuse (NGF). TrkA aide les nerfs à croître et à transmettre la douleur et d’autres signaux. En utilisant une souche de souris spéciale, l’équipe a pu couper la signalisation TrkA dans tout l’organisme en ajoutant une petite molécule, le 1NM-PP1, à l’eau de boisson. Un test classique de douleur par retrait de la queue (« tail-flick ») a confirmé que la signalisation TrkA était bien inhibée : les souris traitées ne devenaient plus hypersensibles à la chaleur après un agent de type NGF. Lorsque ces souris ont été soumises à une augmentation de la charge pondérale, les animaux ayant une signalisation TrkA normale ont perdu un poids corporel et une graisse abdominale significatifs, mais les souris avec TrkA bloqué ont présenté une réponse beaucoup plus faible et statistiquement moins robuste. Fait intéressant, le poids ajouté n’a pas déclenché une croissance évidente de nouvelles fibres nerveuses autour de l’os, ce qui suggère que ce sont les nerfs existants, plutôt que les nouvelles pousses, qui véhiculent le signal.
Ce que cela signifie pour les futurs traitements de l’obésité
Pris ensemble, les résultats soutiennent un modèle dans lequel un excès de poids corporel — qu’il provienne de la graisse ou d’une charge ajoutée — comprime les os des pattes. Les cellules de la lignée osseuse détectent cette pression via le canal Piezo1, puis communiquent via des voies nerveuses dépendantes de TrkA vers des centres cérébraux qui régulent l’appétit et la dépense énergétique. Le cerveau, à son tour, contribue à réduire les réserves de graisse tout en épargnant le muscle. Bien que ce travail ait été réalisé chez la souris et utilise des implants chirurgicaux, il aide à expliquer pourquoi quelque chose d’aussi simple que le port d’un gilet lesté peut réduire la graisse corporelle chez l’humain. À long terme, cibler ce circuit os–nerf–cerveau pourrait conduire à de nouvelles thérapies complétant les médicaments actuels en réduisant sélectivement la graisse sans sacrifier le muscle.
Citation: Hägg, D., Li, L., Beeve, A.T. et al. The effect of increased weight loading on body weight is partly dependent on Piezo1 in osteoblast-lineage cells and TrkA signaling. Sci Rep 16, 7162 (2026). https://doi.org/10.1038/s41598-026-40431-8
Mots-clés: obésité, mécanosensation osseuse, Piezo1, signalisation TrkA, charge pondérale