Clear Sky Science · fr
Comportement dépendant de la température des liquides liés par des liaisons hydrogène : rapprocher expériences, dynamique moléculaire et DFT
Pourquoi les liquides chauds et froids se comportent si différemment
Quiconque a essayé de verser du sirop froid ou de mélanger des huiles réfrigérées sait que la température peut modifier radicalement la façon dont les liquides coulent et se mélangent. Cette étude examine pourquoi cela se produit dans une famille spécifique de liquides importants industriellement : des mélanges d’un aldéhyde appelé heptanal avec plusieurs alcools étroitement apparentés. En observant ces mélanges à la fois en laboratoire et au niveau moléculaire, les auteurs montrent comment un chauffage modeste réorganise discrètement le réseau invisible d’attractions entre molécules, avec de grandes conséquences pour la densité, l’épaisseur et la facilité d’écoulement. 
Solvants du quotidien avec une poignée de main cachée
Les liquides étudiés ici sont loin d’être exotiques. Les aldéhydes et les alcools sont courants dans les carburants, les parfums, les cosmétiques et les formulations pharmaceutiques. Lorsqu’ils sont mélangés, leurs molécules « se serrent la main » par des attractions directionnelles entre le groupe OH de l’alcool et le groupe carbonyle de l’aldéhyde, formant ce que les chimistes appellent des liaisons hydrogène. Ces liaisons rapprochent les molécules plus qu’un simple mélange ne le prédirait, rendant le mélange légèrement plus compact et plus visqueux qu’un mélange idéal sans interactions. Les chercheurs se sont concentrés sur l’heptanal combiné à des alcools à chaîne droite de 1‑propanol à 1‑heptanol, en posant deux questions clés : comment la température modifie-t-elle ces poignées de main moléculaires, et comment la longueur de la chaîne alkyle de l’alcool influence-t-elle le résultat ?
Mesurer comment les liquides se compactent et s’écoulent
En laboratoire, l’équipe a mesuré avec soin la densité et la viscosité de chaque mélange sur une plage de températures autour et au‑dessus de la température ambiante. Ils ont constaté que tous les mélanges présentent un « volume supplémentaire » négatif lors du mélange, c’est‑à‑dire que le liquide mélangé occupe moins d’espace que la somme des composants pris séparément. En parallèle, les mélanges sont plus visqueux qu’une règle empirique simple ne le prévoirait. Les deux effets sont les plus marqués à basse température et pour l’alcool le plus court, le 1‑propanol, et s’atténuent progressivement lorsque les liquides sont chauffés ou que les chaînes d’alcool s’allongent. Ce schéma indique des attractions fortes et efficaces entre l’heptanal et les alcools courts qui rapprochent les molécules et résistent à l’écoulement, et des interactions plus faibles et plus entravées lorsque la queue de l’alcool devient plus volumineuse.
Observer le mouvement et l’agrégation des molécules
Pour saisir l’histoire microscopique derrière ces mesures, les auteurs ont eu recours à des simulations de dynamique moléculaire et à des calculs de chimie quantique. Des modèles informatiques de milliers de molécules ont révélé la fréquence et la proximité des regroupements entre heptanal et alcools. À basse température, les simulations montrent de nombreuses liaisons hydrogène courtes et bien définies et une structure étroitement compacte avec de petites poches vides entre les molécules. Lorsque la température augmente, ces liaisons deviennent moins fréquentes et légèrement plus longues, les molécules se déplacent plus librement, et les poches vides s’agrandissent et se connectent davantage — preuve directe d’un espace libre accru et d’une diffusion plus rapide. Pour les alcools courts, l’environnement autour de l’heptanal est relativement uniforme, tandis que les alcools plus longs créent une première coquille plus irrégulière, leurs queues volumineuses bloquant partiellement l’accès aux sites de liaison clés. 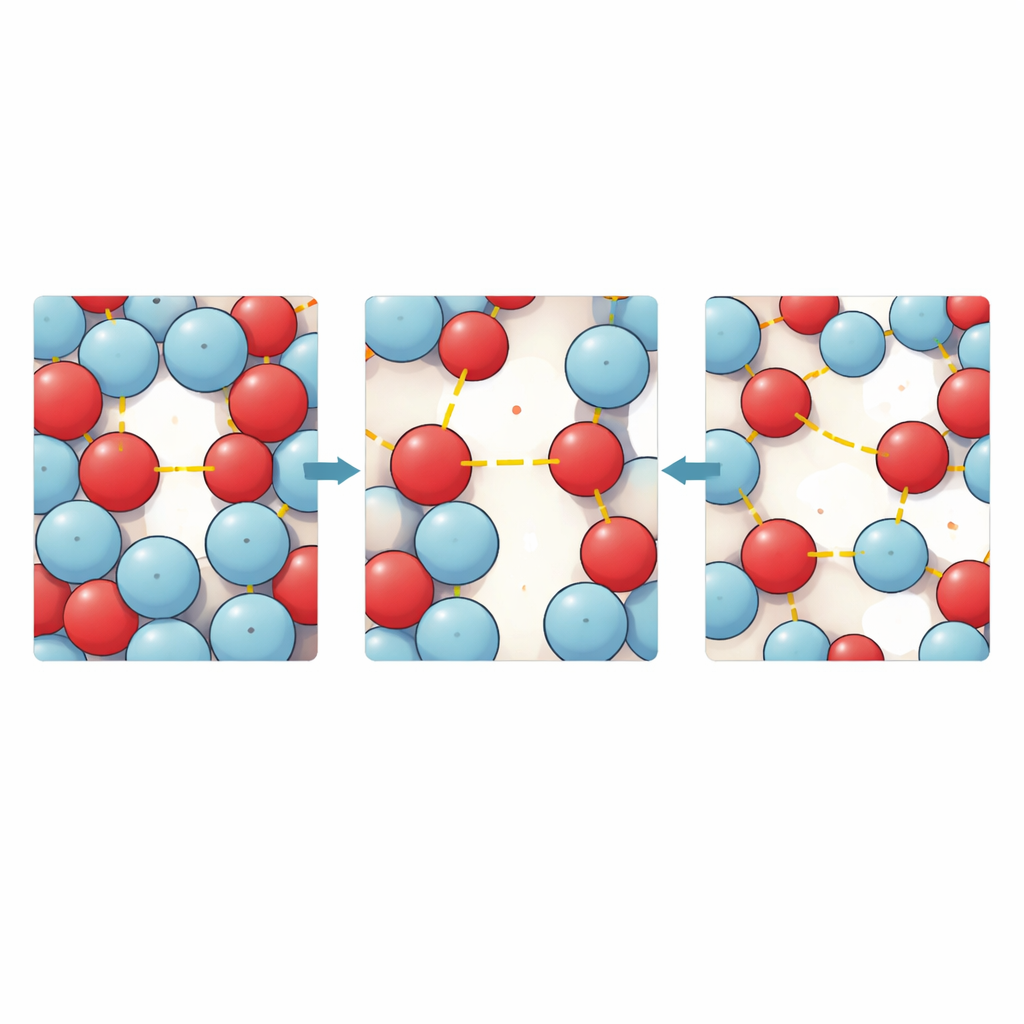
Balancer énergie, ordre et encombrement moléculaire
En analysant comment les arrangements moléculaires évoluent avec la température, l’équipe a pu distinguer les rôles de la stabilisation énergétique et du désordre. La formation de contacts rapprochés entre molécules libère une petite quantité d’énergie, rendant ces interactions favorables, mais elle restreint aussi leur liberté de mouvement et de rotation. Les calculs montrent que, pour ces mélanges, le gain énergétique lié aux liaisons hydrogène compense légèrement la perte de liberté, de sorte que les contacts locaux sont principalement dictés par l’énergie d’attraction avec une pénalité modeste en désordre. Des modèles quantiques de paires simples de molécules confirment que les paires heptanal–alcool sont généralement plus fortement liées que les paires alcool–alcool pour les chaînes courtes, renforçant la liaison mixte et le compactage. Pour l’alcool le plus long étudié, cet avantage disparaît presque, et l’alcool préfère se lier autant avec lui‑même qu’avec l’heptanal, affaiblissant la contraction et l’épaississement spécifiques observés dans les mélanges à chaînes plus courtes.
Ce que cela signifie pour les liquides du monde réel
En termes simples, l’article montre qu’à basse température, l’heptanal et les alcools à chaîne courte s’emboîtent par de nombreuses attractions directionnelles, se tirant en un liquide étroitement compacté et relativement lent. Chauffer le mélange défait ces connexions, ouvre davantage d’espace vide, permet aux molécules de glisser plus aisément les unes sur les autres et rapproche le comportement de celui de liquides ordinaires, moins interactifs. À mesure que les chaînes d’alcool s’allongent, leurs queues volumineuses gênent cet emboîtement soigné, de sorte que la température a un effet plus faible et que les mélanges deviennent globalement moins compacts et moins visqueux. En reliant mesures, simulations et calculs détaillés, l’étude offre un tableau multi‑échelle clair de la façon dont la température et la taille moléculaire modulent le réseau caché de liaisons qui gouverne la compaction, l’écoulement et la réponse des liquides liés par liaisons hydrogène courants dans les procédés industriels.
Citation: Almasi, M., Vatanparast, M. Temperature dependent behavior of hydrogen-bonded liquids: bridging experiments with molecular dynamics and DFT. Sci Rep 16, 9185 (2026). https://doi.org/10.1038/s41598-026-40428-3
Mots-clés: liquides liés par liaisons hydrogène, effets de la température, mélanges aldéhyde–alcool, dynamique moléculaire, viscosité et densité