Clear Sky Science · fr
MOV10, une nouvelle immunothérapie et biomarqueur pronostique, contribue au développement du gliome en régulant l’autophagie
Pourquoi cette étude sur le cancer du cerveau importe
Le glioblastome, une forme agressive de cancer du cerveau, est notoirement difficile à traiter. La plupart des patients ne survivent que quelques mois après le diagnostic, même avec chirurgie, radiothérapie et chimiothérapie. Cette étude se concentre sur une seule molécule, MOV10, anormalement active dans ces tumeurs. En montrant comment MOV10 aide les cellules cancéreuses à croître, échapper au système immunitaire et résister à la mort, les chercheurs identifient une nouvelle cible potentielle pour des thérapies plus efficaces — et un marqueur possible pour prédire l’évolution des patients.
Un complice caché des tumeurs cérébrales mortelles
L’équipe a commencé par exploiter de grandes bases de données publiques sur le cancer contenant des informations génétiques et cliniques de centaines de personnes atteintes de gliome, un groupe large de tumeurs cérébrales incluant le glioblastome. Ils ont découvert que MOV10, une protéine impliquée dans le traitement de l’ARN à l’intérieur des cellules, est surexprimée dans les tissus de gliome par rapport au cerveau normal. Les patients dont les tumeurs produisaient plus de MOV10 avaient tendance à vivre moins longtemps, et ce lien persistait après prise en compte de l’âge, du grade tumoral et des caractéristiques génétiques clés. À partir de ces facteurs, les chercheurs ont construit un modèle mathématique montrant que le niveau de MOV10 peut aider à prédire les chances de survie d’un patient, suggérant que MOV10 pourrait servir de biomarqueur pronostique.
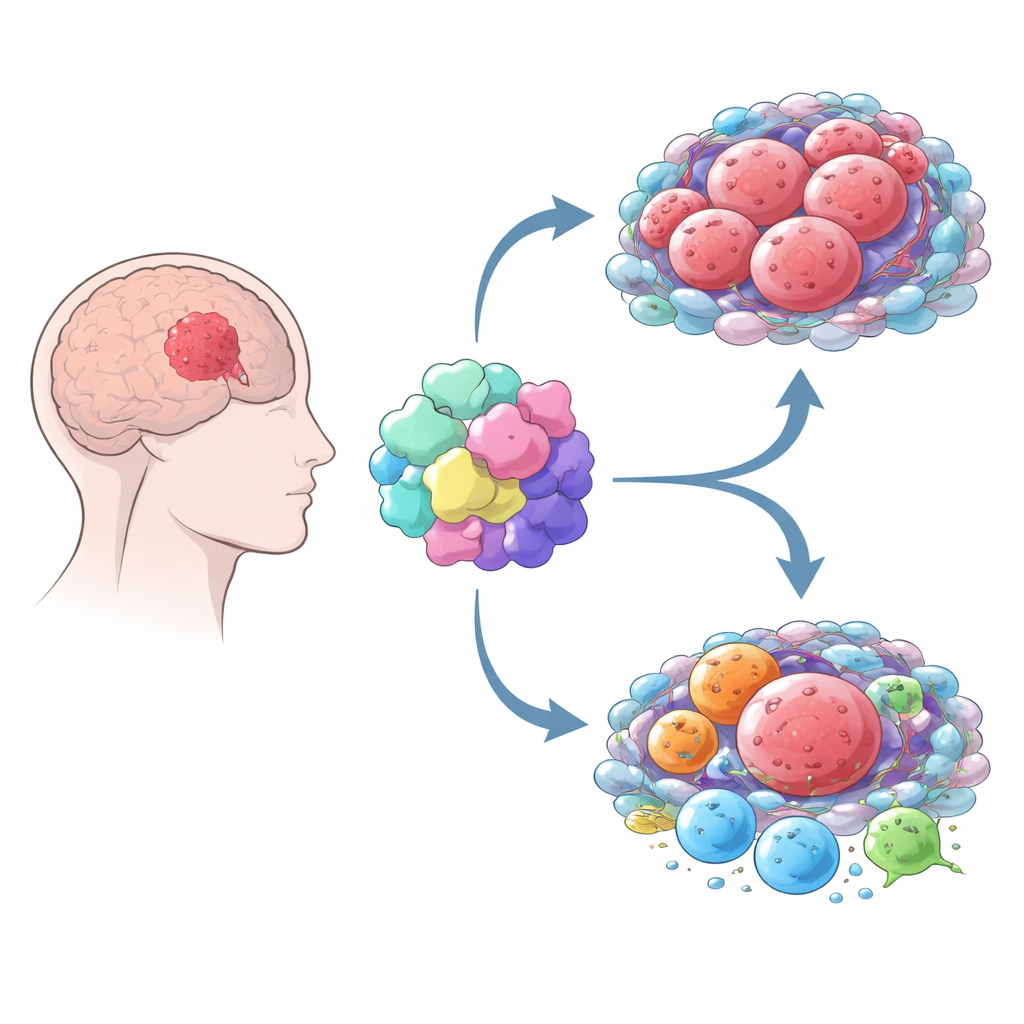
Comment MOV10 remodèle le « quartier » tumoral
Le cancer ne se développe pas en isolation — il détourne le « quartier » environnant constitué de cellules immunitaires et de cellules de soutien. En combinant plusieurs outils computationnels, les auteurs ont montré que les gliomes à forte expression de MOV10 sont entourés d’un mélange plus riche de cellules immunitaires et stromales que les tumeurs à faible MOV10. Mais il ne s’agit pas d’une attaque immunitaire efficace. Au contraire, les tumeurs à fort MOV10 contiennent davantage de macrophages, en particulier d’un sous-type souvent appelé M2, qui soutient typiquement la croissance tumorale et calme les réponses immunitaires. Ces tumeurs présentent aussi des signatures plus marquées de lymphocytes T épuisés et une activité accrue des « freins » immunitaires ciblés par des médicaments d’immunothérapie populaires, tels que PD-1 et CTLA-4. Dans l’ensemble, le profil suggère que MOV10 est associé à un environnement immunosuppressif où les défenses de l’organisme sont affaiblies.
Des données massives aux cellules en laboratoire
Pour dépasser les simples corrélations, les chercheurs ont examiné MOV10 directement dans des échantillons de patients et des cellules en culture. Ils ont confirmé que MOV10 est plus abondant dans les tissus de gliome que dans le cerveau normal, et que plusieurs lignées cellulaires de gliome largement utilisées présentent également des niveaux élevés. Lorsqu’ils ont utilisé de petits ARN interférents pour réduire MOV10 dans des cellules de gliome cultivées en boîte, les cellules se sont divisées plus lentement, ont formé moins de colonies et ont perdu une partie de leur capacité à migrer et à envahir à travers des membranes artificielles. Des protéines qui favorisent la progression du cycle cellulaire et l’invasion ont diminué en abondance, soutenant l’idée que MOV10 favorise activement un comportement agressif plutôt que d’être un simple spectateur.
Relier MOV10 aux cellules immunitaires et aux voies d’auto-nettoyage
L’étude a également exploré comment MOV10 interagit avec deux processus clés : le comportement des macrophages associés à la tumeur et le système d’« auto-nettoyage » cellulaire connu sous le nom d’autophagie. Dans des échantillons tumoraux humains, MOV10 a été détecté dans les mêmes régions que des macrophages de type M2. Dans un système de coculture, lorsque les cellules de gliome étaient modifiées pour produire moins de MOV10, moins de macrophages de type M2 ont migré à travers une barrière vers elles, ce qui implique que MOV10 dans les cellules tumorales aide à attirer ou soutenir ces cellules immunitaires pro-tumorales. Parallèlement, des analyses génétiques ont relié MOV10 à plusieurs gènes impliqués dans l’autophagie. En utilisant des marqueurs fluorescents qui éclairent les structures de recyclage cellulaires, l’équipe a montré que la réduction de MOV10 augmentait l’activité autophagique dans les cellules de gliome et déclenchait davantage de mort cellulaire programmée. Des changements dans des protéines emblématiques de l’autophagie et de l’apoptose ont confirmé ces observations.
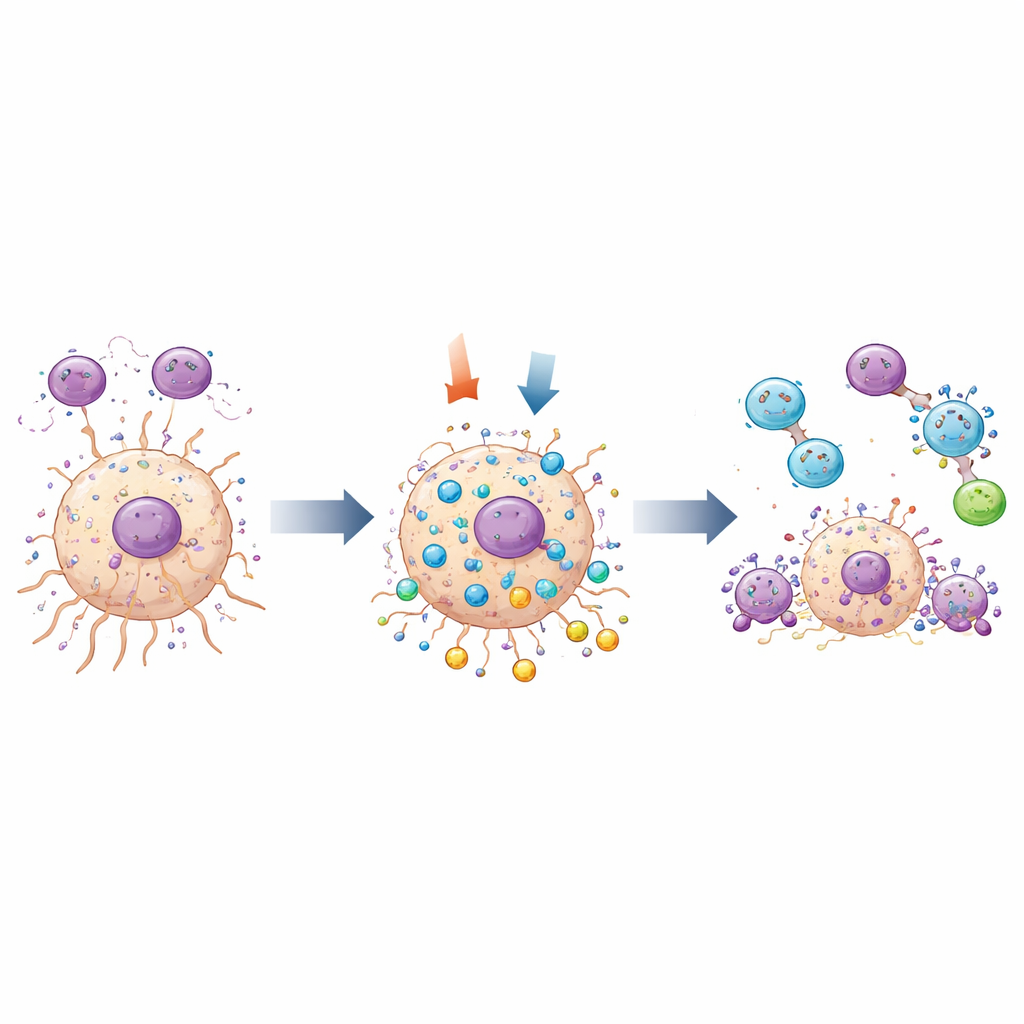
Ce que cela signifie pour les traitements futurs
Pris ensemble, les résultats présentent MOV10 comme un allié multifonctionnel du gliome : il stimule la croissance et l’invasion des cellules tumorales, contribue à construire un microenvironnement immunosuppresseur riche en macrophages favorables à la tumeur, et maintient sous contrôle les systèmes cellulaires d’autodestruction et de recyclage. Lorsque MOV10 est silencé, les cellules de gliome se développent moins, meurent plus facilement et semblent moins aptes à recruter des types de cellules immunitaires délétères. Pour les non-spécialistes, le message clé est que MOV10 est à la fois un « thermomètre » et un « interrupteur » : son niveau dans les tumeurs peut aider à prévoir le pronostic des patients, et le réduire pourrait, en principe, rendre les tumeurs cérébrales plus vulnérables aux traitements. Bien que des études animales supplémentaires et, à terme, des essais cliniques soient nécessaires, MOV10 se distingue désormais comme une cible prometteuse dans la quête de meilleures thérapies contre l’un des cancers cérébraux les plus mortels.
Citation: Wang, F., Ruan, L., Yang, W. et al. MOV10, a novel immunotherapy and prognostic biomarker, contributes to glioma development by regulating autophagy. Sci Rep 16, 9501 (2026). https://doi.org/10.1038/s41598-026-40396-8
Mots-clés: glioblastome, immunothérapie des tumeurs cérébrales, protéine MOV10, microenvironnement tumoral, autophagie et apoptose