Clear Sky Science · fr
Épissage alternatif et expression génique différentielle pendant les variations de la réceptivité endométriale chez des patientes atteintes d’échec d’implantation récurrent
Pourquoi certains embryons ne s’implantent pas
De nombreux couples ayant recours à la fécondation in vitro font face à un mystère décourageant : même lorsque des embryons de haute qualité sont transférés, la grossesse ne se produit pas forcément. Cette étude examine de près la muqueuse utérine — l’endomètre — pour comprendre pourquoi certaines femmes présentent des échecs d’implantation répétés. En analysant la façon dont les gènes sont activés ou désactivés, comment leurs messages sont découpés et réassemblés, et comment se comportent les cellules immunitaires durant la brève fenêtre où l’utérus est prêt à recevoir un embryon, les chercheurs mettent au jour de nouveaux indices moléculaires qui pourraient un jour orienter des tests et traitements plus précis.
La brève fenêtre d’accueil de l’utérus
L’implantation ne peut se produire que durant une courte période de chaque cycle où la muqueuse utérine devient « réceptive ». Les chercheurs ont comparé des échantillons de tissu prélevés chez 90 femmes fertiles et 73 femmes souffrant d’échec d’implantation récurrent, tous pris à trois moments clés : juste avant que la muqueuse ne devienne réceptive, pendant la fenêtre réceptive et peu après sa fermeture. À l’aide du séquençage ARN à haut débit, ils ont mesuré quels gènes étaient actifs et comment leurs messages ARN étaient traités. Ce plan expérimental leur a permis de suivre comment un endomètre sain se prépare à accueillir un embryon et comment cette préparation déraille chez des femmes qui échouent à s’implanter malgré des embryons de bonne qualité. 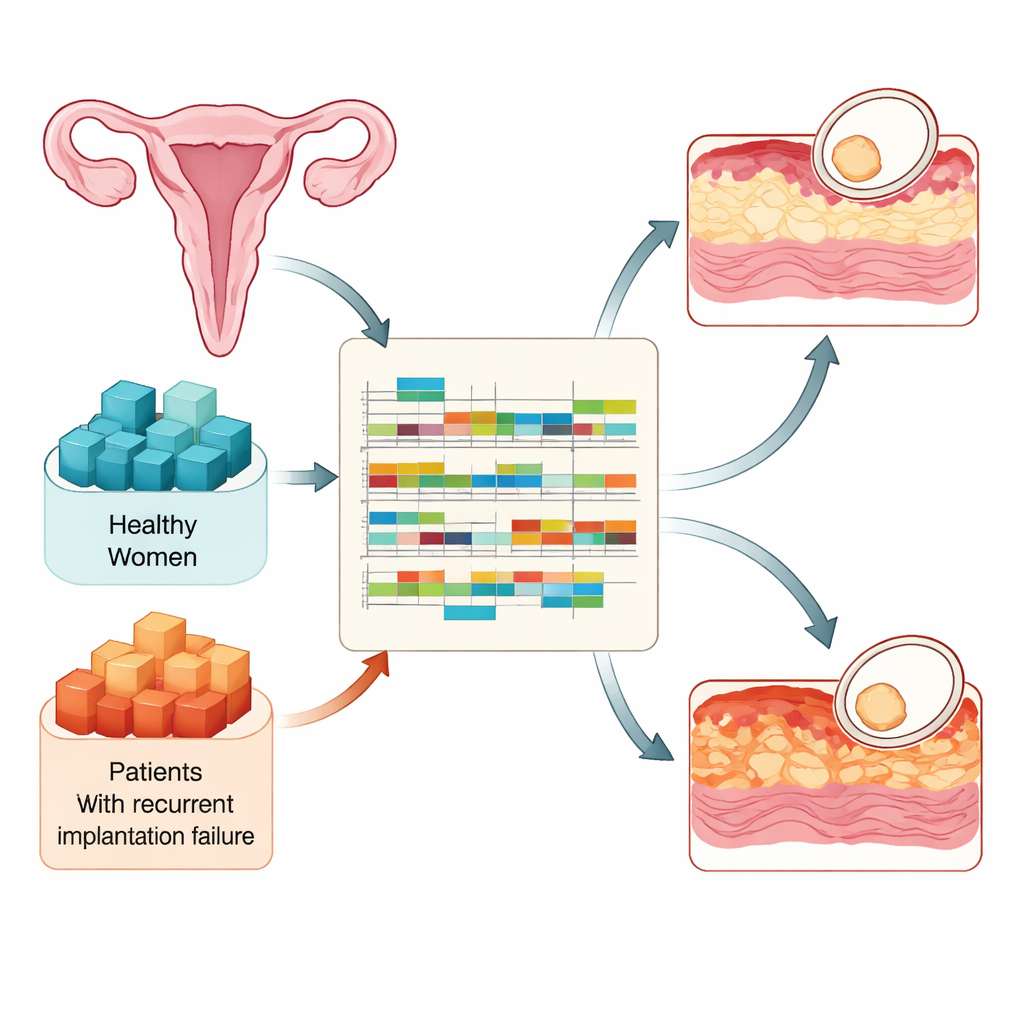
Des messages génétiques coupés et réarrangés
Au‑delà du simple comptage de l’activité génique, l’équipe s’est concentrée sur l’épissage alternatif — le processus par lequel un seul gène peut être découpé en variantes de message différentes, conduisant à des formes protéiques distinctes. Ils ont trouvé plus d’un million d’événements d’épissage au travers des comparaisons, avec deux types — le saut d’exons entiers et le choix entre segments mutuellement exclusifs — particulièrement fréquents. En ne retenant que les changements à la fois fréquents et statistiquement robustes, ils ont observé des centaines à des milliers de modifications d’épissage lorsque la muqueuse passait de la phase non réceptive à la phase réceptive, en particulier de la phase pré‑réceptive vers la fenêtre d’implantation. Nombre de ces changements survenaient même lorsque la quantité totale du gène restait identique, ce qui signifie que la forme de la protéine changeait sans variation de l’activité génique globale.
Cellules adhérant, se remodelant et dialoguant avec le système immunitaire
Les gènes affectés par l’épissage altéré et par les changements d’activité étaient fortement impliqués dans l’adhésion cellulaire, le remaniement du cytosquelette et la transmission de signaux immunitaires. Ces fonctions sont cruciales lorsque l’endomètre se transforme d’une barrière simple en une surface capable d’accueillir et d’ancrer un embryon tout en remodelant les vaisseaux sanguins. Chez les femmes fertiles comme chez celles présentant un échec d’implantation, la phase réceptive s’accompagnait d’un fort remodelage de ces voies, mais les femmes avec échecs récurrents montraient des modifications d’épissage plus fréquentes ou aux schémas différents. Certains des gènes impliqués ont déjà été proposés comme marqueurs de la fenêtre idéale d’implantation, renforçant l’idée que ce n’est pas seulement l’activité génique mais la forme exacte des produits qui définit la réelle préparation de la muqueuse.
Cellules immunitaires et un régulateur clé de l’épissage
L’équipe a aussi estimé les types de cellules immunitaires présentes dans les tissus à partir des mêmes données ARN. Chez les femmes avec échec d’implantation, la phase réceptive montrait moins de lymphocytes T cytotoxiques et de cellules tueuses naturelles au repos, mais davantage de monocytes et de certains macrophages par rapport aux phases antérieures. Plus tard, après la fermeture de la fenêtre, les profils ont de nouveau évolué, avec des changements dans les cellules tueuses naturelles activées et les sous‑types de macrophages. Plusieurs de ces variations de cellules immunitaires suivaient de près des événements d’épissage spécifiques, suggérant un lien entre le remodelage des messages géniques et l’équilibre immunitaire. Parmi les protéines qui contrôlent l’épissage, une nommée KHDRBS3 s’est démarquée comme un nœud central connecté à de nombreux événements modifiés et dont le niveau diminuait systématiquement lorsque la muqueuse devenait réceptive, tant chez les femmes fertiles que chez les patientes concernées. Cela suggère qu’elle pourrait contribuer à entraîner le basculement des modèles d’épissage qui accompagne l’ouverture de la fenêtre d’implantation. 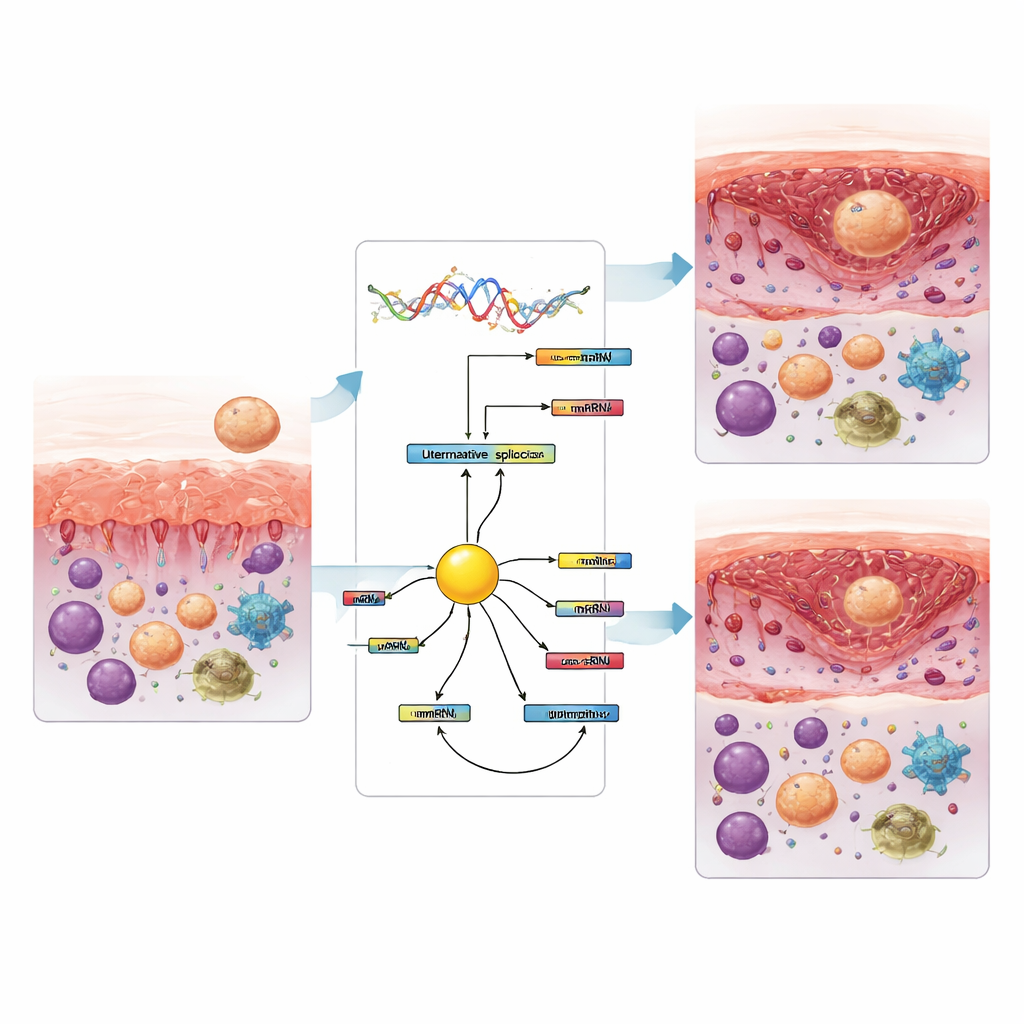
Vers des tests et traitements futurs
Pour traduire ces motifs moléculaires en pistes thérapeutiques, les chercheurs ont cherché si des petites molécules existantes pourraient contrebalancer les signatures d’épissage anormales observées. En confrontant leurs listes de gènes à de larges bases de données de réponses aux médicaments, ils ont identifié plusieurs composés approuvés ou expérimentaux ciblant des gènes liés à l’implantation, y compris des agents modulant les réponses immunitaires ou les voies hormonales. Bien que ces pistes soient encore loin d’une application clinique dans ce contexte, elles fournissent une carte de départ pour des tests en laboratoire.
Ce que cela signifie pour les patientes
Globalement, l’étude montre que l’échec d’implantation n’est pas simplement une question d’avoir les « mauvais » gènes, mais de la manière dont ces gènes sont édités en différents messages et de la façon dont l’environnement immunitaire de l’utérus est modulé dans le temps. Le travail met en lumière KHDRBS3 et des facteurs associés comme régulateurs prometteurs de ce processus et révèle des changements coordonnés des cellules immunitaires qui peuvent soutenir ou entraver la tentative d’un embryon de s’installer. À long terme, ces connaissances pourraient conduire à des tests plus affinés permettant de déterminer le timing et la qualité réels de la fenêtre réceptive d’une femme, ainsi qu’à des traitements ciblés qui ajustent en douceur le façonnage des messages géniques ou l’équilibre immunitaire pour donner aux embryons une meilleure chance de s’implanter.
Citation: Wang, Ml., Lu, Bj., Lu, X. et al. Alternative splicing and differential gene expression during changes in endometrial receptivity in patients with recurrent implantation failure. Sci Rep 16, 9754 (2026). https://doi.org/10.1038/s41598-026-40386-w
Mots-clés: réceptivité endométriale, échec d’implantation récurrent, épissage alternatif, cellules immunitaires utérines, procréation assistée