Clear Sky Science · fr
Trabectedine plus tTF-NGR ciblant le CD13 contre les sarcomes des tissus mous avancés rechutés ou réfractaires : données translationnelles, sécurité clinique et efficacité
Pourquoi cette recherche compte
Les personnes atteintes de sarcomes des tissus mous avancés — des cancers rares qui se développent dans les muscles, les graisses ou d’autres tissus de soutien — manquent souvent d’options thérapeutiques efficaces. Cette étude explore une nouvelle stratégie médicamenteuse en deux temps conçue pour piéger un chimiothérapeutique existant à l’intérieur de la tumeur et couper son apport sanguin, dans l’espoir d’améliorer le contrôle de la maladie tout en maintenant des effets indésirables maîtrisables.
Un cancer rare qui nécessite de meilleures options
Les sarcomes des tissus mous représentent seulement environ 1 % des cancers de l’adulte, mais ils sont souvent agressifs une fois qu’ils se propagent ou qu’ils ne peuvent pas être retirés par chirurgie. La chimiothérapie standard peut ralentir leur progression, mais le pronostic des personnes atteintes d’une maladie avancée reste mauvais. La trabectedine est l’un des principaux médicaments utilisés après l’échec des traitements de première ligne. Elle agit en endommageant l’ADN des cellules cancéreuses et en modifiant également les cellules du microenvironnement tumoral. Malgré cela, de nombreuses tumeurs repoussent finalement, ce qui motive la recherche de moyens pour accroître son impact sans augmenter fortement la toxicité pour les patients.
Un « piège » en deux étapes pour la tumeur
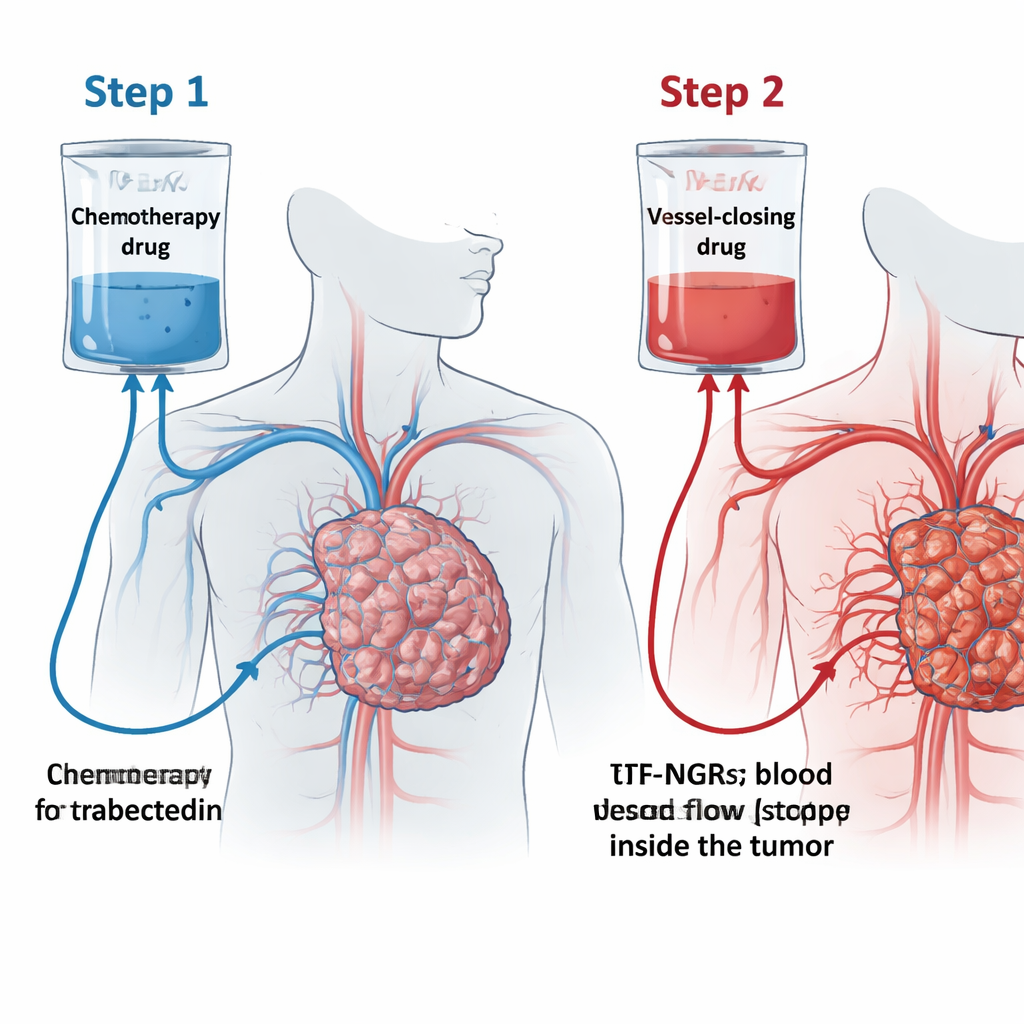
L’équipe a testé un concept qu’elle appelle le « piège trabectedine » (TRABTRAP). D’abord, les patients reçoivent la trabectedine par perfusion de 24 heures. Les deux ou trois jours suivants, ils reçoivent un deuxième médicament, le tTF-NGR. Cette protéine conçue se dirige vers un marqueur nommé CD13, présent principalement sur les vaisseaux sanguins alimentant les tumeurs. Quand le tTF-NGR se fixe à ces vaisseaux, il déclenche une coagulation locale et bloque le flux sanguin, provoquant la nécrose de parties de la tumeur. L’idée est que l’administration de trabectedine en premier lui permet de pénétrer dans la tumeur, puis le tTF-NGR ferme les issues en obstruant les petits vaisseaux tumoraux, piégeant ainsi le médicament là où il est le plus utile et amplifiant l’effet des deux traitements.
Du laboratoire aux premiers essais chez l’humain
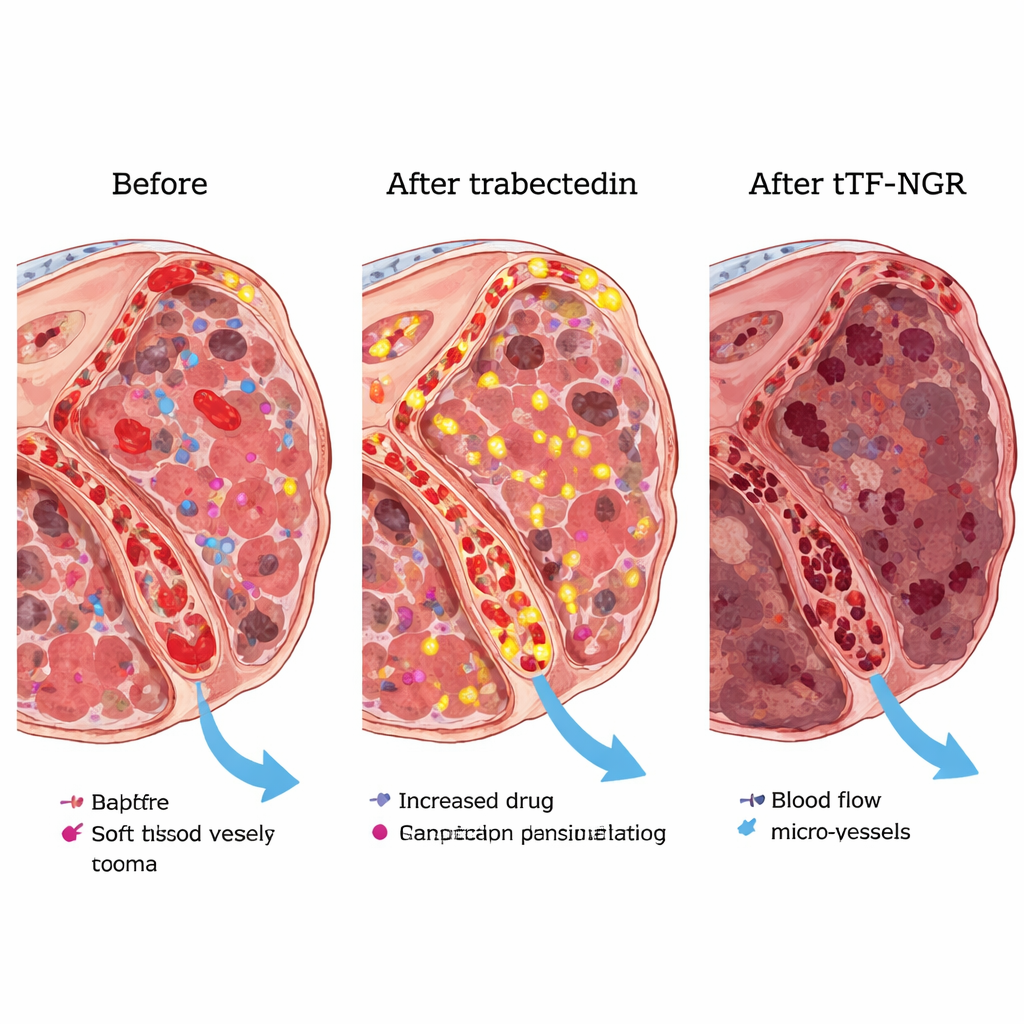
Dans des expériences de laboratoire, les chercheurs ont montré que la trabectedine fait apparaître davantage à la surface des cellules endothéliales des vaisseaux et des cellules de sarcome une certaine molécule lipidique qui favorise la coagulation. Cette modification rendait le tTF-NGR plus efficace pour déclencher une formation locale de caillots sur ces cellules, ce qui est précisément nécessaire pour fermer les vaisseaux tumoraux. Chez des souris porteuses de tumeurs humaines de sarcome, la séquence trabectedine suivie de tTF-NGR réduisait les tumeurs davantage que chaque médicament seul. Parce que les tumeurs animales se dégradaient si complètement sous la combinaison, l’équipe n’a pas pu mesurer de manière fiable combien de trabectedine supplémentaire était piégée, mais le meilleur contrôle tumoral soutenait l’idée de base du « piège ».
Trouver une dose sûre chez de vrais patients
Le cœur de cet article est la phase d’initiation de sécurité de l’essai TRABTRAP menée chez 19 personnes atteintes de sarcomes des tissus mous avancés et fortement prétraités. Tous les patients ont reçu la dose standard de trabectedine. Le second médicament, le tTF-NGR, a été démarré à la dose la plus élevée précédemment tolérée en monothérapie, puis réduit progressivement lorsque des effets indésirables graves sont apparus. À des doses élevées, certains patients ont présenté des problèmes cardiaques ou thrombotiques significatifs, tels qu’une atteinte silencieuse du muscle cardiaque détectée sur des analyses sanguines, de petits emboles pulmonaires ou des thromboses veineuses profondes. Ces événements étaient réversibles avec un traitement et l’arrêt ou la réduction du tTF-NGR, mais ils ont indiqué la nécessité d’abaisser les doses. À 0,5 mg/m² de tTF-NGR administré pendant deux jours après la trabectedine, six patients ont complété au moins deux cycles sans toxicités limitantes de dose, et certains ont poursuivi jusqu’à 14 cycles.
Premiers signes d’efficacité et interaction des médicaments
Bien que cette phase de l’étude soit trop petite pour prouver une efficacité, les résultats étaient encourageants. Parmi les 19 patients, la plupart ont obtenu au moins un contrôle temporaire de la maladie, et deux ont présenté une réduction partielle nette de leurs tumeurs. Chez les personnes atteintes de liposarcome ou de léiomyosarcome — deux sous-types courants pour la trabectedine — près des deux tiers présentaient une maladie stable ou des réponses partielles au premier bilan majeur. Des IRM détaillées chez un patient ont confirmé que le tTF-NGR à la dose choisie pouvait réduire sélectivement le flux sanguin au sein des foyers tumoraux. Les analyses sanguines ont montré que, lorsqu’il était administré après la trabectedine, le tTF-NGR demeurait plus longtemps en circulation et semblait plus actif que lorsqu’il était utilisé seul, ce qui aide à expliquer pourquoi la dose sûre en combinaison est plus faible que celle en monothérapie.
Que signifie cela pour les patients
Pour les personnes confrontées à un sarcome des tissus mous avancé, TRABTRAP représente une tentative soigneusement conçue d’optimiser un chimiothérapeutique existant en l’associant à un agent occlusif vasculaire ciblant l’apport sanguin de la tumeur. La phase d’initiation de sécurité montre qu’à des doses ajustées, cette combinaison peut être administrée de façon répétée, avec des effets indésirables significatifs mais généralement gérables et réversibles sous surveillance étroite. S’il est encore trop tôt pour dire si cela prolongera la survie ou réduira systématiquement les tumeurs, le contrôle tumoral précoce prometteur et les effets clairs sur la perfusion tumorale justifient de passer à un essai randomisé plus large. Si les résultats futurs sont positifs, cette approche en deux étapes pourrait ouvrir une nouvelle voie pour traiter les sarcomes et inspirer des stratégies similaires pour d’autres cancers difficiles à traiter.
Citation: Hessling, K., Brand, C., Schwöppe, C. et al. Trabectedin plus CD13-targeted tissue factor tTF-NGR against advanced relapsed or refractory soft tissue sarcoma: translational data, clinical safety and efficacy. Sci Rep 16, 7389 (2026). https://doi.org/10.1038/s41598-026-40362-4
Mots-clés: sarcome des tissus mous, trabectedine, vaisseaux tumoraux, thérapie de coagulation ciblée, chimiothérapie combinée