Clear Sky Science · fr
Sélection adaptative d’exemples pour une détection explicable des mitoses basée sur des prototypes en pathologie numérique
Pourquoi cela importe pour la prise en charge du cancer
Lorsque les pathologistes examinent des échantillons tumoraux au microscope, compter le nombre de cellules tumorales en division aide à évaluer l’agressivité de la tumeur et à choisir les traitements. L’intelligence artificielle peut désormais repérer rapidement ces cellules en division dans des lames numérisées, mais ses décisions restent souvent opaques même pour des experts. Cet article présente une méthode appelée Sélection Adaptative d’Exemples (AES) qui permet à un système d’IA de « montrer son raisonnement » en mettant en avant des cas réels passés qui appuient ou contredisent chaque décision, rendant la détection automatisée des mitoses plus transparente et dignes de confiance en contexte clinique.
Le défi de repérer les cellules en division
Les cellules tumorales en division, appelées figures mitotiques, sont petites, rares et visuellement hétérogènes. Avec la coloration rose-violet habituelle, elles peuvent ressembler fortement à des structures inoffensives comme des cellules en apoptose ou certains éléments du système immunitaire. Les experts humains doivent parcourir de vastes lames numériques pour les trouver, un processus lent, fatigant et sujet à désaccords. Les systèmes modernes d’apprentissage profond peuvent égaler ou dépasser la performance des spécialistes sur cette tâche, mais ils fonctionnent comme des boîtes noires : ils produisent un score pour chaque cellule suspecte sans expliquer clairement pourquoi. En médecine, où les décisions thérapeutiques peuvent changer une vie, ce manque de clarté est un obstacle sérieux à l’adoption de l’IA au quotidien.
Construire un détecteur performant mais opaque
Les auteurs entraînent d’abord un réseau de détection d’objets à la pointe, basé sur l’architecture Faster R-CNN, pour repérer les figures mitotiques dans un large jeu de données diversifié appelé MIDOG++. Ces images proviennent de tumeurs humaines et canines, couvrant plusieurs types de cancers et laboratoires, et comprennent plus de onze mille cellules en division annotées avec soin. Pour préserver les détails fins, les lames sont découpées en petits patchs et fortement augmentées pour reproduire les variations réelles de coloration et d’imagerie. Le détecteur obtenu atteint des performances solides selon les types tumoraux, avec des scores F1 allant jusqu’à 0,84, ce qui confirme sa précision mais aussi sa complexité — exactement le type de système qui nécessite une meilleure explication avant que les cliniciens puissent lui faire confiance.
Apprendre à l’IA à s’expliquer avec des exemples
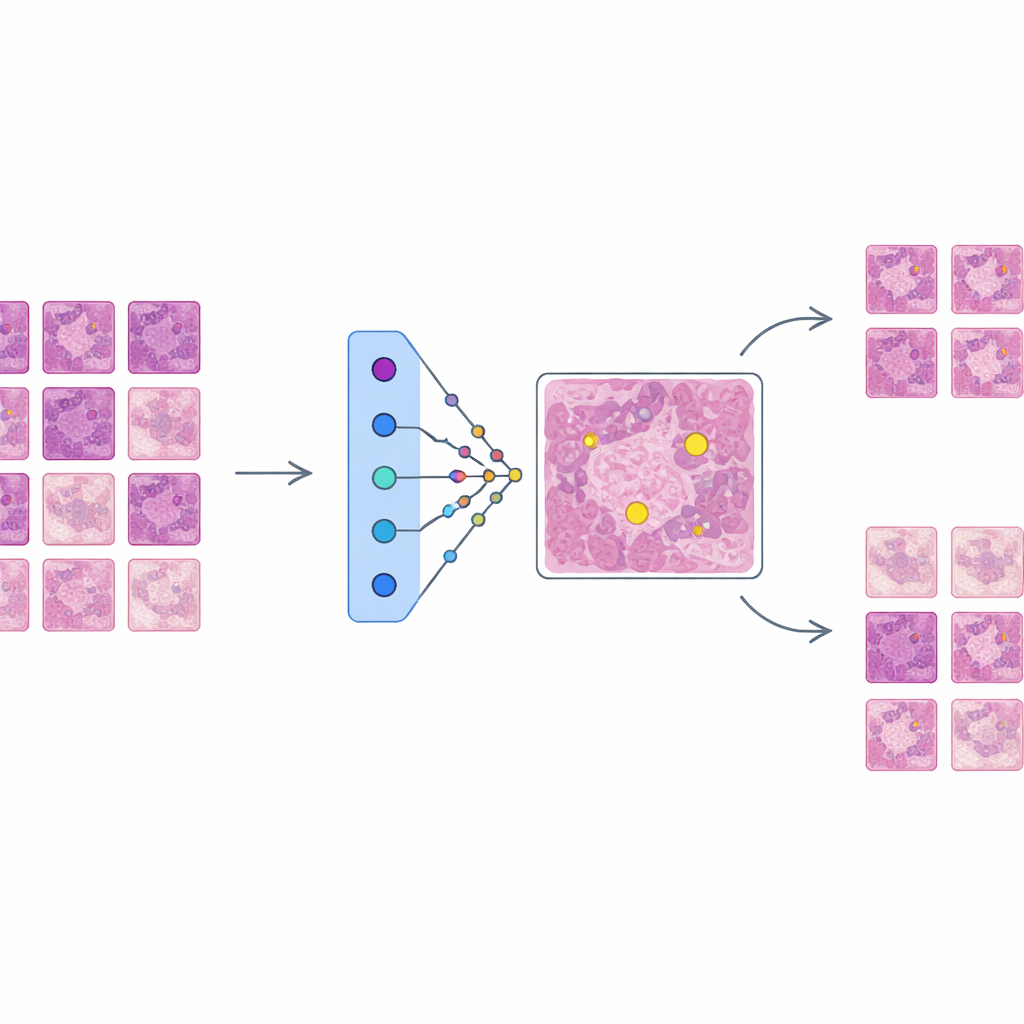
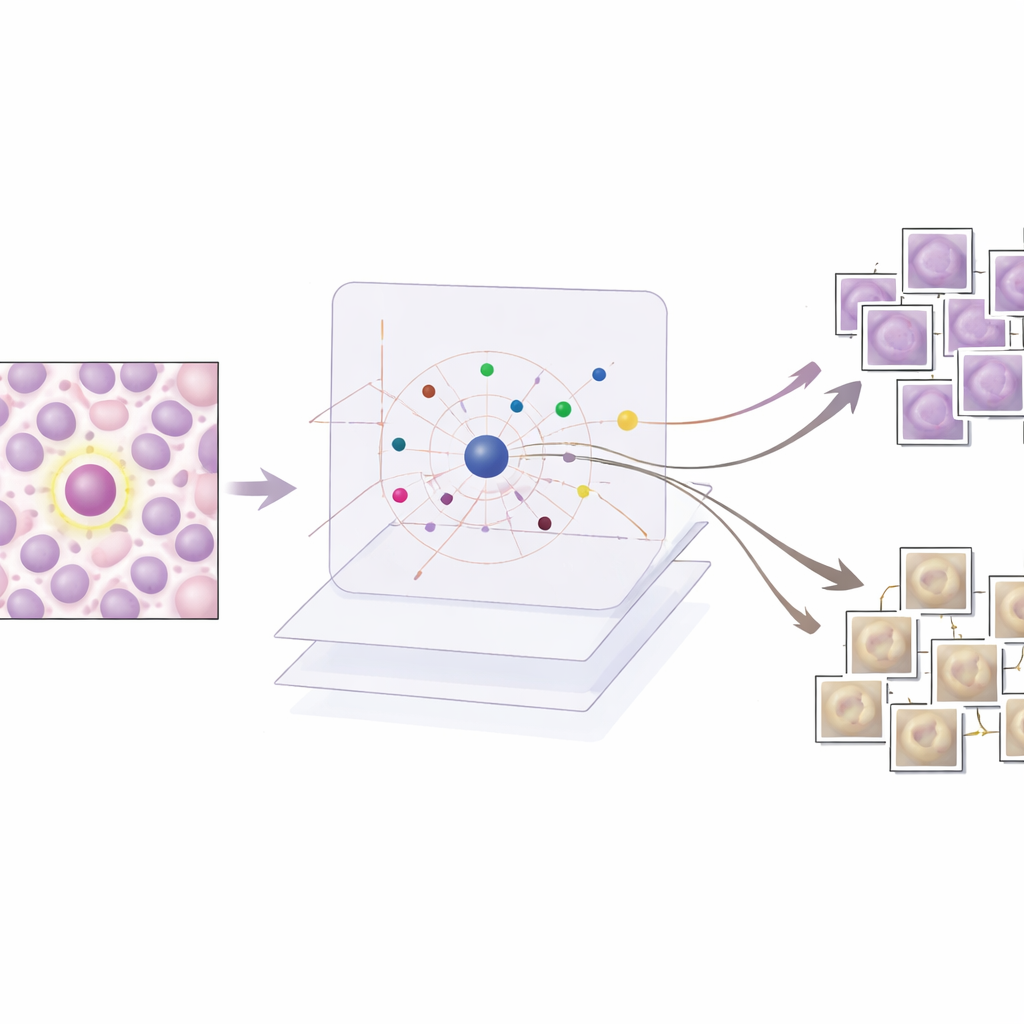
AES s’ajoute en couche d’interprétabilité au-dessus de ce détecteur entraîné, sans modifier son fonctionnement. Pour chaque région candidate marquée comme possiblement mitotique, AES consulte une bibliothèque de patchs tissulaires réels issus des données d’entraînement. De cette bibliothèque, il sélectionne un petit ensemble d’exemples « soutenant » qui ressemblent à de vraies mitoses et un ensemble d’exemples « contredisant » qui paraissent davantage non mitotiques. En coulisses, AES considère les scores de confiance du détecteur comme un paysage lisse et utilise un outil mathématique appelé fonctions de base radiale pour approximer la variation de cette confiance autour de chaque cas. Seuls les prototypes qui influencent significativement la confiance locale sont conservés, de sorte que l’explication d’une décision implique typiquement une dizaine d’exemples choisis avec soin plutôt que des centaines d’éléments à peine pertinents.
Ce que les exemples révèlent sur les décisions de l’IA
Les chercheurs évaluent AES tant quantitativement que qualitativement. Sur le plan quantitatif, ils montrent qu’un dictionnaire compact d’environ 190 images prototypes peut reproduire avec une grande précision les scores de confiance du détecteur, tout en maintenant le nombre d’exemples présentés par cas suffisamment bas pour être revu par un humain. Sur le plan qualitatif, ils examinent trois scénarios courants. Lorsque le détecteur a raison de façon évidente, AES renvoie uniquement des prototypes mitotiques qui appuient fortement la décision, ce qui rassure les cliniciens. Pour les faux positifs, la méthode met en avant des exemples mitotiques ressemblants qui expliquent pourquoi le détecteur a été trompé par des textures ou motifs de chromatine similaires, souvent accompagnés de prototypes non mitotiques plus faibles qui suggèrent une incertitude. Pour les mitoses manquées, AES tend à renvoyer principalement des prototypes non mitotiques ou des exemples ambigus, pointant des angles morts dans les données d’entraînement et indiquant où des exemples nouveaux ou mieux annotés sont nécessaires.
De la boîte noire à l’outil collaboratif
En ancrant chaque prédiction sur une poignée de patchs tissulaires réels et étiquetés, AES fait en sorte qu’un détecteur d’IA complexe se comporte davantage comme un collègue humain qui justifie ses décisions en rappelant des cas passés. Le système ne se contente pas d’indiquer si une cellule est probablement en division ; il montre aussi pourquoi et avec quelle confiance, via la combinaison et l’influence des prototypes soutenant et contredisant. Ce dispositif permet aux pathologistes de confirmer rapidement les prédictions fortes, de concentrer leur attention sur des régions limites ou confuses, et d’identifier des schémas d’erreurs systématiques qui peuvent guider un entraînement ultérieur. Bien que développé pour la détection des mitoses, la même approche pourrait s’étendre à d’autres tâches en pathologie numérique, aidant à faire évoluer l’IA d’une automatisation opaque vers un assistant interprétable, fondé sur des cas, que les cliniciens peuvent interroger, approuver et améliorer.
Citation: Banik, M., Kreutz-Delgado, K., Mohanty, I. et al. Adaptive example selection for prototype based explainable mitosis detection in digital pathology. Sci Rep 16, 9481 (2026). https://doi.org/10.1038/s41598-026-40283-2
Mots-clés: IA explicable, pathologie numérique, détection des mitoses, modèles basés sur des prototypes, diagnostic du cancer