Clear Sky Science · fr
Source pulsée ultra-intense de rayonnement ionisant basée sur l’accélération laser directe d’électrons pour étudier l’effet FLASH
Pourquoi les impulsions de radiation ultra-rapides comptent
La radiothérapie du cancer marche sur une corde raide : délivrer suffisamment de radiation pour tuer les tumeurs sans causer de dommages durables aux tissus sains. Une idée récente et prometteuse, appelée effet FLASH, suggère que l’administration d’une dose de radiation en une rafale ultra-courte et ultra-intense peut épargner les tissus normaux tout en attaquant le cancer. Cette étude présente un nouveau type de source expérimentale fondée sur un laser puissant qui génère des rafales extrêmement brèves d’électrons énergétiques, et l’utilise pour observer comment l’oxygène dans l’eau et les liquides biologiques est soudainement consommé pendant l’irradiation — un processus considéré comme central pour l’effet FLASH. 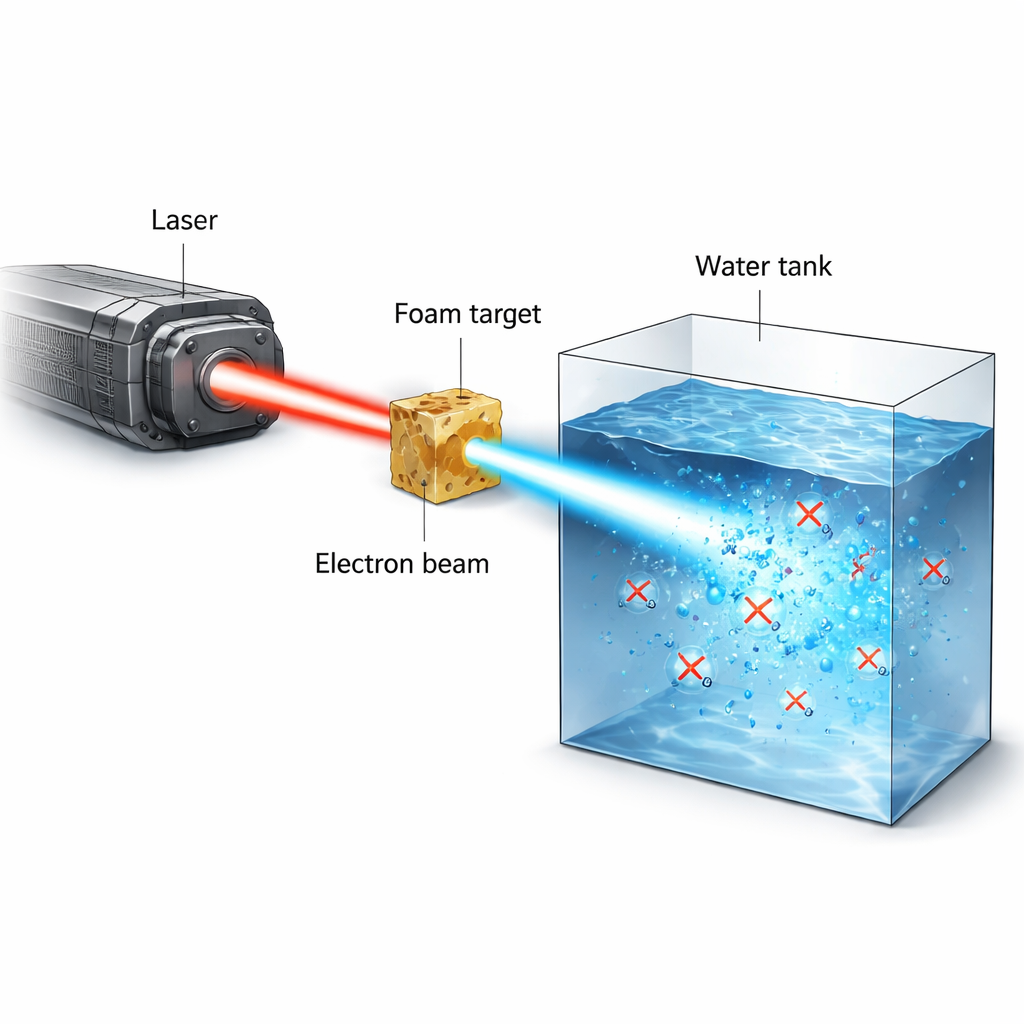
Des machines hospitalières aux faisceaux pilotés par laser
La radiothérapie conventionnelle utilise des rayons X, des électrons ou des protons provenant de grands accélérateurs. Ces machines délivrent typiquement la dose sur des millisecondes à des secondes et, bien qu’elles soient très précises, elles endommagent encore les tissus sains car la radiation provoque indirectement la rupture de l’ADN en scindant les molécules d’eau et en générant des espèces réactives de l’oxygène. L’oxygène dans les tissus sains bien vascularisés aggrave en fait ce dommage — l’effet dit de l’oxygène. La radiothérapie FLASH vise à inverser ce scénario en délivrant la dose thérapeutique complète en une fraction de seconde à des débits de dose ultra-élevés, ce qui semble protéger temporairement les tissus normaux dans des études animales sans protéger les tumeurs. Cependant, les accélérateurs médicaux standard peinent à atteindre ces débits extrêmes, ce qui motive la recherche de sources alternatives comme les lasers de forte puissance.
Transformer la mousse et la lumière en une rafale puissante d’électrons
Les chercheurs ont utilisé le laser de haute puissance PHELIX pour créer des faisceaux d’électrons étroits et à fort courant avec des énergies de plusieurs millions d’électronvolts (MeV). Le laser ionise d’abord une mousse polymère de faible densité en un plasma proche de la densité critique. Dans une seconde impulsion ultra-courte durant moins d’un billionième de seconde, le laser pousse et piège des électrons à l’intérieur d’un canal de plasma, les accélérant directement à des énergies élevées. Ce processus, appelé accélération laser directe, produit un faisceau fortement collimaté capable de transporter des dizaines de nanocoulombs de charge dans une rafale à l’échelle du picoseconde. Lorsque ce faisceau frappe de l’eau ou un matériau similaire à l’eau, il peut déposer 20–50 gray de dose en un seul tir, à des débits de dose instantanés supérieurs à 10¹³ gray par seconde — bien au-delà de ce que peuvent atteindre les machines conventionnelles.
Observer l’oxygène disparaître en un éclair
Pour sonder comment de telles rafales intenses affectent la chimie dans des conditions proches des tissus, l’équipe a construit des réservoirs d’eau scellés pouvant fonctionner en vide et être remplis soit d’eau pure, soit de milieu de culture, soit de cellules lysées, tous entièrement oxygénés au préalable. Le faisceau d’électrons a été façonné et filtré de sorte que des électrons de haute énergie dominent la dose à l’intérieur du réservoir, tandis que les protons et les rayons X étaient largement supprimés ou soigneusement pris en compte à l’aide de couches de blindage et de films radiochromiques. Un capteur optique placé sur la paroi intérieure du réservoir surveillait l’oxygène dissous en mesurant comment les molécules d’oxygène quenchent la luminescence d’une tache de colorant. Après chaque irradiation en une seule impulsion, le capteur a enregistré une chute brutale de la concentration en oxygène qui s’est ensuite lentement rétablie à mesure que l’oxygène diffusait dans la région du capteur. En combinant les données des films, les simulations et la puissance d’arrêt connue des électrons, les auteurs ont reconstruit la dose délivrée au volume irradié et l’ont liée directement à la perte d’oxygène mesurée. 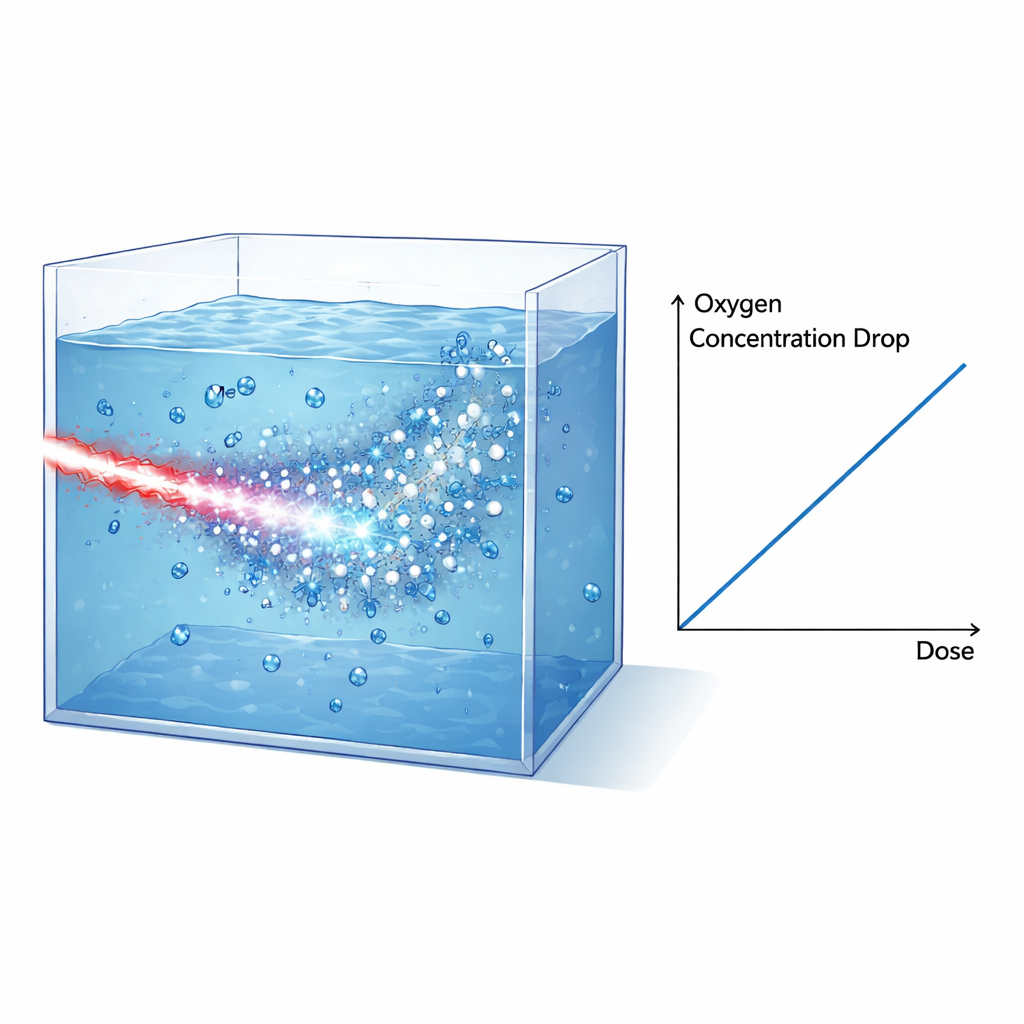
Relier expérience et théorie
La découverte clé est que la diminution d’oxygène dissous est proportionnelle à la dose délivrée tant pour l’eau que pour le milieu de culture, avec des pentes très similaires. Après correction pour une petite dose additionnelle de rayons X, la consommation d’oxygène mesurée dans l’eau est d’environ 0,32 micromole par litre et par gray. Cette valeur concorde remarquablement avec les prédictions issues de simulations détaillées de structure de piste Monte Carlo (TRAX-CHEM), qui suivent les trajectoires des électrons dans l’eau et modélisent la chimie rapide qui se déroule dans les microsecondes suivant l’irradiation. De manière cruciale, dans cette configuration pilotée par laser, presque toute la dose est délivrée en environ une picoseconde — bien plus court que les temps caractéristiques des réactions chimiques qui suivent. Cela signifie que l’expérience reproduit étroitement les conditions idéalisées supposées dans ces simulations, offrant un test rigoureux des modèles sous-jacents.
Construire un meilleur banc d’essai pour la science FLASH
Au-delà de la validation théorique, les auteurs utilisent leurs résultats pour concevoir une configuration expérimentale améliorée. En simplifiant la géométrie, en éliminant les aimants et en plaçant symétriquement l’eau et les films de mesure de dose autour du faisceau, les futurs dispositifs pourraient mesurer directement la dose à l’intérieur du réservoir sans reconstruction complexe, tout en supprimant davantage les contributions indésirables de protons et de rayons X. Les simulations montrent que modifier la cible — par exemple en ajoutant de fines couches de plastique ou d’or — permet d’ajuster la dose par tir entre environ 40 et 80 gray, offrant une plate-forme flexible pour explorer une large gamme de conditions pertinentes pour le FLASH.
Ce que cela signifie pour les traitements du cancer à venir
Pour les non-spécialistes, le message central est que cette source basée sur le laser crée des impulsions d’électrons extrêmement intenses et ultra-courtes qui imitent — et à certains égards dépassent — les conditions envisagées pour la radiothérapie FLASH. L’étude montre que ces impulsions consomment rapidement l’oxygène dissous dans l’eau et les milieux biologiques d’une manière qui concorde avec des prédictions théoriques avancées. Étant donné que l’appauvrissement en oxygène et la chimie radicalaire associée sont des candidats principaux pour expliquer pourquoi le FLASH pourrait épargner les tissus sains, disposer d’une source contrôlable et bien comprise comme celle-ci constitue une avancée majeure. Elle fournit un banc d’essai puissant pour affiner les modèles et, en fin de compte, pour orienter la conception de futures machines cliniques qui pourraient traiter le cancer plus efficacement tout en réduisant les effets secondaires.
Citation: Gyrdymov, M., Bukharskii, N., Fabian, V. et al. Ultra-intense pulsed source of ionizing radiation based on direct laser acceleration of electrons for studying the FLASH effect. Sci Rep 16, 7164 (2026). https://doi.org/10.1038/s41598-026-40281-4
Mots-clés: radiothérapie FLASH, électrons accélérés par laser, débit de dose ultra-élevé, appauvrissement en oxygène, radiolyse de l’eau