Clear Sky Science · fr
Élimination sélective des anticorps monoclonaux via le récepteur du mannose dépendante du jumelage des glycannes
Pourquoi les motifs de sucres sur les médicaments comptent
Beaucoup des médicaments vedettes actuels sont des anticorps monoclonaux — des protéines conçues capables de rester dans le sang pendant des semaines et de cibler précisément des maladies comme le cancer et les troubles auto-immuns. Mais tous les anticorps ne se comportent pas de la même façon une fois injectés. Cette étude pose une question apparemment simple mais aux grandes conséquences : comment le fin « motif de sucre » attaché à un anticorps détermine-t-il la vitesse à laquelle l’organisme l’élimine, et cela pourrait-il aussi influencer des effets secondaires tels que des réactions immunitaires ?
Les petits sucres comme feux de signalisation
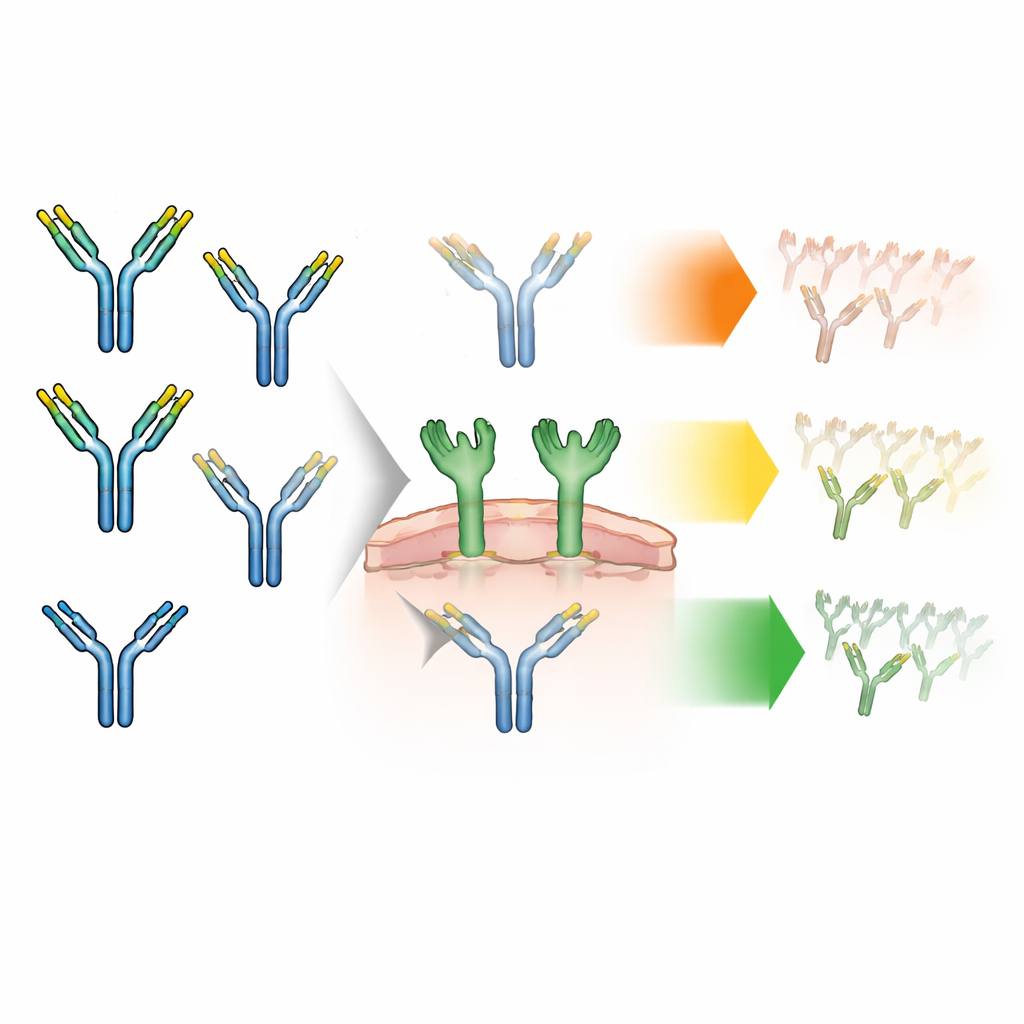
Les anticorps portent naturellement de courtes chaînes de sucres — appelées glycannes — sur leur charpente. Ces glycannes existent sous différentes formes. La plupart sont des structures « complexes », mais une minorité sont des glycannes « riches en mannose », une forme plus simple que des travaux antérieurs avaient liée à une élimination plus rapide du sang. Chaque anticorps possède deux sites glycosylés qui forment une paire, et ceux-ci peuvent être identiques (paires symétriques) ou différents (paires asymétriques). Jusqu’à présent, les fabricants se contentaient souvent de compter la proportion de chaque type de sucre au total, sans examiner comment les deux sucres d’un même anticorps étaient appariés. Les auteurs ont émis l’hypothèse que ce motif de jumelage pouvait modifier l’affinité des anticorps pour une protéine détectrice de sucres située sur des cellules immunitaires — le récepteur du mannose — et donc la vitesse à laquelle l’organisme élimine le médicament.
Trier les anticorps selon leurs paires de sucres
Pour tester cela, l’équipe a conçu des anticorps enrichis en glycannes riches en mannose puis les a physiquement séparés en trois groupes principaux : anticorps avec deux glycannes complexes, avec un glycanne complexe et un glycanne riche en mannose (asymétrique), ou avec deux glycannes riches en mannose (symétrique). Ils ont vérifié avec soin que ces groupes étaient presque identiques sur tous les autres plans : même taille, même forme, même charge et stabilité, et affinité similaire pour le récepteur de recyclage qui protège normalement les anticorps de la dégradation. Cela signifiait que toute différence observée ensuite dans des expériences cellulaires ou animales pouvait être attribuée uniquement au jumelage des glycannes, et non à des dommages cachés ou des impuretés.
Observer les cellules internaliser les anticorps
Ensuite, les chercheurs ont évalué à quelle vitesse chaque motif de sucre permettait aux anticorps d’être ingérés par des cellules exprimant le récepteur du mannose. Ils ont marqué les différentes fractions d’anticorps avec un marqueur fluorescent et les ont incubées avec des cellules humaines génétiquement modifiées pour présenter ce récepteur. Sur presque trois jours, ils ont suivi la fluorescence à l’intérieur des cellules comme mesure de l’internalisation. Tous les anticorps ont été internalisés dans une certaine mesure, mais les vitesses différaient : ceux porteurs de deux glycannes riches en mannose étaient internalisés le plus rapidement, ceux avec un seul glycanne riche en mannose avaient une vitesse intermédiaire, et ceux ne portant que des glycannes complexes étaient les plus lents. Lorsque l’équipe a ajouté de la mannan — un sucre naturel qui concurrence le récepteur du mannose — l’absorption des anticorps riches en mannose a fortement diminué, confirmant que ce récepteur était responsable d’une grande partie de l’internalisation rapide.
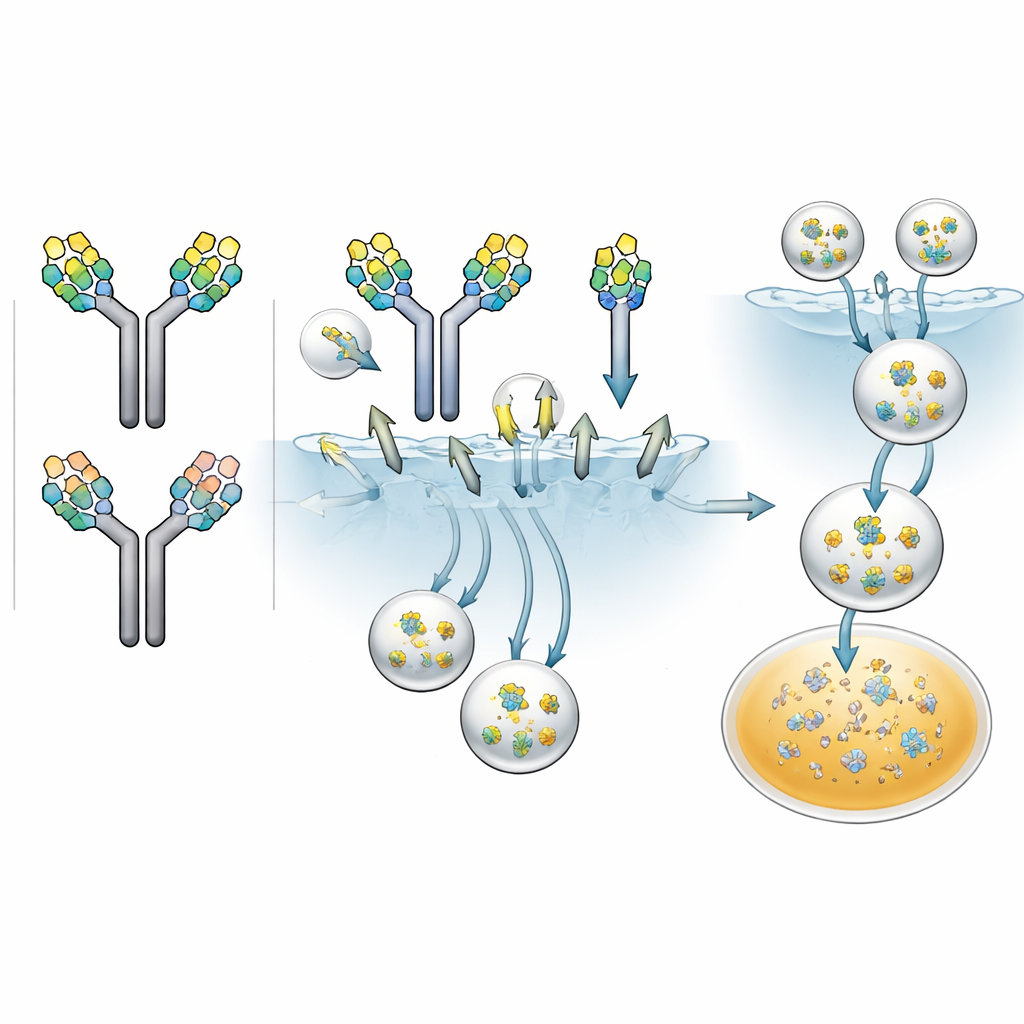
Suivre les anticorps marqués par les sucres chez des animaux vivants
Le test décisif était de savoir si ces différences cellulaires se traduiraient par un comportement réel du médicament. Les scientifiques ont formulé un produit thérapeutique riche en paires haute-mannose symétriques et asymétriques, ainsi qu’en paires uniquement complexes, et l’ont injecté à des rats. À l’aide de méthodes de spectrométrie de masse sensibles, ils ont pu suivre non seulement le niveau total d’anticorps sur deux semaines, mais aussi la décroissance de chaque type de jumelage de glycannes au fil du temps. Le schéma était net : les anticorps portant deux glycannes riches en mannose ont disparu le plus rapidement, avec une demi-vie d’environ 2,4 jours ; ceux avec un seul glycanne riche en mannose ont duré plus longtemps, environ 7,2 jours ; et ceux ne portant que des glycannes complexes ont persisté environ 17,4 jours. L’exposition au fil du temps — l’aire sous la courbe de concentration — est tombée à 38 % pour la paire double haute-mannose et à 73 % pour la paire mixte, comparées à la paire uniquement complexe. En substance, chaque glycanne riche en mannose supplémentaire fonctionnait comme un drapeau « élimine-moi » additionnel pour le récepteur du mannose.
Implications pour des médicaments plus sûrs et plus durables
Pour les patients, ces résultats éclairent pourquoi deux médicaments à base d’anticorps qui semblent similaires sur le papier peuvent se comporter différemment dans l’organisme. L’étude montre que ce n’est pas seulement la présence, mais le jumelage des glycannes riches en mannose qui oriente fortement la vitesse d’élimination, probablement via l’absorption et la dégradation médiées par le récepteur du mannose dans les cellules immunitaires. Parce que cette même voie peut également acheminer des antigènes vers les mécanismes déclenchant des réponses immunitaires, ces motifs de sucres peuvent aussi influer sur le risque d’anticorps anti-médicament et de réactions allergiques. Les auteurs soutiennent que les fabricants devraient surveiller et contrôler le jumelage des glycannes — et pas seulement la composition globale en sucres — lors de la conception et des essais des thérapies par anticorps. Cela pourrait aider à garantir des dosages plus prévisibles, des bénéfices plus durables et un risque réduit de réponses immunitaires indésirables.
Citation: Baumeister, J., Meudt, M., Wei, W. et al. Selective clearance of monoclonal antibodies via the mannose receptor is dependent on glycan pairing. Sci Rep 16, 8489 (2026). https://doi.org/10.1038/s41598-026-40268-1
Mots-clés: anticorps monoclonaux, glycosylation, récepteur du mannose, pharmacocinétique, immunogénicité