Clear Sky Science · fr
Résistance phénotypique aux médicaments et mutations identifiées par séquençage du génome liées à la résistance chez Mycobacterium tuberculosis isolés d’échantillons cliniques extrapulmonaires
Pourquoi cette étude compte pour la santé quotidienne
La tuberculose est souvent perçue comme une maladie pulmonaire, mais chez de nombreuses personnes elle attaque discrètement d’autres parties du corps, comme les ganglions lymphatiques ou la membrane entourant les poumons. Traiter ces cas est particulièrement délicat lorsque la bactérie résiste aux médicaments standards. Cette étude menée en Éthiopie montre que les méthodes de dépistage courantes passent à côté de formes importantes de résistance dans ces infections difficiles d’accès, et que la lecture du génome complet des bactéries peut dévoiler des menaces cachées et orienter de meilleurs traitements.
Infections cachées au‑delà des poumons
En Éthiopie, près d’un cas de tuberculose sur trois signalés survient en dehors des poumons, une forme appelée tuberculose extrapulmonaire. Ces patients présentent souvent des ganglions cervicaux enflés, des épanchements autour des poumons ou de l’abdomen, ou une atteinte des articulations et d’autres organes. Le diagnostic nécessite généralement des procédures invasives, et la charge bactérienne est faible, si bien que les médecins envoient rarement des prélèvements pour des tests détaillés de résistance aux médicaments. La plupart des patients reçoivent plutôt une combinaison médicamenteuse standard destinée à la tuberculose sensible aux médicaments. Cette approche est risquée si des souches résistantes sont présentes mais non détectées.
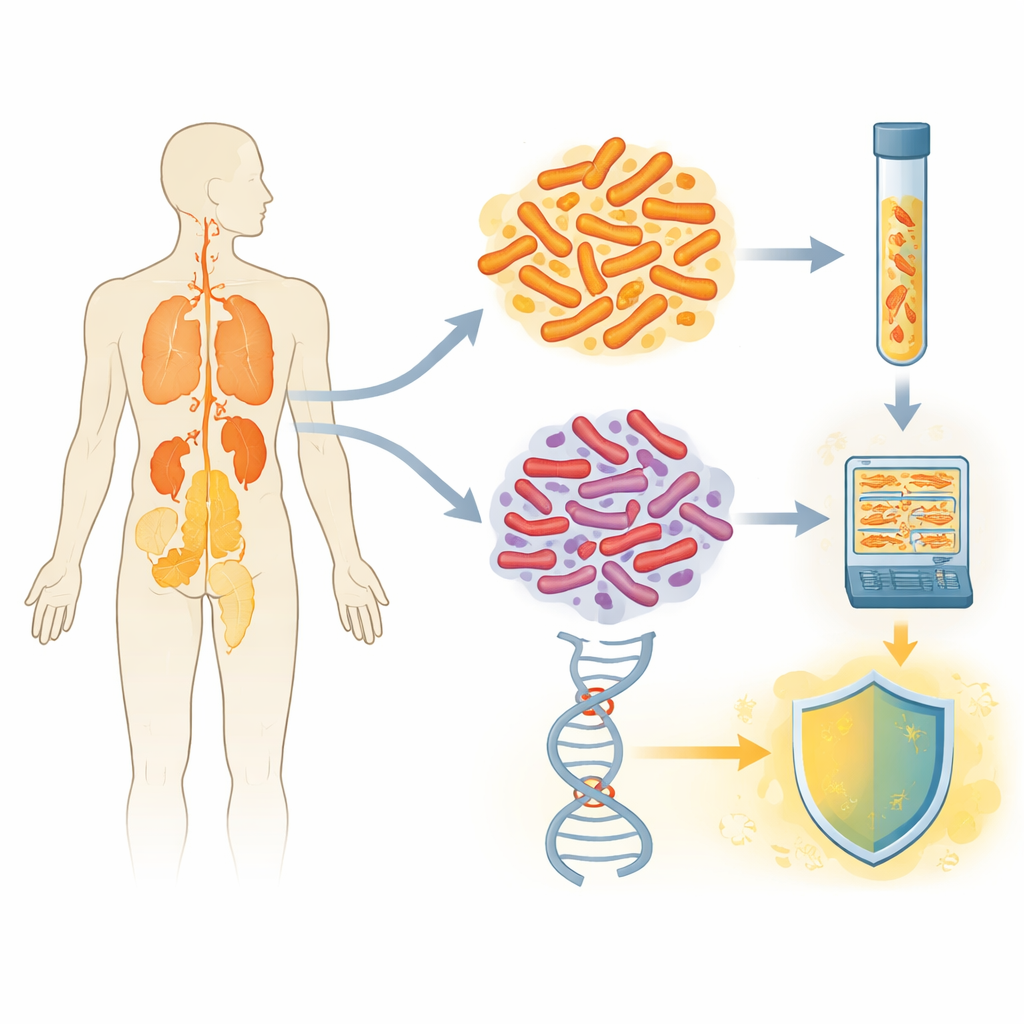
Mesurer la résistance chez de vrais patients
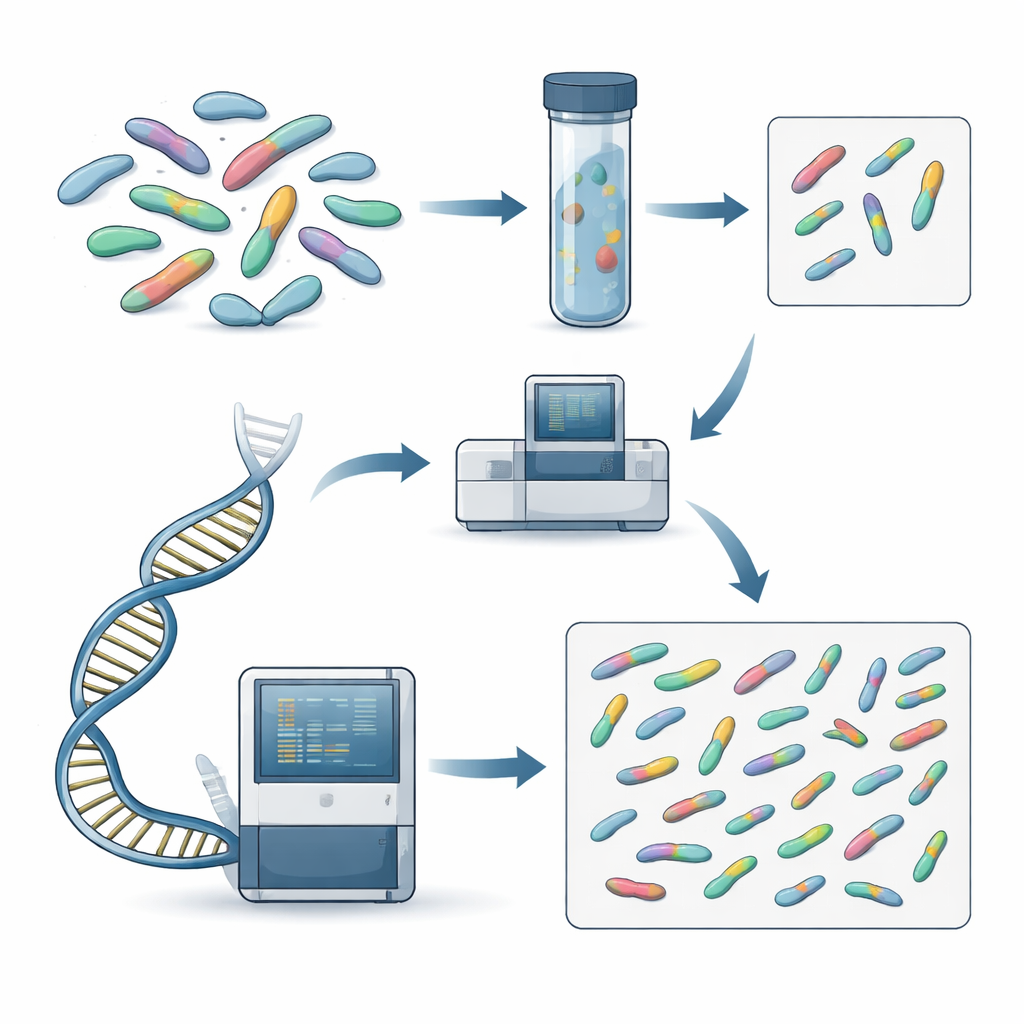
Les chercheurs ont collecté des échantillons de 189 personnes atteintes de tuberculose extrapulmonaire confirmée dans 11 hôpitaux à travers l’Éthiopie entre 2022 et 2023, principalement à partir d’aspirats ganglionnaires. Au laboratoire, ils ont d’abord utilisé un test « phénotypique » conventionnel, qui expose les bactéries aux médicaments antituberculeux en culture liquide pour voir si elles croissent. Ils ont ensuite réalisé le séquençage du génome complet sur 160 isolats bactériens, lisant presque chaque lettre de leur ADN et utilisant des programmes informatiques spécialisés pour rechercher des modifications connues liées à la résistance.
Ce que les tests génétiques ont révélé
Les tests de laboratoire standards suggéraient qu’environ 17 % des patients avaient des bactéries résistantes à au moins un médicament antituberculeux clé, et qu’environ 4 % présentaient une maladie multirésistante, c’est‑à‑dire une résistance à la fois à l’isoniazide et à la rifampicine, les médicaments piliers du traitement. La résistance était beaucoup plus fréquente chez les personnes ayant déjà été traitées pour la tuberculose. Lorsque l’équipe a examiné les génomes, elle a confirmé la plupart de ces résultats mais a aussi découvert des formes additionnelles et plus subtiles de résistance que les tests de croissance avaient manquées, en particulier concernant la rifampicine. Plusieurs patients portaient des bactéries qui semblaient sensibles en laboratoire mais présentaient des mutations « limites » bien reconnues dans le gène cible de la rifampicine. Ces cas, connus sous le nom d’infections mono‑résistantes à la rifampicine ou d’hétéro‑résistance, peuvent se comporter comme une maladie résistante dans l’organisme alors que les tests de routine les classent comme sensibles.
Nouvelles pistes dans le répertoire bactérien
En examinant l’ensemble du génome, les scientifiques ont également trouvé des mutations rares et auparavant non décrites. Ils ont identifié une nouvelle modification dans la région cible de la rifampicine et documenté une mutation dite compensatrice — un ajustement génétique qui aide les bactéries résistantes à la rifampicine à retrouver leur capacité de croissance et de propagation — chez un patient ayant un long antécédent thérapeutique compliqué. De plus, ils ont observé des modifications fréquentes dans d’autres gènes liées à la résistance aux médicaments de deuxième intention utilisés lorsque les médicaments de première ligne échouent. Globalement, le séquençage du génome concordait bien avec les tests traditionnels pour les principaux médicaments de première ligne, mais il apportait des informations complémentaires dans les cas où la résistance était limite, rare ou génétiquement complexe.
Ce que cela signifie pour les patients et les politiques
Pour les personnes atteintes de tuberculose extrapulmonaire en Éthiopie, l’étude montre que la maladie multirésistante et la résistance uniquement à l’isoniazide ne sont pas rares, et que certaines souches résistantes à la rifampicine échappent effectivement aux tests utilisés en soins de routine. Ces formes cachées de résistance peuvent entraîner des échecs thérapeutiques et une transmission continue. Les auteurs soutiennent que l’intégration d’outils modernes de séquençage dans les directives nationales — au moins dans des centres de référence — permettrait aux médecins de repérer à la fois les mutations de résistance courantes et inhabituelles, de choisir des combinaisons médicamenteuses plus efficaces et de surveiller l’apparition de souches problématiques. En termes simples, lire le plan génétique complet des bactéries peut transformer ce qui ressemble à un jeu d’hypothèses en une approche plus précise et personnalisée pour traiter l’un des plus anciens tueurs infectieux au monde.
Citation: Mollalign, H., Alemayehu, D.H., Melaku, K. et al. Phenotypic drug resistance and genome sequencing based identified mutations linked to resistance in Mycobacterium tuberculosis isolated from extrapulmonary clinical specimens. Sci Rep 16, 9160 (2026). https://doi.org/10.1038/s41598-026-40253-8
Mots-clés: tuberculose extrapulmonaire, TB résistante aux médicaments, séquençage du génome complet, résistance à la rifampicine, Éthiopie