Clear Sky Science · fr
Un pipeline automatisé d’analyse d’images pour l’imagerie redox optique grand champ d’organoïdes cancéreux dérivés de patients
Pourquoi cette étude d’imagerie du cancer est importante
Trouver le bon médicament pour le cancer de chaque personne reste un processus lent et aléatoire. Cette étude s’attaque à ce problème en combinant de petits tissus tumoraux cultivés en laboratoire à partir de patients — appelés organoïdes — avec une méthode rapide, basée sur une caméra, pour observer comment leur métabolisme énergétique évolue après l’ajout de médicaments. Les auteurs montrent comment un nouveau pipeline informatique automatisé peut parcourir de grands lots d’images de microscope, suivre des centaines d’organoïdes sur plusieurs jours et révéler quels traitements fonctionnent, le tout beaucoup plus rapidement et de façon plus fiable que ce qu’un opérateur humain pourrait faire manuellement.
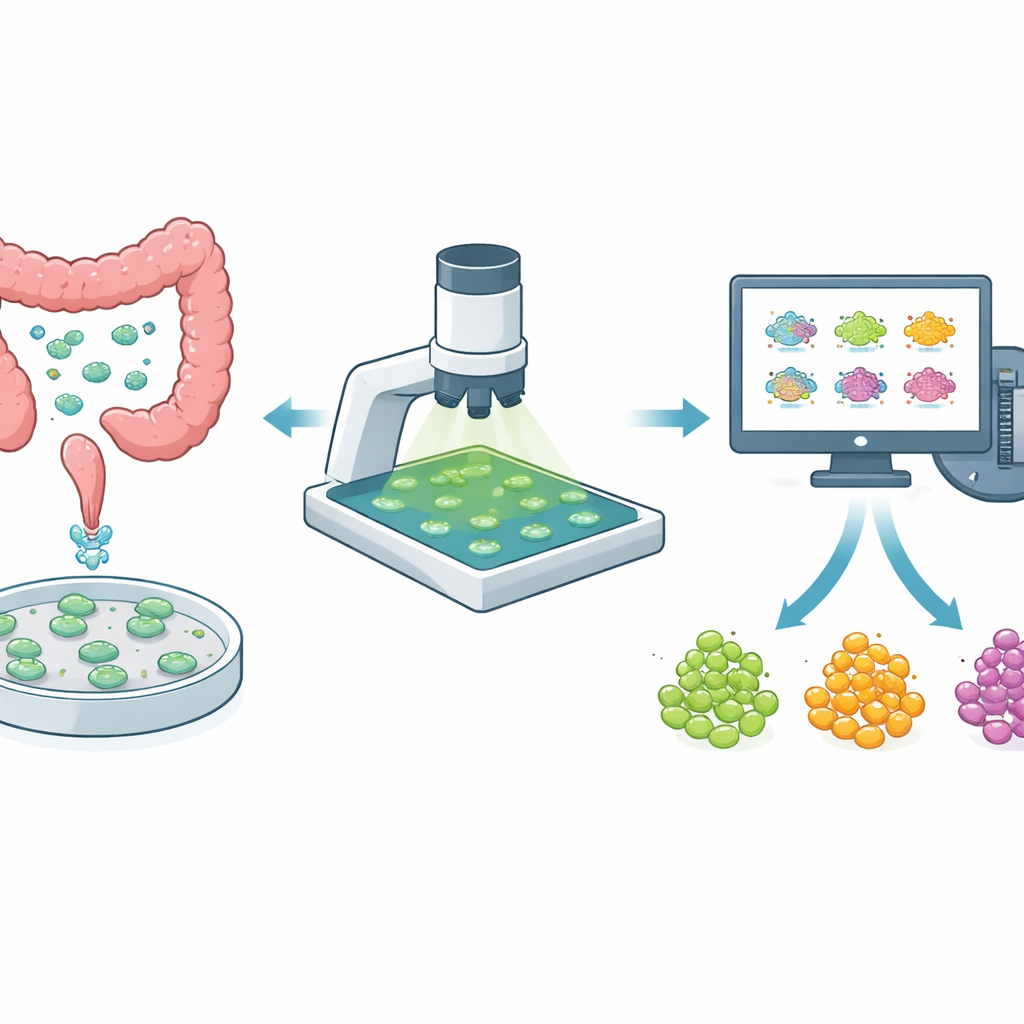
Des mini‑tumeurs en boîte comme bancs d’essai
Plutôt que de se limiter à des cellules cancéreuses cultivées en monocouche, les chercheurs utilisent désormais souvent des organoïdes tridimensionnels issus directement de la tumeur d’un patient. Ces mini‑tumeurs préservent mieux la diversité des types cellulaires et les poches de cellules résistantes aux médicaments qui existent in vivo. Pour le cancer colorectal, où les tumeurs varient fortement d’un patient à l’autre et même au sein d’un même patient, les organoïdes constituent un moyen puissant d’évaluer l’efficacité des traitements nouveaux ou existants. Mais pour être utiles à l’orientation thérapeutique, les tests sur organoïdes doivent être à la fois non destructifs — afin de pouvoir observer le même organoïde dans le temps — et suffisamment rapides pour cribl er de nombreux médicaments et concentrations.
Observer la « consommation de carburant » tumorale par la lumière
L’équipe utilise une technique appelée imagerie redox optique, qui s’appuie sur la faible fluorescence naturelle de molécules intracellulaires impliquées dans la production d’énergie. En excitant ces molécules avec des longueurs d’onde spécifiques et en collectant la fluorescence émise, un microscope grand champ simple peut saisir une cartographie de l’état d’oxydation ou de réduction de chaque organoïde — un instantané de son état métabolique. Contrairement aux microscopes haut de gamme plus complexes, ce dispositif utilise des composants standards que de nombreux laboratoires possèdent déjà, ce qui facilite son adoption. Les variations de ce signal redox apparaissent souvent avant les changements de taille des organoïdes ou la mort cellulaire, en faisant un indicateur précoce de l’efficacité d’un médicament.
Transformer des images brutes en mesures fiables
Jusqu’à présent, l’analyse de ces images demandait à un opérateur de dessiner des contours autour de chaque organoïde, de choisir visuellement des régions de fond, puis d’essayer d’identifier chaque organoïde au fil des jours. Cette méthode lente et sujette aux erreurs n’est pas adaptée aux cribles médicamenteux à grande échelle. Les auteurs ont créé un pipeline automatisé de bout en bout qui réalise trois tâches difficiles : séparer précisément chaque organoïde de son environnement, attribuer à chacun une identité cohérente sur plusieurs jours, et estimer le signal de fond d’une manière évitant le biais humain. Ils ont affiné un outil d’intelligence artificielle existant (Cellpose) pour reconnaître des organoïdes même lorsqu’ils varient en forme, taille et mise au point, puis construit un algorithme de suivi qui aligne les images prises à différents jours et assigne les organoïdes en fonction du recouvrement de leurs formes et positions.
Se focaliser sur la bordure la plus active
Les organoïdes présentent des zones distinctes : un noyau mort ou mourant, une zone intermédiaire peu active, et une bordure externe dynamique où les cellules se divisent activement et sont souvent les plus sensibles au traitement. Le pipeline découpe automatiquement cet anneau externe fin — appelé le bord d’attaque — pour chaque organoïde et calcule sa valeur redox. En suivant le bord d’attaque du même organoïde pendant trois jours de traitement avec différentes doses de romidepsine, le logiciel détecte des variations métaboliques subtiles. Les auteurs montrent que ce suivi organoïde par organoïde réduit la variabilité par rapport à une analyse globale noyant tous les organoïdes ensemble, augmentant ainsi la puissance statistique pour discerner des effets de médicaments même lorsque les réponses varient d’un mini‑tumeur à l’autre.
Des résultats plus rapides et plus robustes pour évaluer la réponse aux médicaments
Les chercheurs ont testé leur pipeline sur des images provenant de deux systèmes de microscope différents et constaté que les contours automatisés correspondaient étroitement à ceux dessinés par des experts, et que le suivi automatique concordait avec le suivi manuel dans plus de 94 % des cas. Lorsqu’ils ont comparé les mesures globales de réponse aux médicaments, la méthode automatisée a égalé la sensibilité de l’approche manuelle tout en réduisant le temps d’analyse d’un facteur supérieur à cent — passant de nombreuses heures de travail humain à seulement quelques minutes de traitement informatique. Pour les laboratoires travaillant avec des organoïdes dérivés de patients, cela signifie qu’ils peuvent raisonnablement analyser de grandes collections d’images et révéler la réaction de chaque mini‑tumeur au traitement. À long terme, ce type d’analyse automatisée pourrait aider à rapprocher les tests thérapeutiques basés sur les organoïdes de la clinique, soutenant une prise en charge du cancer plus personnalisée et efficace.
Citation: Hsu, A., Samimi, K., Gillette, A.A. et al. An automated image analysis pipeline for wide-field optical redox imaging of patient-derived cancer organoids. Sci Rep 16, 9757 (2026). https://doi.org/10.1038/s41598-026-40249-4
Mots-clés: cancer colorectal, organoïdes dérivés de patients, imagerie redox optique, analyse d’images automatisée, réponse aux médicaments