Clear Sky Science · fr
Évolution moléculaire et diversité de l’ARN polymerase dépendante de l’ARN du norovirus
Pourquoi les gastro-entérites nous surprennent toujours
Le norovirus est le tristement célèbre virus de la « grippe intestinale » capable de mettre hors service des paquebots, des écoles et des hôpitaux en quelques jours. Il se propage facilement, rend malade des centaines de millions de personnes chaque année et engendre constamment de nouveaux variants. Cette étude examine les mécanismes de cette évolution en se concentrant sur une seule enzyme virale — une « machine à copier » interne appelée ARN polymérase — pour comprendre comment elle change au fil du temps et quelle est sa stabilité réelle. Comprendre ce moteur caché du changement peut aider à expliquer pourquoi certaines souches de norovirus dominent à l’échelle mondiale et à orienter la conception de futurs antiviraux.
La machine interne de copie du virus
Le norovirus porte son matériel génétique sous forme d’ARN et dépend d’une enzyme, l’ARN polymérase dépendante de l’ARN, pour copier cet ARN à l’intérieur des cellules infectées. Cette enzyme, longue d’environ 510 acides aminés, ressemble à une main enroulée avec des doigts, une paume et un pouce, formant un canal où l’ARN et les nouveaux éléments constitutifs passent. Dans cette structure se trouvent sept petits « points chauds » presque identiques entre les souches ; ces régions effectuent la chimie centrale de la copie du génome. Parce que la polymérase est essentielle à la reproduction virale, même de petites perturbations dans ces points chauds peuvent être désastreuses pour le virus, si bien que l’évolution tend à les préserver avec un soin extrême.
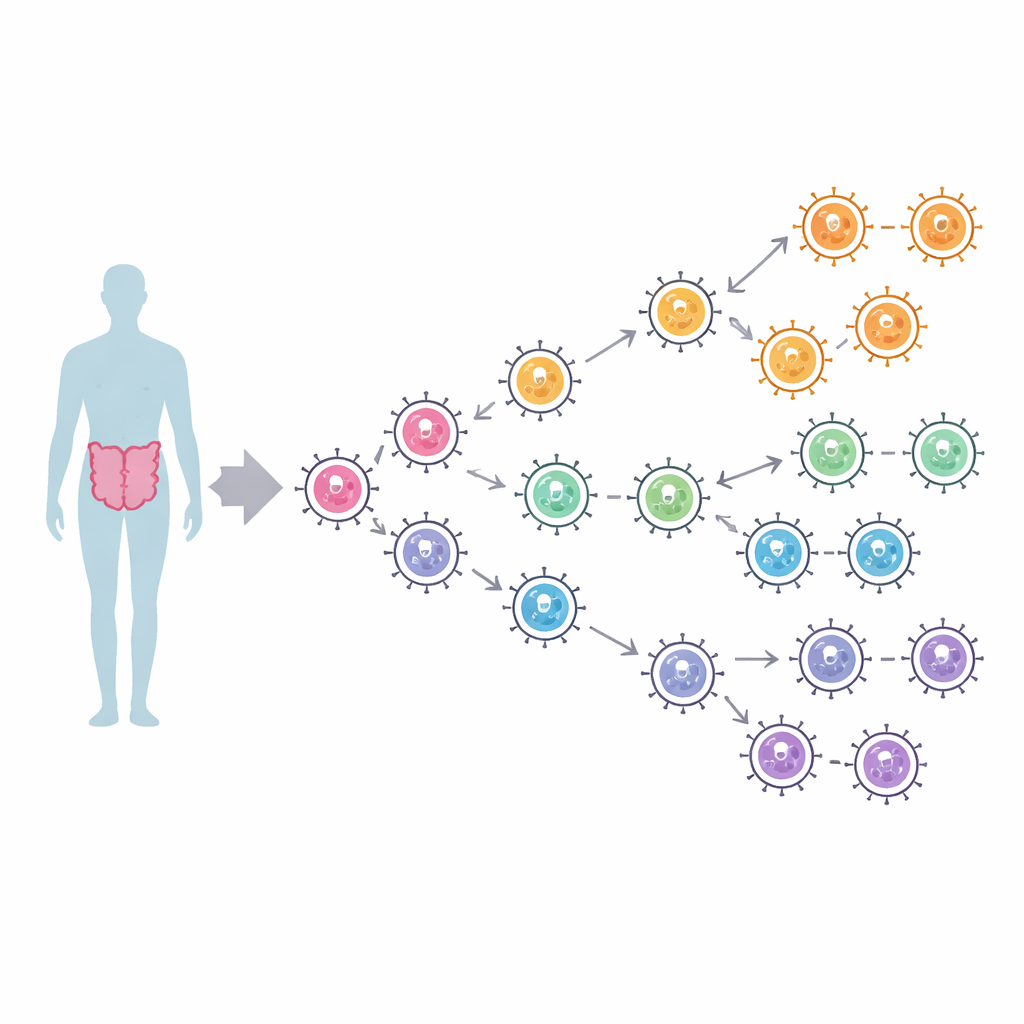
Des centaines de souches, quelques familles clés
Les chercheurs ont rassemblé 1 094 séquences complètes de la polymérase provenant de deux grands groupes de norovirus humains, appelés GI et GII, collectées dans le monde entre 1972 et 2024. À l’aide d’arbres phylogénétiques computationnels intégrant à la fois les dates et les lieux d’échantillonnage, ils ont retracé la façon dont ces enzymes se sont ramifiées sur près de quatre siècles. Les polymérases GI se répartissent en trois lignées principales qui se seraient séparées à partir d’environ les années 1600, tandis que les polymérases GII forment quatre lignées, incluant une branche distincte pour un type connu sous le nom de P16. Les infections modernes sont dominées par deux types de polymérase GII, P16 et P31, historiquement associés au génotype de capside pandémique de longue date GII.4. Pourtant, malgré une diffusion mondiale, les arbres n’affichent que peu de regroupement géographique — des souches de différents continents se mélangent — ce qui suggère que le norovirus circule rapidement à l’échelle mondiale sans rester confiné à des régions particulières.
Un changement lent et régulier avec des noyaux bien protégés
En comparant les acides aminés à chaque position de la polymérase, l’équipe a répertorié des milliers de substitutions entre types. Ils ont trouvé beaucoup moins de changements dans GI que dans GII, reflétant en partie un nombre moindre de séquences disponibles, mais un schéma clair est apparu : les sept points chauds conservés et le site de liaison à l’ARN à proximité ont été presque intacts. Lorsqu’il y avait des substitutions à ces endroits, il s’agissait généralement d’échanges modérés entre acides aminés chimiquement similaires, suggérant que l’enzyme tolère seulement de très légères modifications dans ces zones cruciales. La majorité des changements fréquents se regroupent dans les « doigts » et d’autres régions externes de l’enzyme, éloignées de la chimie centrale. Certaines positions ont même montré des allers-retours réversibles entre différents types de polymérase, signe d’une évolution convergente où des souches non apparentées aboutissent à des solutions similaires.
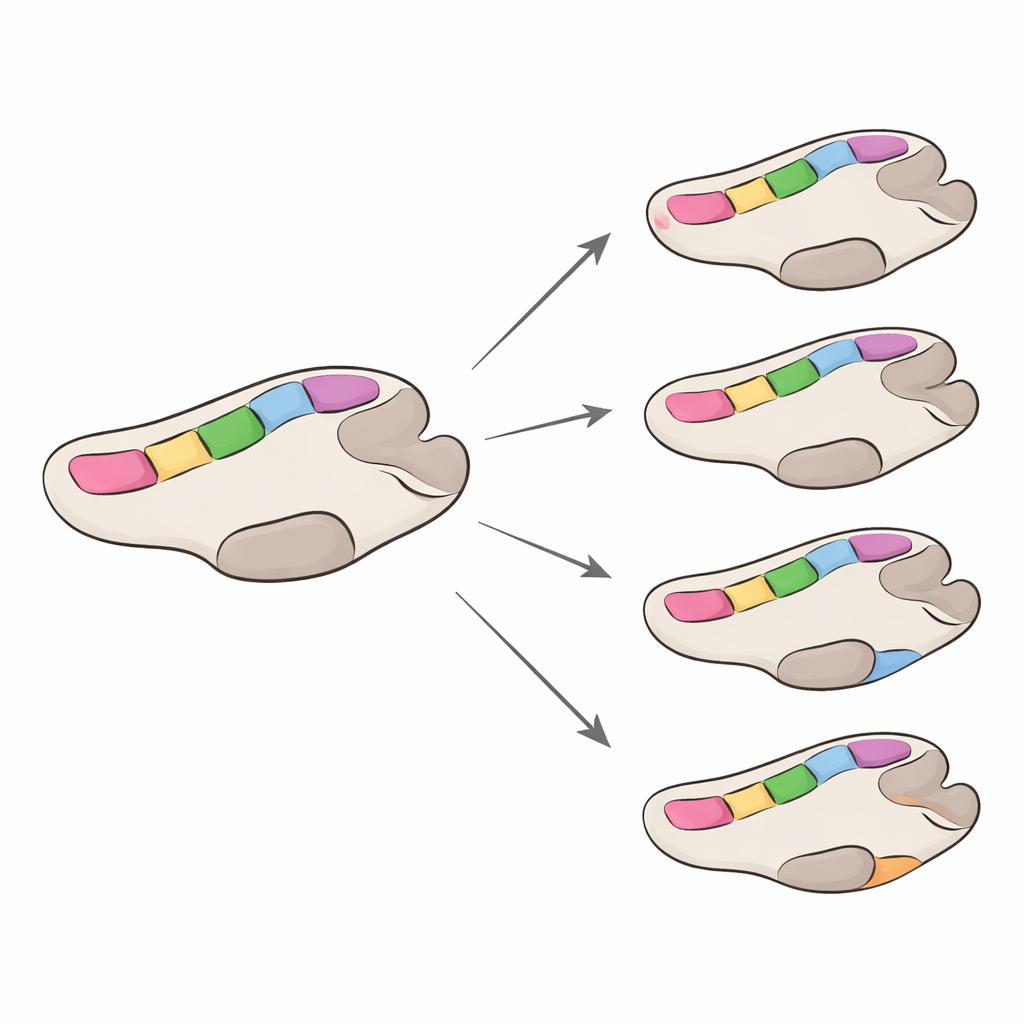
Vitesses différentes selon les familles virales
L’équipe a ensuite estimé la vitesse d’évolution de la polymérase, en se concentrant sur les changements qui altèrent les acides aminés, car ceux-ci ont plus de chances d’affecter la fonction. Globalement, les polymérases GII ont évolué environ quatre fois plus vite que les polymérases GI, bien que les deux aient évolué plus lentement que la protéine de la capside du norovirus, connue pour ses variations rapides permettant d’échapper à l’immunité. Au sein de chaque groupe, certains types de polymérase ont évolué un peu plus rapidement que d’autres, mais les différences restent modestes. De manière importante, la plupart des positions de l’enzyme sont soumises à une forte pression de « purification » — les mutations qui perturbent la fonction sont éliminées — tandis qu’un petit nombre de sites seulement montre des signes de sélection positive. Lorsque ces sites sous sélection positive ont été cartographiés sur des modèles tridimensionnels de l’enzyme, ils se situaient presque toujours en dehors des points chauds les plus conservés, bien que quelques-uns soient suffisamment proches pour potentiellement affiner la façon dont la polymérase lie l’ARN ou se déplace pendant la copie.
Implications pour les futures épidémies et traitements
Ensemble, ces résultats décrivent la polymérase du norovirus comme un noyau étonnamment stable entouré de régions plus flexibles permettant une adaptation graduelle. Les polymérases GII, en particulier celles associées à des souches historiquement pandémiques, évoluent quelque peu plus rapidement, ce qui peut aider ces virus à suivre l’évolution des hôtes et la concurrence entre variants. Pourtant, la conservation profonde des régions fonctionnelles clés sur des siècles suggère que cette enzyme constitue une cible fixe prometteuse pour les antiviraux : perturber la machinerie centrale de copie laisse peu de marge au virus pour échapper au traitement sans se handicaper lui-même. Pour les non-spécialistes, la conclusion est que si les faces externes du norovirus continueront probablement à changer, rendant de nouvelles épidémies inévitables, le moteur interne qui alimente ces changements est à la fois strictement contraint et abordable sur le plan scientifique — offrant une cible stable pour de futurs traitements.
Citation: Flint, A., Jawad, M. & Nasheri, N. Molecular evolution and diversity of the norovirus RNA-dependent RNA polymerase. Sci Rep 16, 9042 (2026). https://doi.org/10.1038/s41598-026-40248-5
Mots-clés: norovirus, évolution virale, ARN polymérase, cibles antivirales, épidémiologie moléculaire