Clear Sky Science · fr
Une plateforme modulaire pour la culture automatisée d’organoïdes et l’imagerie longitudinale
Mini organes sur puce
Imaginez pouvoir observer de minuscules versions cultivées en laboratoire d’organes humains se développer en temps réel, comme un film au ralenti montrant comment nos tissus croissent, tombent malades ou réagissent aux médicaments. Voilà la promesse des organoïdes — des amas cellulaires 3D qui reproduisent certaines caractéristiques des vrais organes. Cet article décrit une nouvelle plateforme de paillasse capable de maintenir automatiquement des organoïdes cérébraux en vie, de les alimenter et de les surveiller durant plusieurs jours sans nécessiter un incubateur encombrant. Elle ouvre la voie à des modèles de maladie plus fiables, à des tests de médicaments plus intelligents et, à terme, à une médecine plus personnalisée.
Pourquoi faire pousser des mini‑organes est si difficile
Les organoïdes sont devenus des outils puissants pour étudier le cerveau, l’intestin, le rein et d’autres organes, car ils reproduisent de nombreuses structures et types cellulaires des organes réels. Mais les maintenir en bonne santé est étonnamment délicat. Les méthodes standard reposent sur des manipulations manuelles du milieu nutritif et sur le placement des flacons sur des plateaux oscillants à l’intérieur d’incubateurs chauds et humides. Ce dispositif est gourmand en travail et peut varier d’un laboratoire à l’autre. Pire, l’environnement exigu et humide à l’intérieur d’un incubateur complique la mise en place de caméras et d’autres électroniques, si bien que les chercheurs ne peuvent généralement pas observer en continu l’évolution des tissus. Les systèmes microfluidiques existants améliorent le contrôle du milieu, mais la plupart restent confinés dans ces mêmes incubateurs, ce qui limite l’imagerie à long terme.
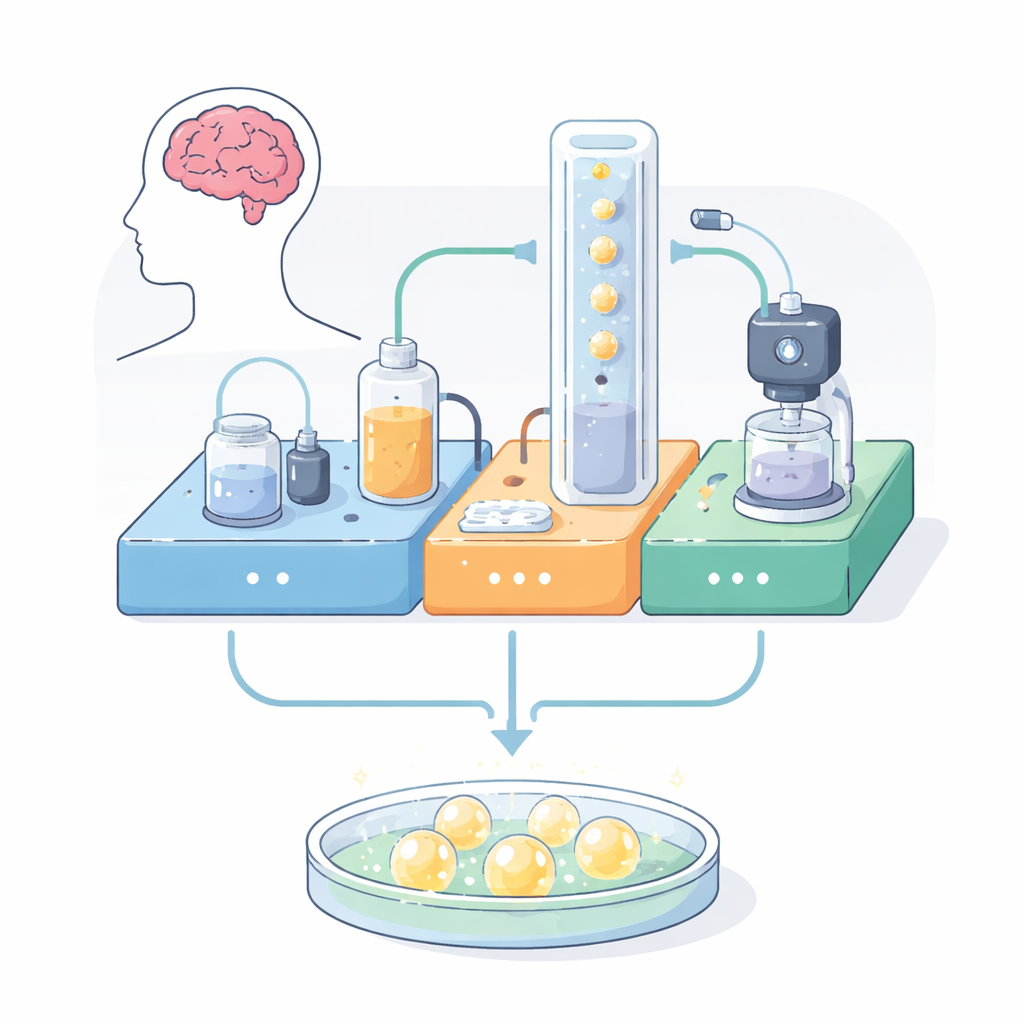
Un système de survie autonome
Les auteurs ont construit une plateforme modulaire qui rassemble trois fonctions habituellement réparties sur plusieurs appareils : alimentation automatisée, imagerie en direct et contrôle de l’environnement. Tout est monté sur une platine métallique perforée compacte à l’aide de supports imprimés en 3D et de pièces standard prêtes à l’emploi. Un module pompe un liquide nutritif chauffé dans une boucle fermée, le faisant circuler au‑delà des organoïdes tout en filtrant les impuretés. Un second module ajuste en continu la température et l’acidité, utilisant un chauffe‑eau et des injections contrôlées de bulles de dioxyde de carbone pour maintenir des conditions proches de celles du corps. Un troisième module place un petit microscope numérique près de la chambre de culture, capturant des images en champ clair et en fluorescence et détectant même des marqueurs verts et rouges courants dans les cellules. Les trois modules communiquent entre eux via une électronique simple, autorisant des expériences longues et sans surveillance.
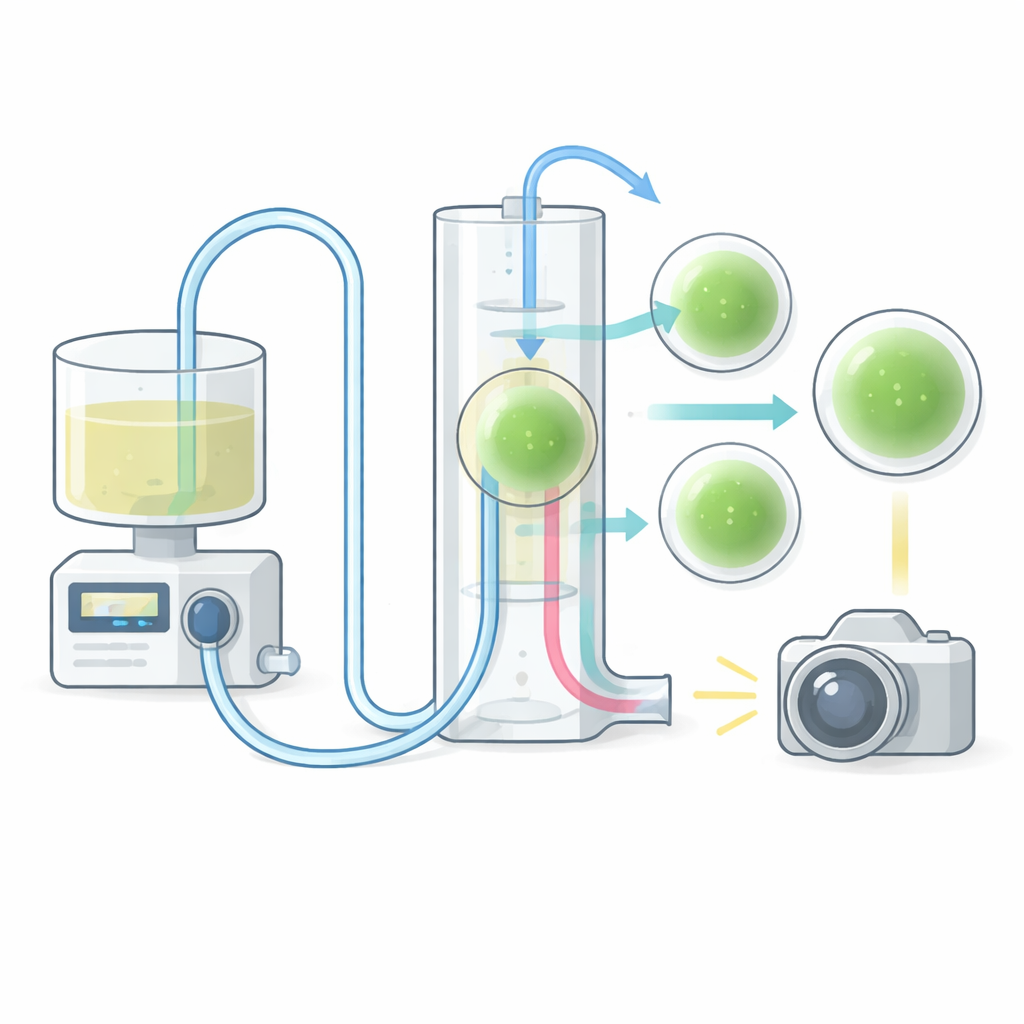
La puce verticale qui montre tout
Au cœur du système se trouve une chambre de culture sur mesure : un puits clair en silicone lié à une lame de microscope en verre. Contrairement aux plaques traditionnelles plates, cette puce est montée verticalement. Cette orientation inhabituelle permet d’observer comment le liquide circule réellement autour et au‑près de chaque organoïde, plutôt que de n’obtenir qu’un plan d’ensemble vu de dessus. Le puits comprend des canaux d’entrée et de sortie placés suffisamment haut pour éviter que les échantillons ne soient emportés, et l’ouverture est assez large pour charger des organoïdes avec une pipette de laboratoire standard tout en permettant l’échange gazeux. La puce peut être fabriquée en moins d’une journée à l’aide de moules imprimés en 3D et de matériaux peu coûteux, et elle peut être configurée en un grand puits unique ou en versions multi‑puits qui accueillent plusieurs organoïdes en série ou en parallèle. Cette flexibilité facilite l’extension des expériences ou la comparaison de différents régimes d’écoulement.
Les mini‑cerveaux restent‑ils sains ?
Pour vérifier si la plateforme soutient réellement des tissus vivants, l’équipe a cultivé des organoïdes cérébraux de souris et les a répartis entre des conditions d’incubateur standard et le nouveau dispositif. Après six jours, ils ont coloré les organoïdes avec un colorant marquant les membranes cellulaires vivantes et ont vérifié leur structure avec des anticorps dirigés contre une protéine neuronale spécifique. Les organoïdes sur la plateforme étaient aussi viables et structurés que ceux placés en incubateur, pour tous les designs de puce testés. Ils ont aussi mesuré des nutriments et des sels clés — comme le glucose, le sodium, le potassium, le calcium et le chlorure — dans le milieu de culture. Les taux sont restés stables et statistiquement indiscernables des contrôles en incubateur, montrant que le flux automatisé n’a pas stressé les tissus. Les images en timelapse ont révélé une croissance régulière de la taille des organoïdes, et les puces multi‑puits ont réduit les fusions indésirables entre organoïdes voisins, un problème fréquent dans les cultures traditionnelles.
Observer les nutriments en mouvement, en temps réel
La plateforme n’est pas seulement un système de survie ; c’est aussi une fenêtre sur la façon dont les molécules se déplacent à travers un tissu 3D. Dans une expérience, les chercheurs ont injecté par impulsion un colorant fluorescent dans la puce et ont suivi son absorption dans différentes régions d’un organoïde sur plusieurs minutes. Les motifs d’intensité obtenus concordaient avec des simulations informatiques d’écoulement et de diffusion, confirmant que l’appareil peut capturer des processus de transport dynamiques avec un haut niveau de détail. Cette capacité à aligner des films réels de pénétration de colorants ou de médicaments avec des modèles prédictifs pourrait aider à optimiser la façon dont les thérapies sont délivrées et la manière dont les signaux formateurs de motifs sont appliqués dans des expériences mimant le développement.
Ce que cela signifie pour la suite
Concrètement, ce travail fournit un « mini‑incubateur sur une plaque » compact et abordable capable de faire croître automatiquement des organoïdes cérébraux tout en les filmant et en mesurant leur environnement. Il surmonte le compromis classique entre conserver des tissus dans un état réaliste et bien contrôlé et pouvoir observer ce qui se passe à l’intérieur. Bien que l’étude actuelle se concentre sur du tissu cérébral de souris sur environ une semaine, la même approche pourrait être étendue aux organoïdes humains et à des expériences plus longues, offrant un banc d’essai plus fidèle et plus instructif pour étudier le développement cérébral, les maladies neurologiques et de nouveaux médicaments.
Citation: Torres-Montoya, S., Hernandez, S., Seiler, S.T. et al. A modular platform for automated organoid culture and longitudinal imaging. Sci Rep 16, 9717 (2026). https://doi.org/10.1038/s41598-026-40231-0
Mots-clés: organoïdes, modèles cérébraux, microfluidique, imagerie cellulaire en direct, culture cellulaire automatisée