Clear Sky Science · fr
Caractérisation multimodale de l’initiation et de la croissance des thrombus induits par l’écoulement dans l’oxygénation par membrane extracorporelle
Pourquoi les caillots sanguins dans les appareils d’assistance vitale sont importants
L’oxygénation par membrane extracorporelle, ou ECMO, est une forme de contournement cœur–poumons qui peut maintenir en vie des patients en état critique pendant que leurs organes récupèrent. Mais faire circuler le sang dans des pompes et des tubes plastiques l’expose à des forces mécaniques sévères pour lesquelles notre organisme n’est pas conçu. Ces forces peuvent déclencher des caillots dangereux à l’intérieur du circuit, ce qui augmente le risque d’AVC, de lésions d’organes ou de défaillance de l’appareil. Cette étude visait à élucider comment, précisément, l’écoulement du sang à travers une pompe ECMO façonne la naissance et la croissance de ces thrombus, dans l’objectif à long terme de rendre l’ECMO à la fois plus sûr et plus efficace.
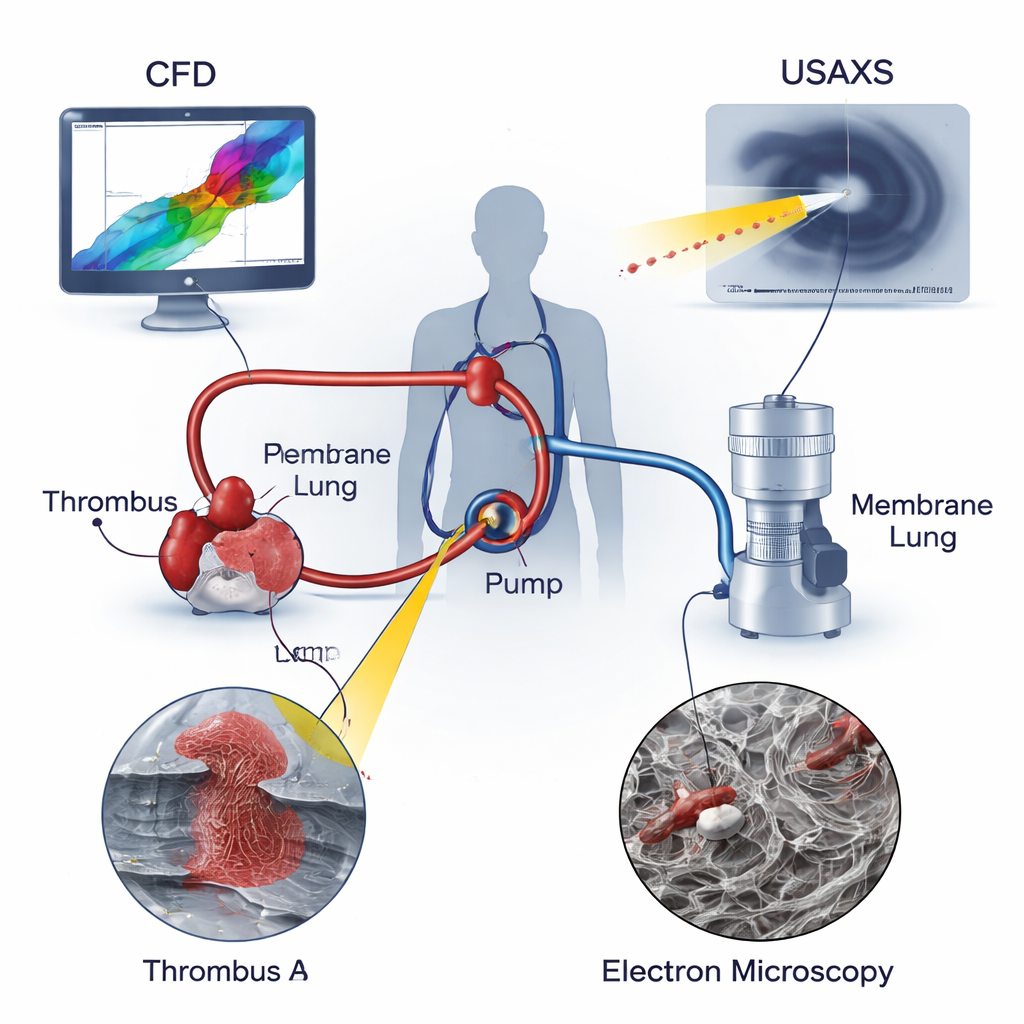
Comment l’ECMO maintient les patients en vie
En ECMO, le sang est prélevé dans une grosse veine ou artère, poussé par une pompe centrifuge à travers un « poumon à membrane » qui apporte de l’oxygène et retire le dioxyde de carbone, puis réinjecté chez le patient. Contrairement à l’écoulement lisse dans les vaisseaux naturels, l’écoulement dans un circuit ECMO comporte des conditions extrêmes : des jets très rapides, des changements brusques de direction et des poches presque stagnantes où le sang stagne. Ces environnements sont connus pour endommager les cellules sanguines et stimuler la coagulation. Les modèles médicaux classiques se concentrent sur l’écoulement lent ou l’obstruction dans les vaisseaux, mais ils ne tiennent pas pleinement compte des cisaillements et des étirements intenses que subit le sang à l’intérieur d’une pompe en rotation. Les auteurs soutiennent que pour comprendre véritablement le risque de thrombose en ECMO, il faut étudier à la fois les forces mécaniques dans le dispositif et la structure microscopique des caillots qui apparaissent.
Observer les caillots sous trois angles
Les chercheurs ont combiné trois outils puissants pour analyser deux vrais thrombus prélevés sur des circuits ECMO utilisés chez des enfants : un thrombus à l’entrée de la pompe (Thrombus A) et un autre dans la tubulure juste en aval de la pompe (Thrombus B). La dynamique des fluides numérique (CFD) a simulé le mouvement du sang à travers la pompe, révélant des zones d’écoulement recirculant et tourbillonnant et identifiant où les forces de cisaillement et d’étirement étaient maximales. La diffusion aux très petits angles par rayons X (USAXS) a sondé en profondeur chaque thrombus, mesurant la compacité et l’alignement directionnel de l’échafaudage de fibrine — le réseau protéique qui maintient les caillots — dans l’échantillon. La microscopie électronique à balayage (SEM) a fourni des images fortement agrandies des surfaces des caillots, montrant les formes des globules rouges, globules blancs, plaquettes et des fibres de fibrine environnantes. En superposant ces trois approches, l’équipe a pu relier les conditions d’écoulement locales à l’architecture interne de chaque thrombus.
Une zone de recirculation engendre un caillot rigide et aligné
La CFD a montré que la zone près de l’entrée de la pompe, où s’est formé le Thrombus A, contenait une zone de recirculation : le sang était repoussé en arrière et vers le haut le long du carter avant de rejoindre le flux principal. Cette région permettait aux composants sanguins de séjourner plus longtemps tout en subissant de fortes différences de vitesse à la frontière entre l’écoulement recirculant et l’écoulement entrant. À l’intérieur du Thrombus A, l’USAXS a indiqué une forte teneur en fibrine — au moins 70 pour cent — et un fort alignement global des fibres dans une direction privilégiée, suggérant un échafaudage dense et rigide. Les images SEM ont confirmé un réseau de fibrine étroitement tissé, parsemé de globules rouges de forme anormale et de fragments de plaquettes. Les auteurs proposent que la combinaison de temps de résidence longs et de cisaillement local élevé ait favorisé la croissance d’un caillot compact, fortement organisé et capable de résister aux contraintes mécaniques de la pompe.
Un écoulement tourbillonnant produit un caillot plus lâche et torsadé
En revanche, le Thrombus B, prélevé dans la tubulure après la pompe, s’est développé dans une région dominée par un écoulement de sortie tourbillonnant. La CFD a révélé des structures d’écoulement rotatives, en spirale, émergeant de la sortie de la pompe, et les données USAXS ont montré un réseau de fibrine toujours dominant mais moins dense et moins fortement aligné dans l’ensemble. La direction principale d’orientation de la fibrine changeait progressivement à travers le thrombus, d’un angle d’inclinaison à un autre, faisant écho au motif d’écoulement torsadé. Les images SEM montraient des fibres de fibrine d’épaisseurs variées et de nombreux globules rouges et blancs piégés, incluant des signes de lésion cellulaire et d’inflammation. De manière importante, les simulations ont aussi identifié de petites mais significatives portions du volume de la pompe où les forces d’étirement étaient suffisantes pour dérouler le facteur von Willebrand, une protéine sanguine clé qui devient adhésive sous contrainte et peut recruter rapidement des plaquettes. Ces zones étaient concentrées près des pales de l’impeller et de la sortie, ce qui en fait des sites probables d’événements d’activation initiaux ayant conduit au Thrombus B.
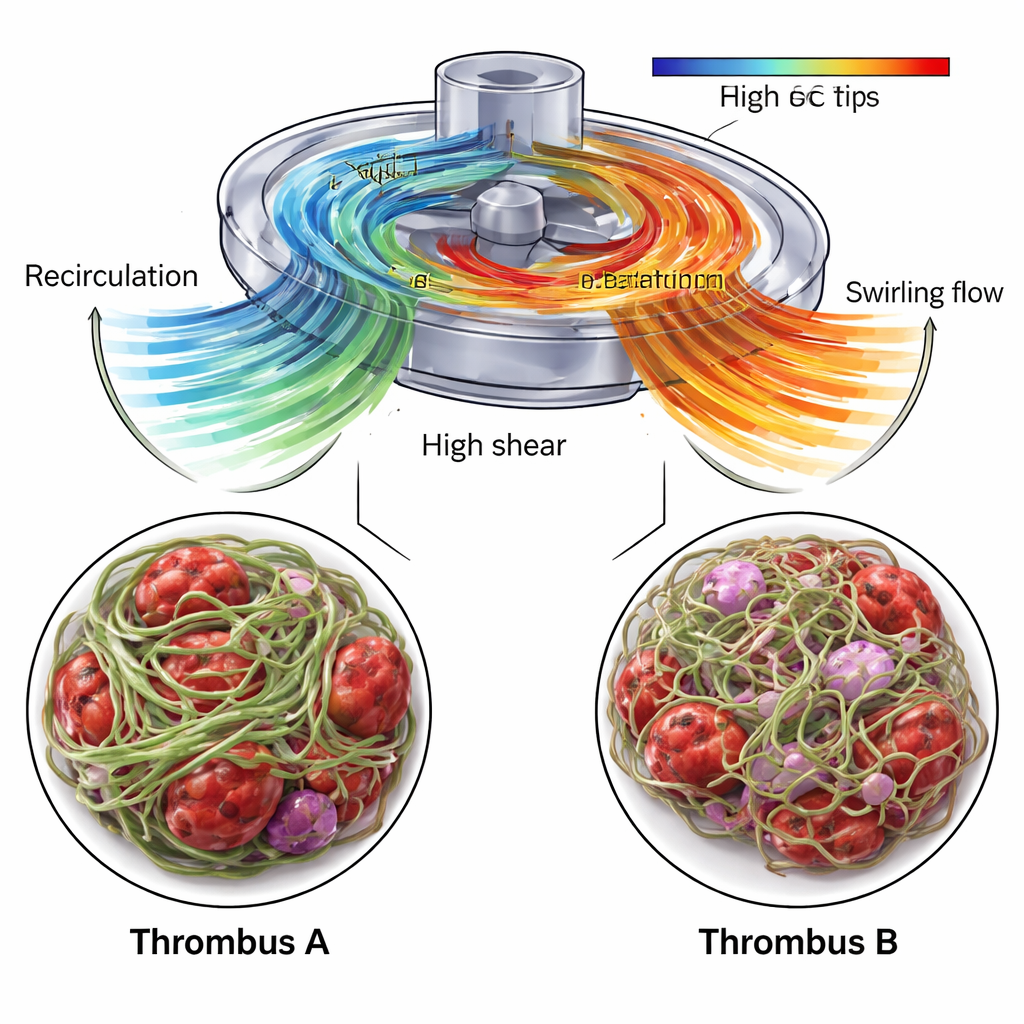
Vers des appareils d’assistance vitale plus sûrs
En combinant des simulations détaillées de l’écoulement sanguin avec des mesures par rayons X et microscopie électronique de véritables thrombus d’ECMO, ce travail montre que la « granularité » et la densité internes d’un caillot reflètent l’environnement mécanique dans lequel il s’est formé. L’écoulement recirculant près de l’entrée de la pompe était lié à un échafaudage de fibrine dense et fortement aligné, tandis que l’écoulement tourbillonnant de sortie s’associait à un réseau plus ouvert et torsadé qui piégeait néanmoins de nombreuses cellules sanguines et immunitaires. Ces observations mettent en lumière des zones spécifiques dans les pompes et la tubulure ECMO où des modifications de conception ou des ajustements ciblés de l’anticoagulation pourraient réduire le risque de thrombose de manière plus efficace. À terme, une telle cartographie multi-échelle — de la géométrie de la pompe et des profils d’écoulement jusqu’à l’organisation des protéines — pourrait orienter des conceptions d’appareils plus sûres et aider les cliniciens à mieux équilibrer les risques hémorragiques et thrombotiques durant le support ECMO salvateur.
Citation: Nilsson, F., Sochor, B., Henriksson, S. et al. Multimodal characterization of flow-induced thrombus initiation and growth in extracorporeal membrane oxygenation. Sci Rep 16, 7166 (2026). https://doi.org/10.1038/s41598-026-40177-3
Mots-clés: ECMO, coagulation sanguine, contrainte de cisaillement, pompe centrifuge pour le sang, structure de la fibrine