Clear Sky Science · fr
Réponses des cellules gliales de Müller et des microglies associées à la récupération des photorécepteurs cônes après une ablation limitée des cônes dans la rétine du poisson zèbre
Pourquoi la guérison des yeux de poisson compte
La partie arrière de l’œil, appelée rétine, transforme la lumière en vision. Chez l’humain, lorsque ces cellules sensibles à la lumière sont gravement endommagées, elles repoussent rarement, ce qui entraîne une perte de vision permanente. Le poisson zèbre est différent : il peut réparer naturellement des portions de sa rétine. Cette étude examine ce qui se passe lorsque seule une petite fraction des cellules sensibles aux couleurs du poisson zèbre est brièvement stressée ou perdue, révélant comment les cellules de soutien et les cellules immunitaires se mobilisent pour aider la rétine à récupérer. Comprendre cette chorégraphie pourrait un jour inspirer de nouvelles stratégies pour protéger ou réparer la vision humaine.
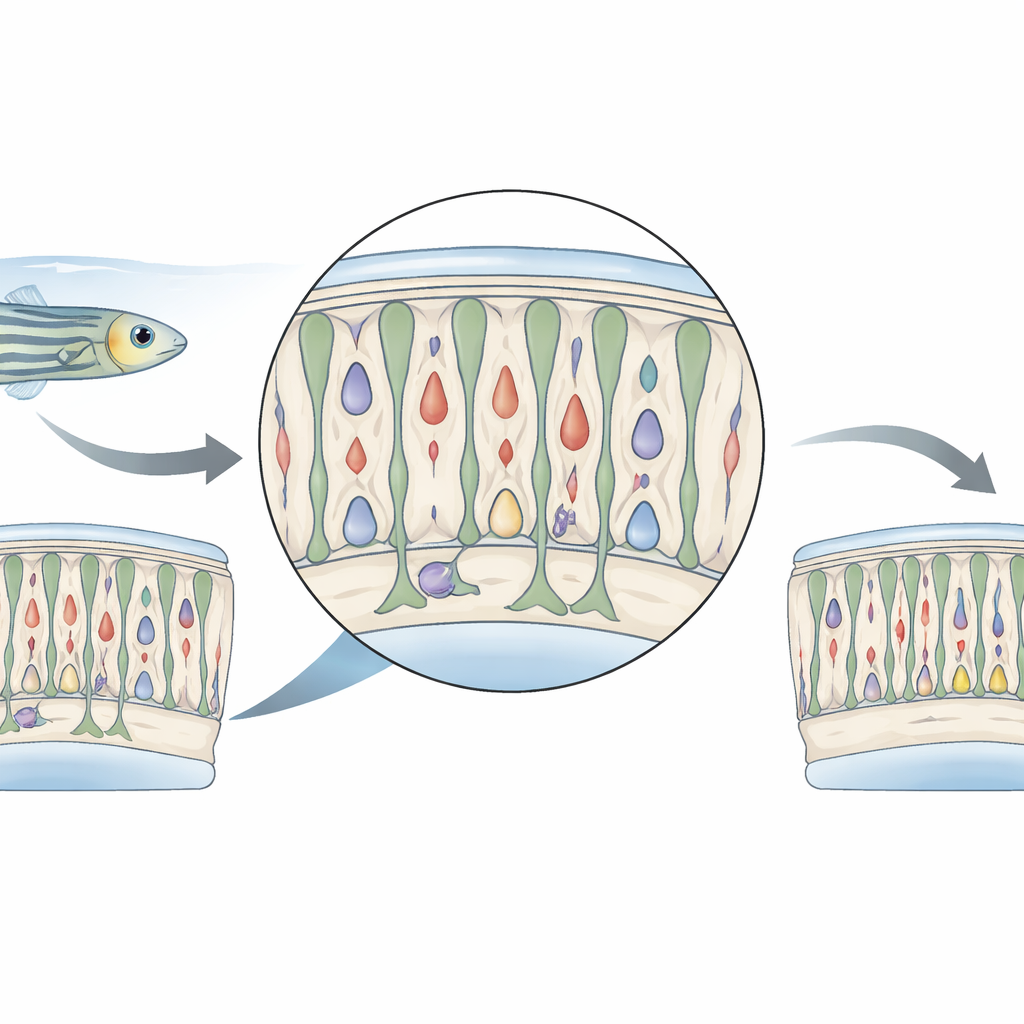
Une poussée légère pour l’œil
Les chercheurs ont travaillé avec des poissons zèbres génétiquement modifiés dont les photorécepteurs cônes — les cellules qui détectent la couleur et la lumière du jour — portent une enzyme capable de convertir un médicament inoffensif en toxine, mais uniquement à l’intérieur de ces cônes. Les poissons adultes ont été immergés pendant 24 heures dans le médicament métronidazole, puis replacés dans de l’eau propre. Plutôt que d’éliminer un grand nombre de cônes, ce traitement n’a tué qu’un petit sous-ensemble. La plupart des cônes ont survécu mais ont montré des signes de dommage temporaire : leur apparence a changé, leur signal fluorescent a diminué et un gène clé des cônes, gnat2, a été réprimé. Les poissons eux-mêmes se comportaient comme si leur vision était atténuée juste après le traitement, mais ces problèmes se sont estompés en quelques jours à mesure que la rétine commençait à récupérer.
Des cellules de couleur sous stress
Pour voir ce qui se passait à l’intérieur des cellules individuelles, l’équipe a utilisé le séquençage d’ARN monocellulaire, qui révèle quels gènes sont activés dans des milliers de cellules uniques simultanément. Ils se sont concentrés sur la période de deux à cinq jours après l’arrêt du médicament, une fenêtre pendant laquelle les cônes semblaient se rétablir plutôt que mourir. Les cônes survivants ont réduit l’expression de nombreux gènes impliqués dans la détection de la lumière et le traitement du signal, ce qui suggère qu’ils « réduisaient la puissance » de leur machinerie visuelle de façon temporaire. En parallèle, ils ont augmenté l’expression de gènes liés à la gestion des sous-produits d’oxygène nocifs et au maintien de la qualité des protéines. Ce profil correspond à un mode de réponse au stress dans lequel les cônes se concentrent sur le contrôle des dégâts et la restauration plutôt que sur des performances visuelles optimales.
Les cellules de soutien passent en mode réparation
Les principales cellules de soutien de la rétine, appelées glies de Müller, ont réagi fortement même si seule une mortalité limitée des cônes a été détectée. Ces cellules gliales s’étendent du bas jusqu’au haut de la rétine, touchant directement les cellules photoréceptrices, et il est établi chez le poisson zèbre qu’elles peuvent servir de source de nouveaux neurones après une lésion. Dans cette étude, les glies de Müller ont augmenté l’expression de gènes typiquement associés à la réactivité et au remodelage tissulaire, et beaucoup d’entre elles sont revenues dans le cycle cellulaire, signe qu’elles ont commencé à se diviser. Les auteurs ont observé l’apparition de nouvelles cellules de type progéniteur dans la couche médiane de la rétine, puis leur migration vers la couche externe qui contient les photorécepteurs. Certaines de ces réponses de réparation s’accompagnaient de basculements dans l’expression de gènes habituellement actifs dans les cellules souches, indiquant que les glies de Müller retrouvaient partiellement un état plus flexible et régénératif, même si la perte nette de cellules restait modeste.
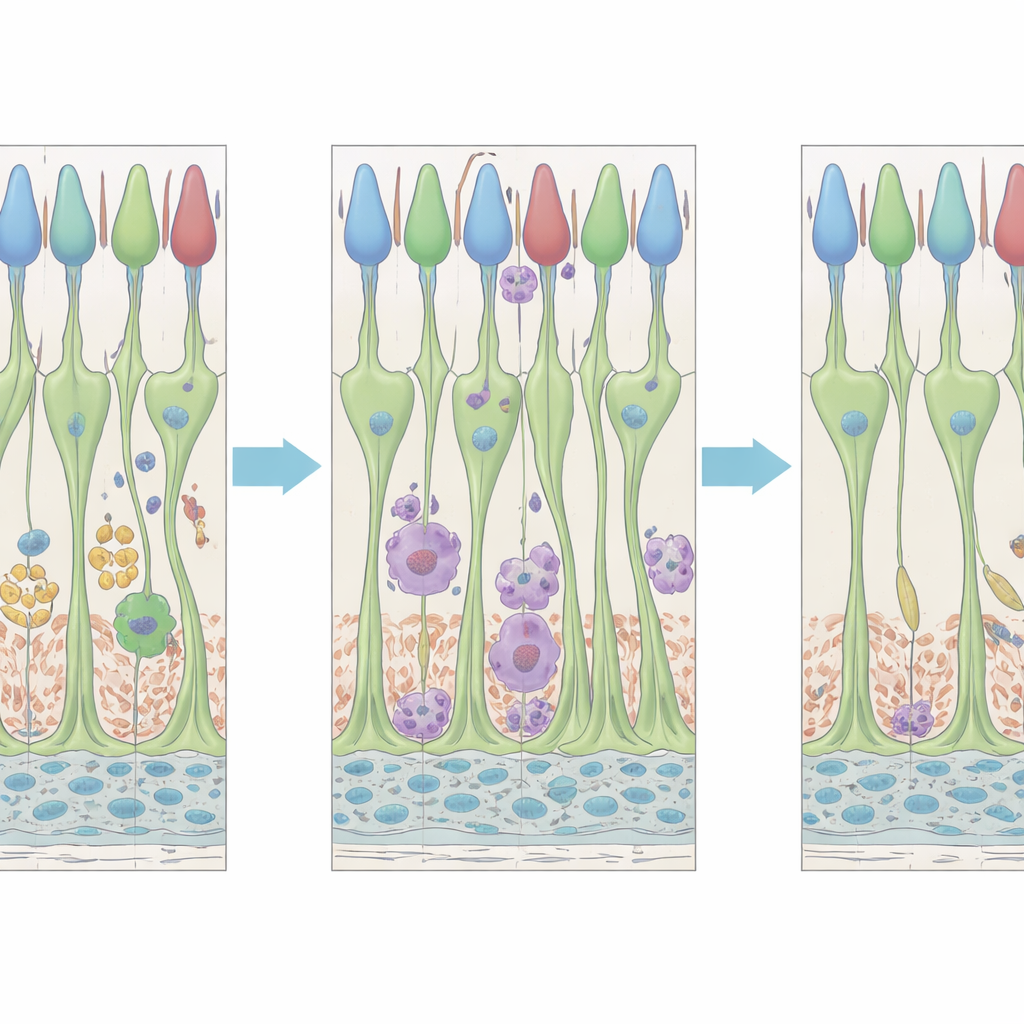
Les cellules immunitaires agissent en deux vagues
Les cellules immunitaires résidentes de la rétine, appelées microglies et autres cellules myéloïdes apparentées, ont également montré une réponse en deux étapes. Environ deux jours après le traitement, les microglies ont changé de forme, se regroupant autour des cônes mourants et aidant probablement à éliminer les débris. Plus tard, vers quatre à cinq jours, une seconde vague de comportement microglial modifié est apparue : des cellules ont été observées près des segments externes des cônes et dans l’espace proche de la couche pigmentée derrière la rétine, à un moment où les cônes montraient de forts signes de récupération. Les profils d’expression génique suggèrent qu’il existe au moins deux sous-populations microgliales distinctes avec des signatures moléculaires différentes, ce qui laisse entendre que certaines cellules immunitaires pourraient se spécialiser dans le nettoyage des cellules mourantes tandis que d’autres pourraient se concentrer sur le soutien des neurones stressés mais survivants.
Ce que cela signifie pour la protection de la vue
Ce travail montre que chez le poisson zèbre, même une perturbation limitée et brève des cellules sensibles aux couleurs suffit à déclencher une réponse coordonnée des cellules de soutien et des cellules immunitaires. Les cônes réduisent temporairement leur fonction visuelle tout en activant des programmes de réparation internes. Les glies de Müller deviennent réactives, se divisent et produisent des cellules progénitrices, et les microglies répondent en vagues temporelles liées d’abord à la mort cellulaire, puis à la récupération du stress. Ensemble, ces réponses semblent aider la rétine à restaurer sa structure et sa fonction après une agression légère. Pour les maladies oculaires humaines qui impliquent des lésions lentes et chroniques plutôt que des blessures soudaines, comprendre comment le poisson zèbre mobilise les glies et les cellules immunitaires en réponse à un stress sous-létal pourrait indiquer des voies thérapeutiques pour renforcer la capacité de l’œil à stabiliser ou même reconstruire des photorécepteurs vulnérables.
Citation: Weimar, H.V., Farre, A.A., Rumford, J.E. et al. Müller glial and microglial responses coupled to recovery of cone photoreceptors following limited cone ablation in zebrafish retina. Sci Rep 16, 9058 (2026). https://doi.org/10.1038/s41598-026-40141-1
Mots-clés: rétine de poisson zèbre, photorécepteurs cônes, glie de Müller, microglie, régénération rétinienne